Clear Sky Science · sv
Ytmodifierade liposomala nanopartiklar med två läkemedel riktade mot tumörer för att övervinna terapeutisk resistens vid glioblastoma multiforme
Varför denna hjärntumörforskning är viktig
Glioblastom är en av de dödligaste formerna av hjärntumör. Även med kirurgi, strålning och cytostatika lever de flesta patienter bara drygt ett år efter diagnos. Ett stort problem är att standardläkemedel ofta inte når tumören i hjärnan, och även när de gör det anpassar sig tumören snabbt och blir resistent. Denna studie undersöker en ny metod för att smuggla flera läkemedel förbi hjärnans naturliga barriärer och koncentrera dem inne i tumören, med målet att göra befintliga behandlingar som strålning avsevärt mer effektiva.
En liten leveransbil för cancerläkemedel
Forskarna byggde ultramindre läkemedelsbärare kallade tumörriktade liposomer. Dessa är mjuka, fettbaserade bubblor på miljarddelsmeterskala som kan hålla läkemedel inuti. Teamet modifierade ytan på dessa bubblor med en särskild peptid som känner igen och fäster vid glioblastomceller, vilket hjälper partiklarna att söka sig till tumörer istället för frisk vävnad. Varje bubbla designades för att bära ett par cancerläkemedel samtidigt: antingen everolimus plus vinorelbin, eller rapamycin plus vinorelbin. Idén är att de två läkemedlen angriper tumörceller på kompletterande sätt, medan det skyddande skalet hjälper läkemedlen att överleva i blodbanan och smyga in i hjärnan.
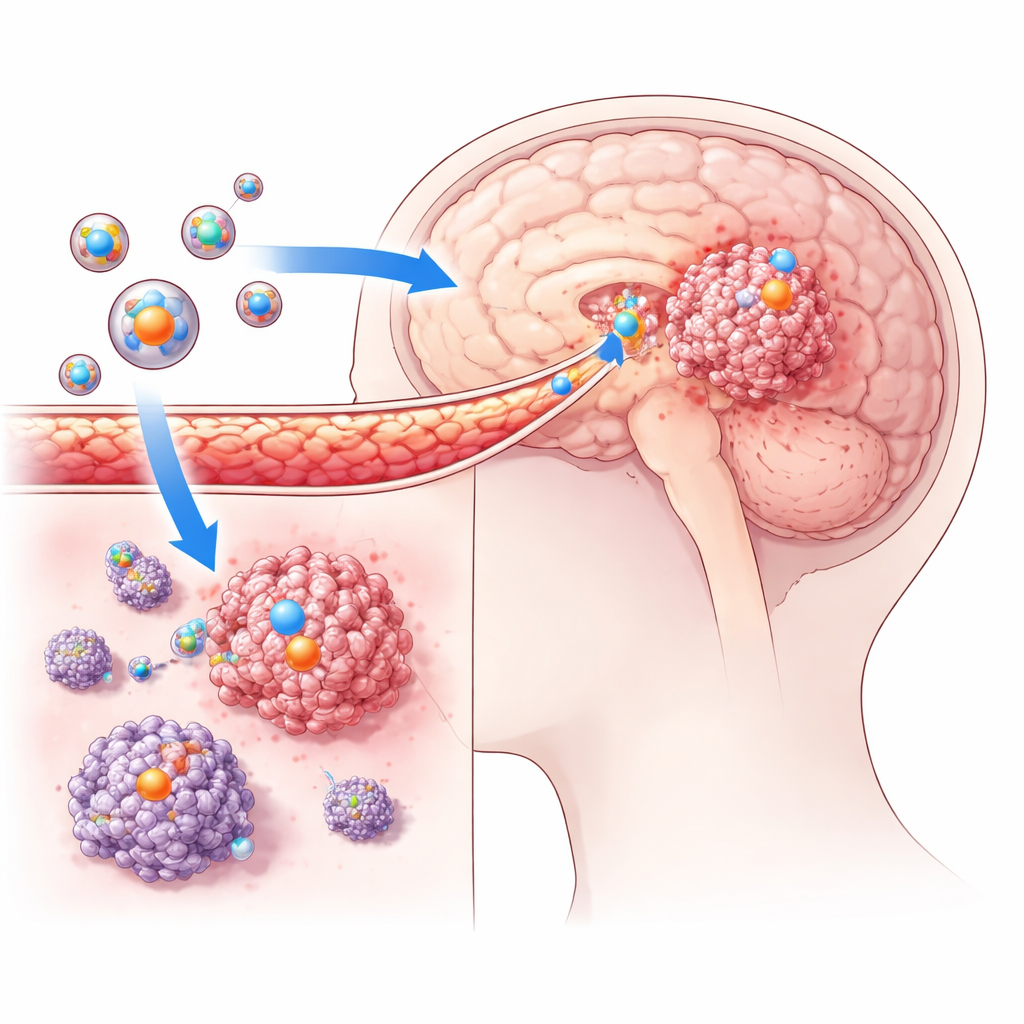
Att korsa hjärnans skyddande mur
Med hjälp av musmodeller som hade implanterade mänskliga glioblastomceller testade teamet om dessa liposomer verkligen kunde nå tumörer inne i hjärnan. De märkte partiklarna med fluorescerande färgämnen och följde deras färd med hjälp av avancerade avbildningsverktyg. Jämfört med icke-riktade liposomer visade de tumörriktade versionerna mycket starkare signaler inne i hjärntumörerna och nästan ingen signal i normala hjärnregioner. Detta bekräftade att de konstruerade partiklarna kunde korsa blod–hjärnbarriären och ackumuleras specifikt där cancercellerna växte. I cellkulturförsök tog glioblastomceller också upp mycket mer av de riktade liposomerna än kontrollpartiklarna, vilket stärker idén att yttekniken av peptiden avsevärt förbättrar tumörtropism och inträde.
Att slå hårdare mot tumören samtidigt som resten av kroppen skonas
Forskarna jämförde först hur väl enkel- respektive dubbel-läkemedelsliposomer dödade cancerceller i odlingsskålar. Dubbel-läkemedelsversionerna, särskilt kombinationen everolimus–vinorelbin, var mer potenta än något av läkemedlen ensamt och fungerade bättre än samma läkemedel utan liposomal bärare. När de kombinerades med strålning blev effekten ännu starkare: cancerceller bildade betydligt färre kolonier, rörde sig mindre och visade tecken på ökad skada. I musens hjärntumörer hade djur som behandlades med dubbel-läkemedelsliposomer plus strålning långsammare tumörtillväxt och längre överlevnad än de som fick enbart strålning, enbart liposomer eller standardkemoterapi med temozolomid. Viktigt är att forskarna inte observerade uppenbara skador i andra organ, vilket tyder på att koncentrerad behandling i tumören kan minska biverkningar.
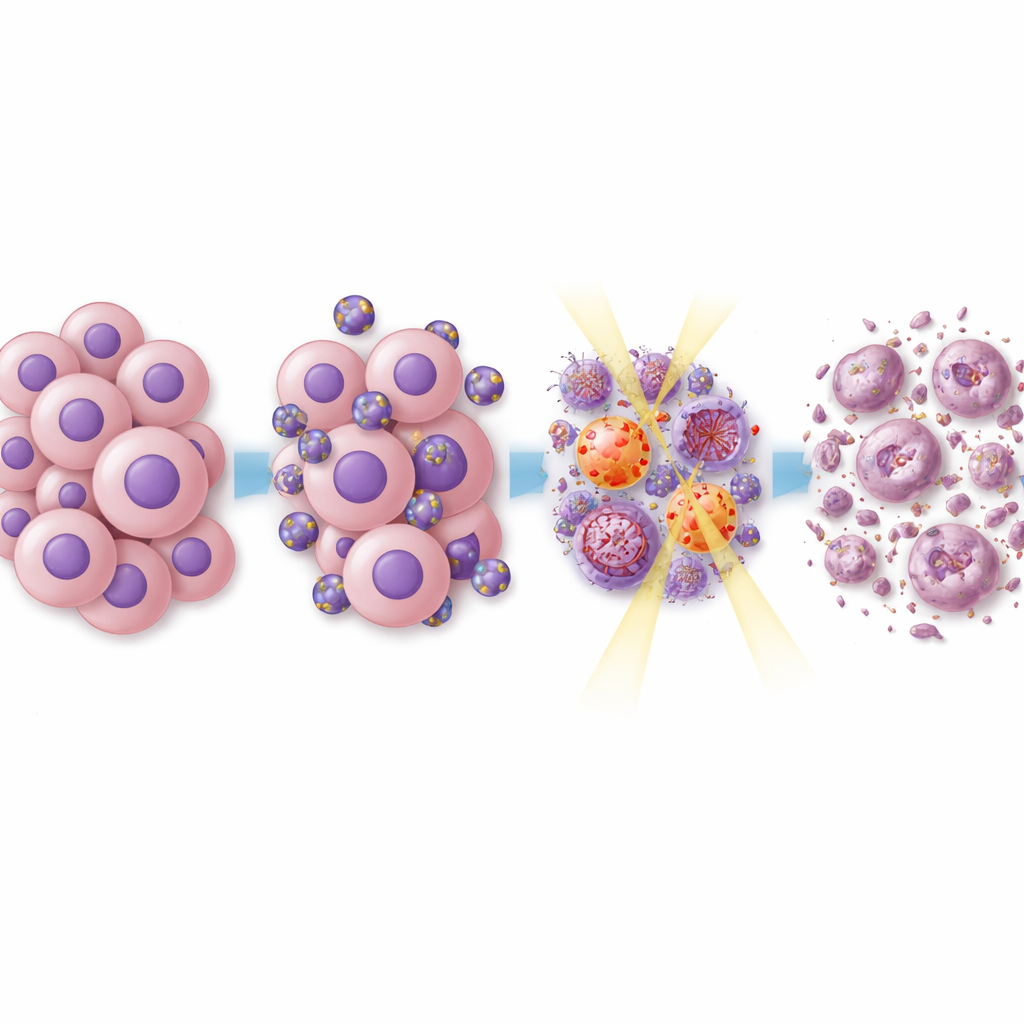
Vad som händer inne i cancercellerna
För att förstå varför detta angreppssätt gjorde tumörer mer känsliga för behandling undersökte teamet centrala signalsystem inne i cancercellerna. Everolimus och rapamycin är kända för att blockera en bana kallad mTOR, som hjälper celler att växa och motstå stress. Dubbel-läkemedelsliposomerna dämpade mTOR-relaterade signaler, liksom andra tillväxtvägar som driver glioblastomcellernas delning och rörelse. När strålning adderades minskade även proteiner involverade i reparation av DNA-skador. Det innebär att tumörcellerna hade mindre förmåga att åtgärda den genetiska skada som orsakades av strålning, vilket pressade dem mot död snarare än återhämtning. Detaljerade analyser av genaktiviteten i behandlade tumörer visade breda förändringar i nätverk kopplade till cellcykelkontroll, DNA-reparation och tumörens interaktion med immunsystemet, och många gener associerade med behandlingsresistens var nedreglerade.
Vad detta kan innebära för framtida patienter
Detta arbete visar att noggrant konstruerade, tumörriktade nanopartiklar kan föra två samverkande läkemedel över hjärnans skyddande barriär, koncentrera dem inne i glioblastom och göra strålbehandling mer effektiv. I möss bromsade strategin tumörtillväxten och förlängde överlevnaden utan uppenbar ökad toxicitet. Även om dessa resultat fortfarande är prekliniska och mycket mer testning krävs innan användning hos människor, pekar studien på ett praktiskt sätt att kombinera riktad läkemedelsleverans med befintliga behandlingar för att överlista en starkt resistent cancer. Om liknande fördelar ses hos människor kan sådana dubbelladdade liposomer en dag erbjuda glioblastompatienter längre och bättre livskvalitet.
Citering: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
Nyckelord: glioblastom, nanopartiklar, liposomer, hjärntumörbehandling, strålningssensibilisering