Clear Sky Science · sv
Subtypning av Alzheimers sjukdom och Parkinsons sjukdom med hjälp av longitudinella elektroniska journaler
Varför detta spelar roll för familjer och patienter
Alzheimers och Parkinsons sjukdom nämns ofta som om de vore enskilda, enhetliga tillstånd. Men den som sett en nära anhörig försämras vet att inga två förlopp är identiska. Denna studie ställer en enkel men kraftfull fråga: kan de medicinska journaler vi redan samlar över många år avslöja dolda “varianter” av dessa hjärnsjukdomar på ett sätt som så småningom kan leda till mer skräddarsydd vård? Genom att använda moderna mönsterigenkänningsverktyg på vårdhistorik för över 100 000 personer i Storbritannien visar författarna att både Alzheimers och Parkinsons kan delas in i fem distinkta subtyper vardera, med olika risker, symtom och sannolika framtider.
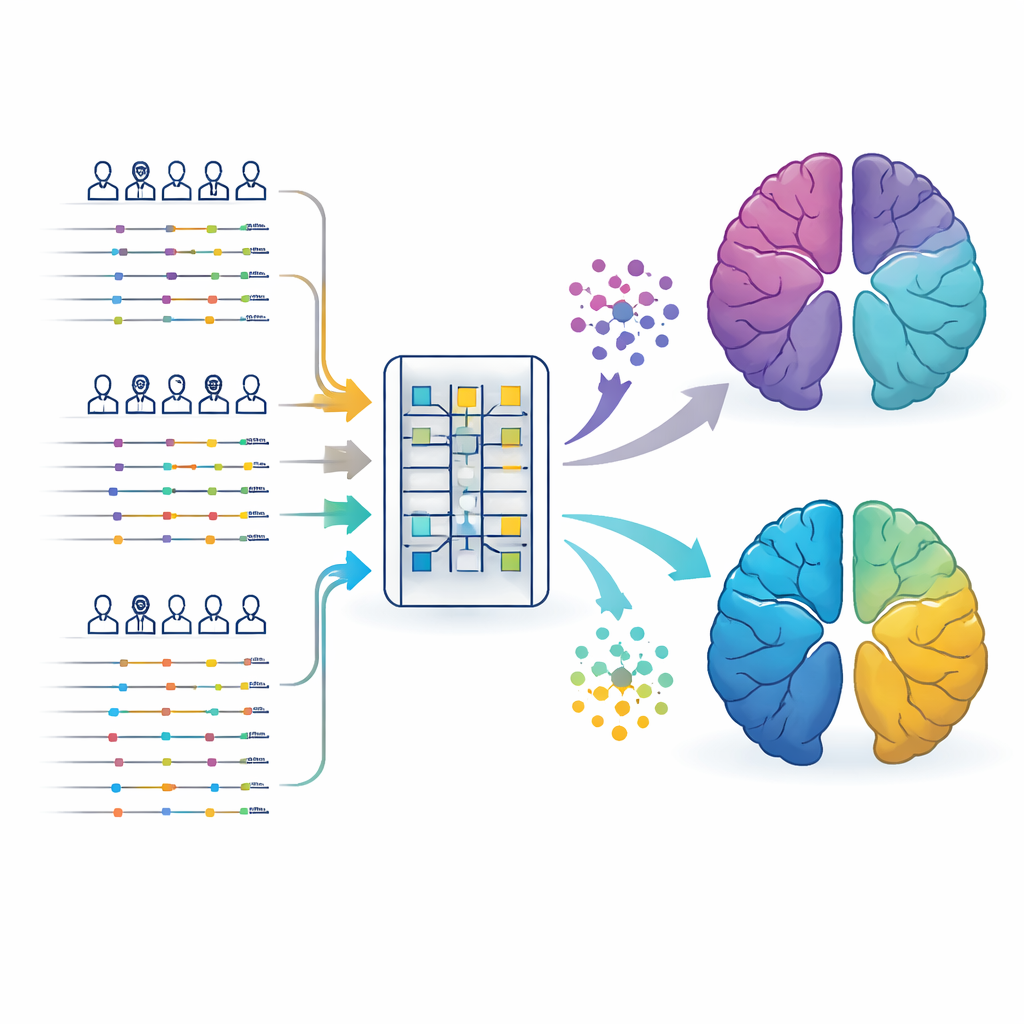
Att följa människors hälsoberättelser över årtionden
Forskarna använde anonymiserade elektroniska journaler från två stora brittiska källor: Clinical Practice Research Datalink, som innehåller uppgifter från allmänläkare, och UK Biobank, ett långvarigt forskningsprojekt som kopplar klinikbesök, sjukhusvistelser, recept och genetiska data. De fokuserade på mer än 113 000 personer med Alzheimers sjukdom och över 45 000 med Parkinsons sjukdom, var och en med omkring två till tre decenniers medicinsk historia före diagnos. Istället för att endast titta på provresultat tagna efter att hjärnsjukdomen identifierats matade teamet dessa långa, tidsstämplade hälsoberättelser in i en transformer, en typ av artificiell intelligens som är skicklig på att förstå sekvenser som språk eller, i detta fall, en tidslinje av läkarbesök.
Låta data sortera patienter i dolda grupper
Från varje persons journal skapade modellen ett kompakt numeriskt “fingeravtryck” som fångade mönster av sjukdomar, förskrivningar och tidpunkter. En klustringsmetod sorterade sedan dessa fingeravtryck i grupper utan att få förhandsinformation om vad den skulle leta efter. För både Alzheimers och Parkinsons var den mest stabila och reproducerbara lösningen fem subtyper vardera. En grupp i varje sjukdom liknade ett klassiskt, relativt ”rent” hjärntillstånd: personerna hade högre genetiska riskpoäng men få andra medicinska problem och klarade sig bättre efter diagnosen. Andra grupper formades av mönster som syntes år tidigare, såsom omfattande kärlsjuklighet, metabola problem som diabetes och fetma eller en lång historia av ångest och depression.
Olika vägar, olika utfall
De fem Alzheimers-subtyperna sträckte sig från en vanlig sen debut med färre övriga sjukdomar, till ett kärldominerat mönster med utbredd hög blodtrycksnivå, till en ”psykisk hälsa”-form präglad av framträdande depression, ångest och snabbare försämring av tänkande. En annan subtyp var starkt kopplad till diabetes, njursjukdom och tecken på kronisk inflammation, trots lägre ärftlig risk; dessa patienter blev ofta sjuka tidigare och hade högre dödlighet. En sista Alzheimers-grupp visade mer hjärtsjukdom och rörelsestörningar och hade de högsta nivåerna av sjukhusinläggning och död. Parkinsons-subtyperna ekade dessa teman: en grupp med relativt ”rena” journaler och högre genetisk risk, en dominerad av högt blodtryck och kärlsjukdom, en med allvarliga humör- och rörelsesvårigheter, en med starka metabola och inflammatoriska drag och en som kombinerade allvarliga hjärt- och rörelseproblem med särskilt dålig överlevnad.
Gener och gemensamma riskfaktorer över hjärnsjukdomar
Eftersom UK Biobank inkluderar DNA-data kunde författarna undersöka huruvida dessa kliniskt definierade subtyper också skiljer sig biologiskt. I båda tillstånden hade samtliga patientgrupper högre sjukdomsrelaterade genetiska riskpoäng än personer utan diagnos, vilket var väntat. Ändå bar vissa kluster särskilt starka eller svaga genetiska signaler. Till exempel hade en ”metabol–inflammatorisk” Alzheimers-subtyp lägre poäng för klassiska Alzheimers-riskgener och var relativt rikare på en skyddande form av APOE-genen, vilket tyder på att livslånga tillstånd som diabetes och fetma kan driva fram en demensliknande bild även när ärftlig risk är måttlig. Över både Alzheimers och Parkinsons upprepade sig subtyper formade av högt blodtryck, stroke-risk eller humörstörningar på liknande sätt, vilket antyder att blodkärlshälsa, ämnesomsättning och psykisk hälsa kan styra hjärnan mot olika degenerationsmönster snarare än att vara blotta bieffekter av åldrande.
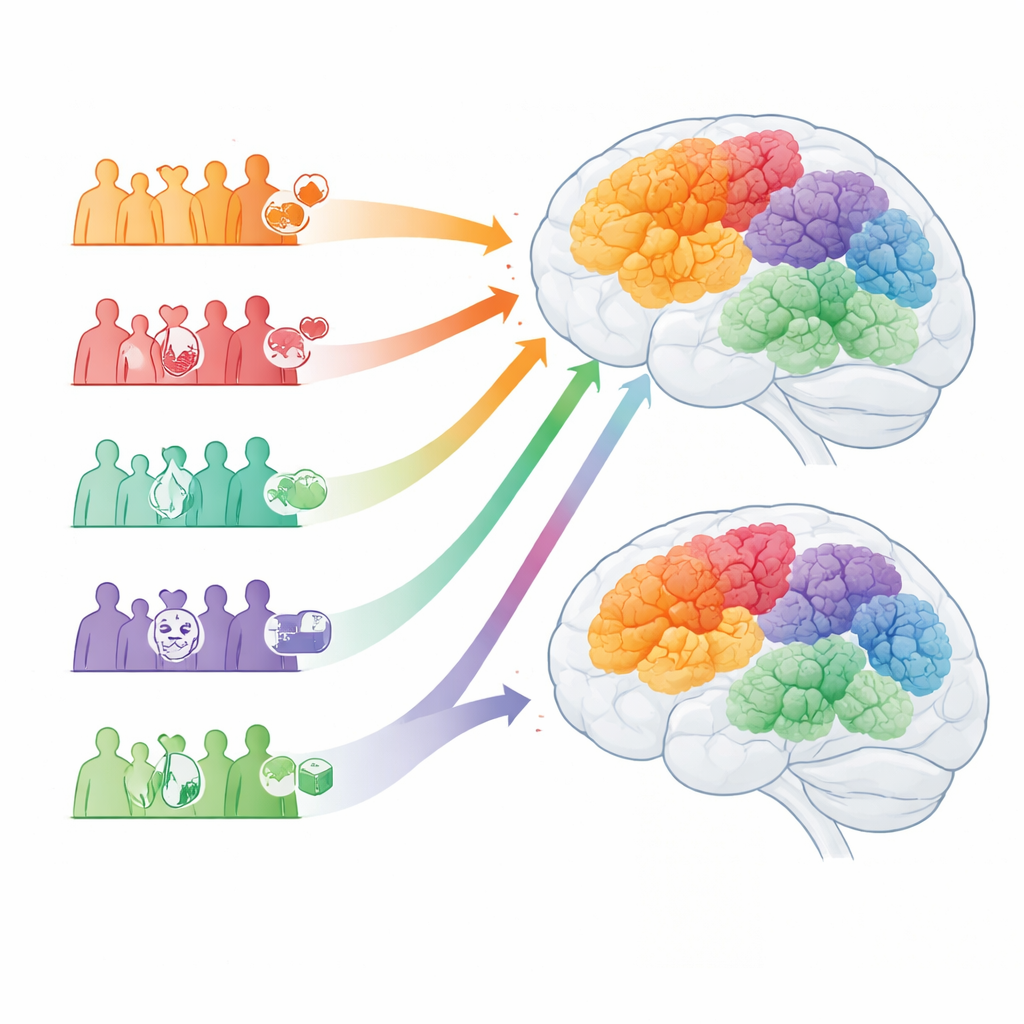
Vad detta kan innebära för framtida vård
Detta arbete ändrar ännu inte hur läkare ställer diagnos vid sängkanten, och författarna betonar att medicinska journaler i sig inte kan bevisa de exakta biologiska orsakerna bakom varje subtyp. Men genom att visa att långsiktiga rutinuppgifter naturligt faller i konsekventa, meningsfulla grupper som stämmer överens med skillnader i symtom, överlevnad och genetik erbjuder studien en modell för mer precis, tidig riskprofilering. I framtiden kan personer med vissa kombinationer av kärlsjukdom, diabetes eller psykiska problem övervakas noggrannare för specifika mönster av Alzheimers eller Parkinsons, och läkemedelsprövningar kan rikta in sig på de subtyper som mest sannolikt gynnas. Kort sagt stödjer resultaten en förskjutning från att betrakta dessa tillstånd som enstaka monolitiska sjukdomar till att se dem som familjer av relaterade men distinkta förlopp — vilket öppnar dörren för mer personanpassad prevention och behandling.
Citering: Lian, J., Fan, Z., Petrazzini, B.O. et al. Subtyping Alzheimer’s disease and Parkinson’s disease using longitudinal electronic health records. Nat Aging 6, 612–625 (2026). https://doi.org/10.1038/s43587-026-01085-3
Nyckelord: Alzheimers sjukdom subtyper, Parkinsons sjukdom subtyper, elektroniska journaler, maskininlärning inom neurologi, riskfaktorer för neurodegeneration