Clear Sky Science · sv
201‑studien: en placebokontrollerad randomiserad fas 2‑studie om säkerhet och tolerans av c‑Abl‑kinashämmaren risvodetinib vid obehandlad Parkinsons sjukdom
Varför denna studie betyder något för familjer som står inför Parkinsons
Parkinsons sjukdom berövar människor gradvis rörelsefrihet och självständighet, och dagens läkemedel lindrar i huvudsak symtom utan att förändra sjukdomens förlopp. Denna studie prövade en ny tablett, risvodetinib, hos personer med tidig, obehandlad Parkinsons för att se om den var säker och om den eventuellt kunde börja angripa sjukdomen vid dess rötter. Istället för att bara dölja skakningar eller stelhet syftar läkemedlet till att störa en stressignal i nervceller som man tror driver celldöd och uppbyggnad av skadliga proteiner.
Ett nytt mål inne i sårbara hjärnceller
Forskare har länge vetat att Parkinsons är förknippat med klumpar av ett protein som kallas alfa‑synuklein som ansamlas i nervceller och sprider sig genom nervsystemet. Dessa klumpar kan utlösa en cellulär stressensor kallad c‑Abl, som sedan sätter igång en kedjereaktion som driver celler mot död. Risvodetinib är en tablett utformad för att ta sig in i hjärnan och selektivt blockera c‑Abl. I djurmodeller för Parkinsons gav daglig dosering skydd åt nervceller, minskade skadlig proteinansamling och förbättrade rörelseförmågan. Dessa uppmuntrande resultat ledde forskarna till att starta det de kallar ”201‑studien”, den första längre doseringsstudien av risvodetinib hos människor.
Hur 201‑studien var upplagd
Studien rekryterade 137 vuxna i USA som nyligen diagnostiserats med Parkinsons och ännu inte börjat med standardbehandling. Deltagarna tilldelades slumpmässigt att få en av tre dagliga doser risvodetinib (50, 100 eller 200 milligram) eller placebo i 12 veckor, följt av en två veckor lång säkerhetsuppföljning. Varken deltagare eller läkare visste vem som fick aktivt läkemedel. Huvudsyftet var inte att bevisa symptomförbättring, utan att noggrant följa biverkningar, allvarliga medicinska händelser och hur många som kunde fortsätta ta medicinen under hela behandlingsperioden.
Säkerhet, biverkningar och dagligt fungerande
Risvodetinib klarade detta första säkerhetstest. Ungefär 95% av de som fortsatte efter en kort regulatorisk paus slutförde 12‑veckorsbehandlingen, med nästan perfekt följsamhet till tablettintag. Antalet personer som rapporterade minst ett nytt medicinskt besvär var likartat i risvodetinib‑ och placebogrupperna, och inga dödsfall inträffade. Allvarliga problem, såsom infektioner eller skador som krävde sjukhusvård, var sällsynta och bedömdes inte relaterade till studiepreparatet. Biverkningar som ofta ses med andra läkemedel i samma breda familj — till exempel hjärtpåverkan, uttalad svullnad eller ögonskada — var minimala eller frånvarande. Sammantaget framstod risvodetinib som oväntat mildt för ett läkemedel som verkar på ett kraftfullt signalenzym.
Eftersom studien var kort och relativt liten förväntades den inte visa tydlig klinisk förbättring. Faktum är att standardiserade skalor för rörelse och dagligt liv förändrades lite över 12 veckor, och huvudresultatet för kombinerad rörelseskala skilde sig inte signifikant mellan risvodetinib och placebo. Ett fåtal mått visade små, ”nominala” vinster vid vissa doser, till exempel måttliga förbättringar i självskattade dagliga aktiviteter, men dessa signaler är för svaga och kortvariga för att räknas som bevis för symptomlindring. Viktigt är att risvodetinib inte verkade förvärra rörelse‑ eller icke‑rörelserelaterade symtom i stort.
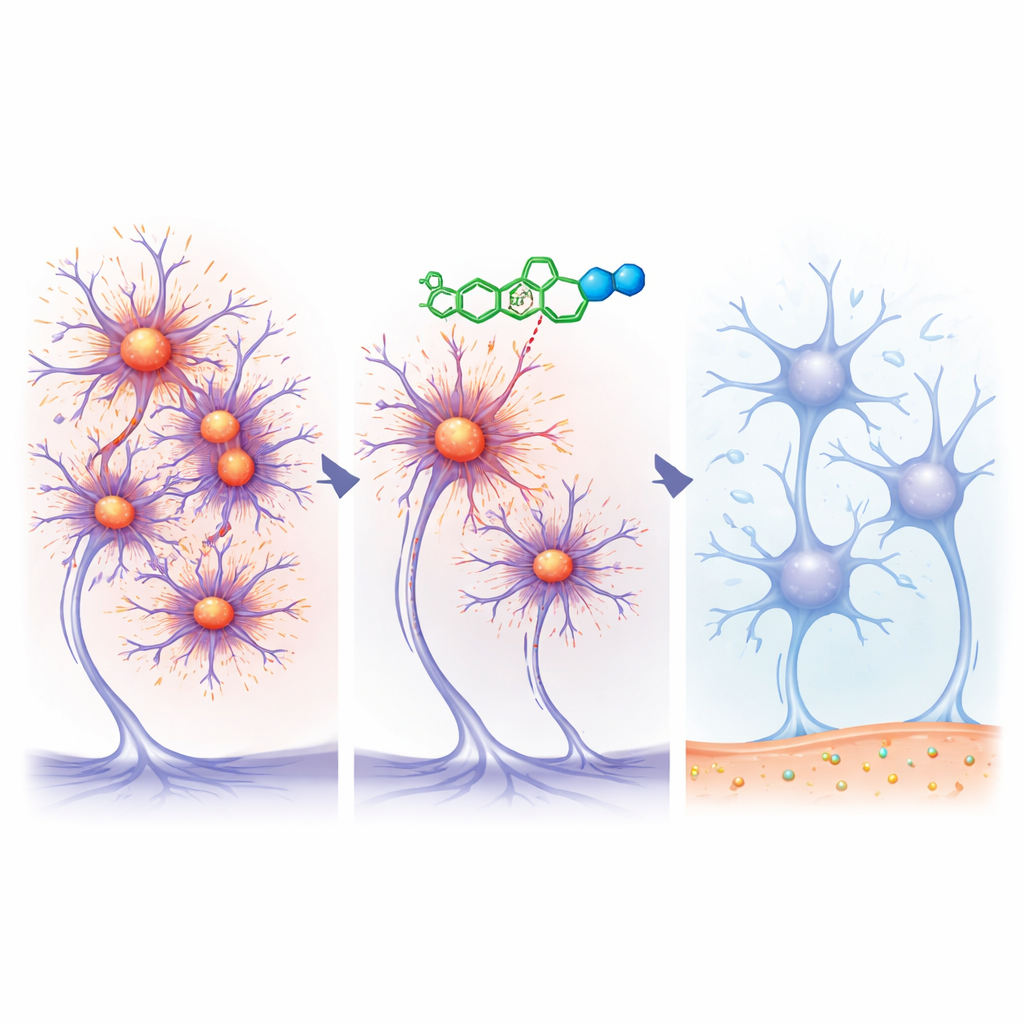
En inblick i sjukdomsprocessen i huden
För att se bortom symtomen använde teamet ett ovanligt fönster in i sjukdomen: små hudbiopsier. Nervfibrer i huden hos personer med Parkinsons kan också samla onormalt alfa‑synuklein, vilket kan visualiseras med fluorescensmikroskopi. Ungefär 40% av deltagarna gick med på upprepade hudprov, och 36 hade användbart vävnad både före och efter behandling. I placebogruppen visade många oförändrade eller ökande nivåer av proteinavlagringar över 12 veckor, även om några visade spontana minskningar. Bland dem som fick risvodetinib var ökningar av avlagringar mindre vanliga, och andelen personer med minskade avlagringar ökade med högre doser, och nådde ungefär två tredjedelar i högst dosgruppen. Grupperna var dock små och skillnaderna nådde inte konventionella statistiska gränser, så fynden är antydande snarare än avgörande.
Vad detta innebär för framtida behandling
201‑studien visar att blockad av c‑Abl med risvodetinib kan genomföras säkert i minst tre månader hos personer med tidig Parkinsons, vid läkemedelsnivåer som är mycket högre än de som används för befintliga cancerläkemedel som påverkar samma väg. Tidiga hudbiopsieresultat antyder att läkemedlet kan påverka den underliggande sjukdomsprocessen genom att hjälpa nervceller rensa skadlig proteinansamling, men starkare och längre studier behövs för att bekräfta detta och för att ta reda på om sådana förändringar översätts till långsammare symtomsutveckling. För nu gör studien inte anspråk på att risvodetinib förbättrar hur människor mår eller fungerar — bara att det verkar tillräckligt säkert för att motivera nästa steg: större, längre prövningar för att undersöka om det faktiskt kan förändra Parkinsons sjukdoms förlopp.
Citering: Werner, M.H., McGarry, A., Meyer, C. et al. The 201 Trial: a placebo-controlled randomized phase 2 study of safety and tolerance of the c-Abl kinase inhibitor risvodetinib in untreated Parkinson’s disease. Nat Aging 6, 626–635 (2026). https://doi.org/10.1038/s43587-026-01084-4
Nyckelord: Parkinsons sjukdom, neuroprotektion, klinisk prövning, proteininlagring, tyrosinkinashämmare