Clear Sky Science · sv
Strukturellt signatur av plasmaproteiner klassificerar statusen för Alzheimers sjukdom
Varför ett blodprov för minnesförlust spelar roll
Alzheimers sjukdom har ofta kommit långt innan minnesproblem blir uppenbara, men dagens tester för att upptäcka den tidigt kan vara invasiva, kostsamma eller svåra att få tillgång till. Denna studie undersöker en annan idé: om små förändringar i de tredimensionella formerna hos proteiner som cirkulerar i blodet kan avslöja var en person befinner sig på skalan från hälsosamt åldrande till lindrigt glömska till fullständig Alzheimers sjukdom. Om detta lyckas skulle ett sådant blodprov kunna förenkla screening, stödja tidigare behandling och hjälpa forskare att följa vilka som drar nytta av nya terapier.
Tittar på proteinform, inte bara mängd
De flesta blodprov mäter hur mycket av en viss molekyl som finns. Här fokuserade forskarna istället på proteinernas form. Inne i våra celler håller ett system för kvalitetskontroll proteiner korrekt vikta; när detta system sviktar med åldern kan felvikta proteiner ansamlas och skada hjärnceller. Forskargruppen undrade om den här försämringen i ”proteinunderhåll” lämnar ett strukturellt fingeravtryck i blodproteiner. Från 520 volontärer som antingen var kognitivt friska, hade lindrad kognitiv svikt (MCI) eller Alzheimers sjukdom tog de blodprover och använde en kemisk metod kallad kovalent proteinprofilering för att märka exponerade delar av proteiner. Ju mer exponerad en plats är, desto lättare märks den, vilket ger ett numeriskt mått på proteinform som till stor del är oberoende av hur mycket protein som finns.
Hittar strukturella fingeravtryck i blodet
Över nästan 900 märkta proteinfragment såg forskarna en subtil men konsekvent trend: när människor gick från friska till MCI till Alzheimers blev vissa proteinyta mindre exponerade och mer varierande från person till person. Detta mönster stämmer med idén att kroppens kontroll av proteinvikning försämras i takt med att sjukdomen utvecklas. Gruppen undersökte också hur en viktig genetisk riskfaktor för Alzheimers, APOE ε4-varianten, påverkade proteinform. De fann att personer med två kopior av ε4 visade distinkta strukturella skift i flera proteiner som interagerar med APOE-proteinet, vilket tyder på att denna riskfaktor inte bara ändrar vilka proteiner som finns, utan också hur de viks och är ordnade.
Kopplar blodproteiner till stämning och beteende
Alzheimers påverkar mycket mer än minnet; symtom som agitation, depression och hallucinationer är vanliga och skiljer sig ofta mellan män och kvinnor. Forskarna kombinerade kliniska bedömningar av 12 typer av neuropsykiatriska symtom med sina mätningar av proteinform. I båda könen tenderade svårare symtom att gå hand i hand med att proteiner blev mer strukturellt ”stängda”. Vissa proteiner, inklusive clusterin och flera andra kopplade till amyloidansamling, följde symtomens svårighetsgrad på liknande sätt hos män och kvinnor, medan andra visade könsspecifika mönster. Dessa fynd antyder att blodproteiners struktur kan spegla inte bara sjukdomens närvaro utan också hur den yttrar sig i beteende och humör.
Ett treproteins-panel för att klassificera sjukdomsstadiet
För att omvandla dessa komplexa mätningar till något kliniskt användbart matade gruppen de strukturella uppgifterna in i 18 olika maskininlärningsmetoder. Den bäst presterande modellen, baserad på djupinlärning, förlitade sig på bara tre proteinfragment från C1QA, clusterin (även kallat CLUS) och apolipoprotein B (ApoB). Genom att använda endast de strukturella avläsningarna från dessa tre fragment sorterade modellen korrekt personer i grupperna friska, MCI eller Alzheimers ungefär 83 % av gångerna i en oberoende testuppsättning. När man ställde enklare tvåvägsfrågor—såsom att skilja friska från MCI, eller MCI från Alzheimers—var panelens prestanda ännu starkare, med noggrannhetsmått jämförbara med eller bättre än många nuvarande blodbaserade metoder som fokuserar på proteinmängder istället för struktur.
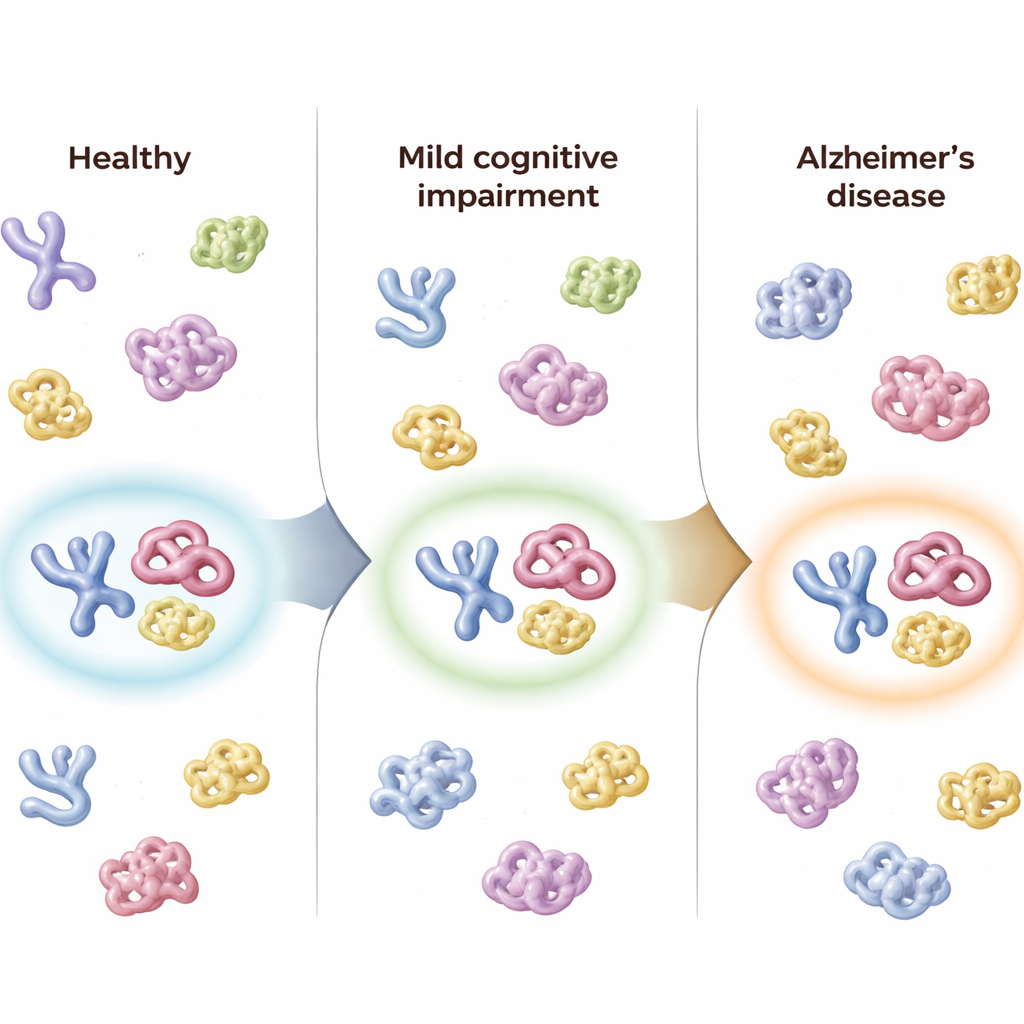
Följer personer över tid
Forskarna hade också uppföljningsprover från 50 deltagare tagna upp till cirka åtta månader senare. Hos personer vars diagnos försämrades—till exempel från frisk till MCI, eller från MCI till Alzheimers—skiftade den kombinerade poängen från treproteins-panelen i samma riktning och speglade sjukdomsprogression. Däremot visade individer vars kliniska status förblev densamma liten förändring i sina panelpoäng. Panelens övergripande ”Alzheimers-förtroende”-poäng följde nära standardiserade kognitiva tester, mått på dagligt fungerande, hjärnatrofi på MR-bilder och etablerade ryggvätskemarkörer för amyloid och tau, vilket tyder på att den blodbaserade strukturella signalen speglar underliggande hjärnförändringar.
Vad detta kan betyda för patienter
Sammantaget visar arbetet att små, samordnade förändringar i formerna hos bara några få rikliga blodproteiner kan på ett tillförlitligt sätt signalera om någon är kognitivt frisk, lindrigt nedsatt eller har Alzheimers sjukdom. Eftersom testet använder blod snarare än ryggvätska eller hjärnavbildning skulle det i princip kunna skalas upp för rutinmässig screening eller för att välja och övervaka deltagare i kliniska prövningar. Författarna varnar för att större och längre studier behövs, och att den använda kemin fortfarande är specialiserad. Ändå pekar deras resultat på proteinstruktur—inte bara proteinnivåer—som en lovande ny informationskälla för att upptäcka och följa Alzheimers sjukdom tidigare och mer precist.
Citering: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Nyckelord: Biomarkörer för Alzheimers sjukdom, blodprov för demens, förändringar i proteinfällning, maskininlärningsdiagnostik, clusterin och C1QA