Clear Sky Science · sv
Resistens mot platina-baserad kemoterapi vid lung- och ovarialcancer drivs av ett målinriktbart TGFβ-senescent sekretom
När cancerbehandling slår tillbaka
Platina-baserad kemoterapi är en av hörnstenarna i modern cancerbehandling, särskilt för lung- och ovarialcancer. Den är avsedd att skada tumörens DNA så allvarligt att cancerceller inte längre kan dela sig. Ändå ser många patienter att deras tumörer krymper först, för att sedan återkomma, starkare än tidigare. Denna studie ställer en enkel men oroande fråga: kan de läkemedel som räddar liv också hjälpa överlevande cancerceller att återhämta sig? Svaret, menar författarna, ligger i en särskild grupp skadade, åldringsliknande celler och de kraftfulla kemiska budskap de sänder ut.
Den dubbla existensen hos åldrande cancerceller
Kemoterapi påverkar inte alla tumörceller på samma sätt. Några dör omedelbart, men andra går in i ett tillstånd kallat cellulär senescens—de slutar permanent dela sig, men är fortfarande levande. Dessa senescenta celler sväller i storlek och börjar utsöndra en blandning av proteiner och signaler känd som senescence-associated secretory phenotype, eller SASP. Med hjälp av humana lung- och ovariecancerceller i laboratoriet, samt musmodeller, visade forskarna att platinaläkemedel som cisplatin och karboplatin skapar särskilt potenta senescenta celler. När färska cancerceller exponerades för vätska tagen från dessa senescenta kulturer växte de snabbare, migrerade lättare och bildade större, mer aggressiva kluster och sfärer än kontrollceller.
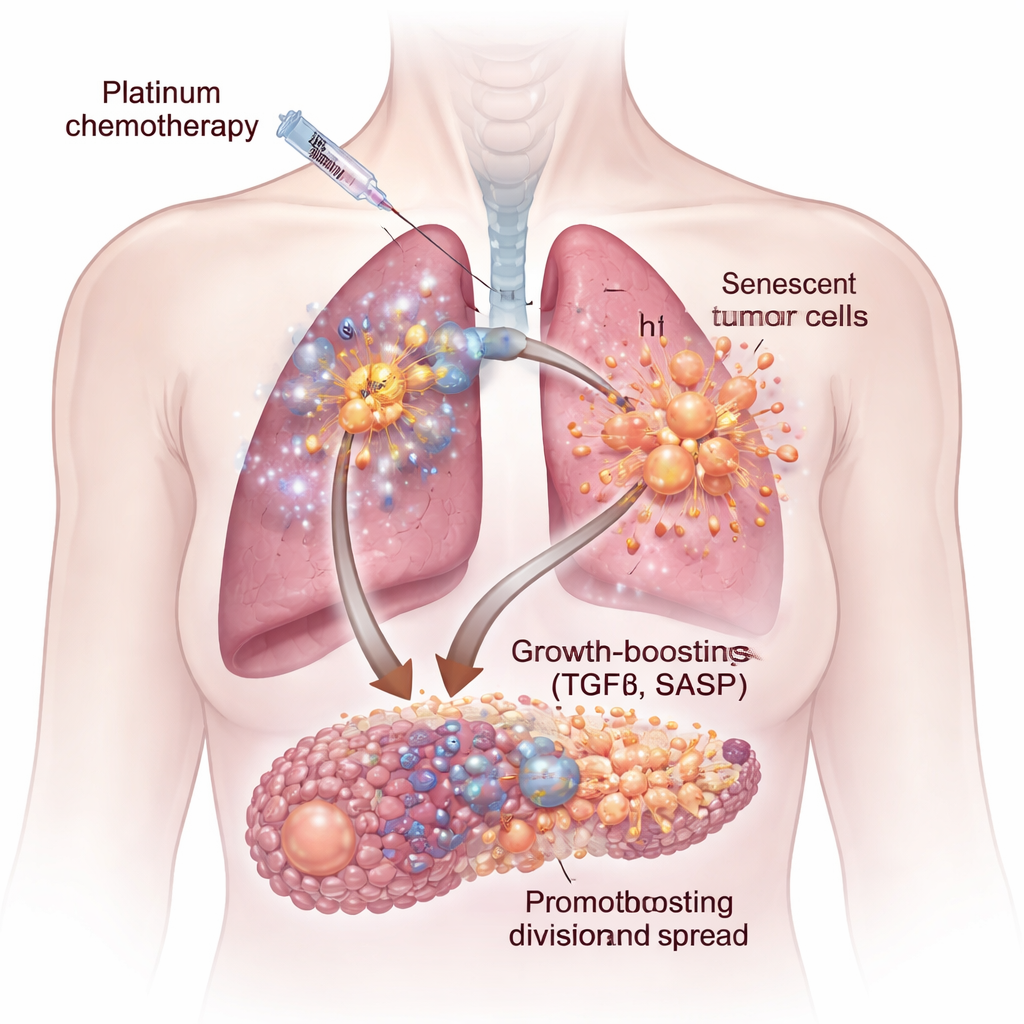
En dold tillväxtsignal: TGFβ
Alla kemoterapier utlöste inte samma skadliga utsöndringar. När teamet jämförde platina-läkemedel med två andra vanliga medel, docetaxel och palbociklib, producerade endast de platina-behandlade cellerna en SASP som starkt ökade tumörtillväxt. Genom en kombination av genuttrycksstudier, proteinmätningar och en höggenomströmmande mikro-miljö-mikroarray identifierade de en nyckelorsak: signalmolekylen transforming growth factor-beta, eller TGFβ. Senescenta celler inducerade av cisplatin var berikade för flera TGFβ-former och relaterade signalvägar. Tillsats av renat TGFβ till cancerceller efterliknade den tillväxtökning som sågs med vätskan från senescentaceller och lyfte fram denna cytokinfamilj som en central drivkraft i det pro-tumorala sekretomet.
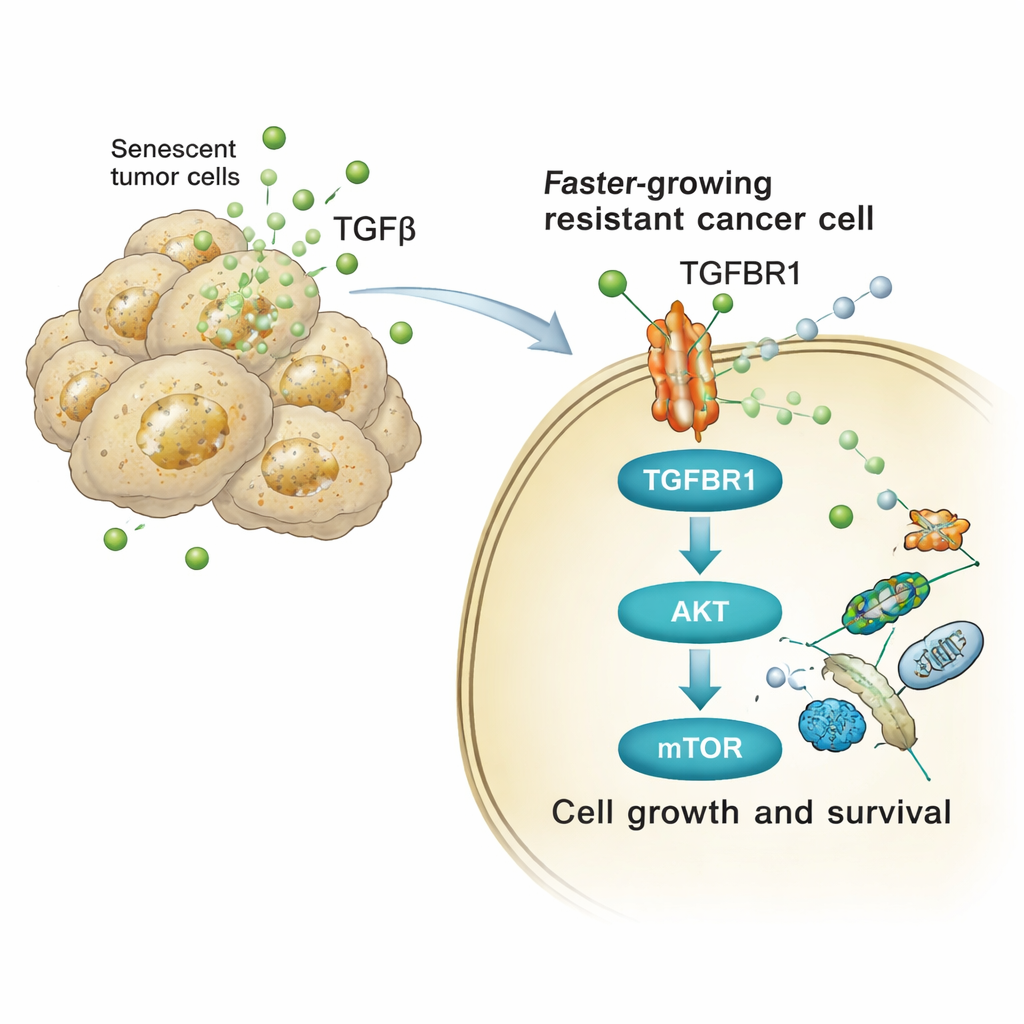
Hur signalen omprogrammerar cancerceller
Studien spårade sedan hur dessa TGFβ-rika signaler förändrar beteendet hos närliggande tumörceller. På mottagarcells yta binder TGFβ till en receptor kallad TGFBR1. Detta aktiverar i sin tur en intern kedja av proteiner—särskilt AKT- och mTOR-vägarna—som är kända för att styra celltillväxt, metabolism och överlevnad. I både humana och musbaserade lungcancerceller ökade exponering för cisplatin-orsakade sekretionsprodukter snabbt de aktiverade (fosforylerade) formerna av AKT och dess nedströmsmål p70S6K, och ökade uttrycket av cellcykelgener. Att blockera TGFBR1 med ett läkemedel kallat galunisertib, eller att hämma mTOR direkt, stängde i stor utsträckning ner denna signalökning och minskade den extra proliferation, kolonibildning och invasiv sfärtillväxt som utlöstes av det senescenta sekretomet.
Från möss till patienter: en gemensam svag punkt
Dessa mekanismer var inte begränsade till petriskålar. Hos möss med lungtumörer ledde blandning av senescenta och icke-senescenta cancerceller till snabbare tumörtillväxt och kortare överlevnad, medan eliminering av senescenta celler eller blockad av TGFBR1 dämpade denna effekt. När standard cisplatinbehandling gavs till möss med genetiskt framtagna lungcancerformer ackumulerade tumörer senescensmarkörer tillsammans med hög AKT/mTOR-aktivitet i närliggande, fortfarande delande celler. Kombination av cisplatin med TGFBR1-hämning eller senolytiska läkemedel (som selektivt dödar senescenta celler) minskade tumörbördan och förlängde överlevnaden jämfört med enbart kemoterapi. Viktigt är att analyser av humana lung- och höggradig serös ovarialcancerprover tagna efter platina-baserad behandling visade liknande mönster: ökade markörer för senescens och förhöjd AKT/mTOR-signalering i tumörmikromiljön, särskilt i regioner rika på senescenta celler.
Förvandla en svaghet till en fördel
För en lekmannaläsare är slutsatsen att platina-kemoterapi kan lämna kvar en population av skadade men farliga "zombie"-celler. Dessa senescenta tumörceller delar sig inte längre, men de pumpar ut TGFβ-rika signaler som väcker närliggande cancerceller, vilket hjälper tumörer att växa tillbaka och bli motståndskraftiga mot fortsatt behandling. Uppmuntrande är att denna svaghet kan riktas mot. I prekliniska lung- och ovarialcancermodeller gjorde tillsats av läkemedel som blockerar TGFβ-receptorn TGFBR1 eller som selektivt rensar senescenta celler platina-kemoterapi mer effektivt och förbättrade överlevnaden utan uppenbar extra toxicitet. Arbetet pekar mot framtida kliniska prövningar som kombinerar standard platina-behandling med senolytiska eller anti-TGFβ-strategier, med målet att bevara kemoterapins fördelar samtidigt som dess dolda, senescensdrivna bieffekter desarmeras.
Citering: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Nyckelord: kemoterapiresistens, cellulär senescens, TGFβ-signalering, lungcancer, ovarialcancer