Clear Sky Science · sv
DNA-skador i makrofager driver immunautoreaktivitet via presentation av nukleära antigener
När cellulärt slitage vänder immunsystemet mot oss
Åldrande medför en ökad risk för autoimmuna sjukdomar, där immunsystemet börjar attackera den kropp det ska skydda. Denna studie undersöker en överraskande gärningsman: vardagliga DNA-skador inne i immunceller kallade makrofager. Genom att spåra hur dessa skador förändrar vad makrofager visar för andra immunceller avslöjar forskarna en möjlig saknad länk mellan åldrande och sjukdomar som lupus.
Väktare av kroppen som tappar manus
Makrofager är frontlinjeförsvarare som slukar mikrober och skräp och sedan visar upp proteindelar för T‑celler, vilket hjälper immunsystemet avgöra vad som ska attackeras. Forskarna konstruerade möss vars makrofager var defekta i ett viktigt DNA-reparationsprotein, ERCC1‑XPF, så att dessa celler bar på bestående DNA‑skador. När dessa möss åldrades utvecklade de kännetecken för autoimmunitet: inflammatoriska fokus i njurarna, depositioner av immunkomplex och komplementsystemets proteiner, förstorade mjältar och höga nivåer av antinukleära antikroppar liknande dem som ses hos naturligt gamla djur. Detaljerad immunprofilering visade en expansion av plasmaceller, aktiverade T‑celler och naturliga mördarceller, alla tecken på ett kroniskt stimulerat immunsystem.
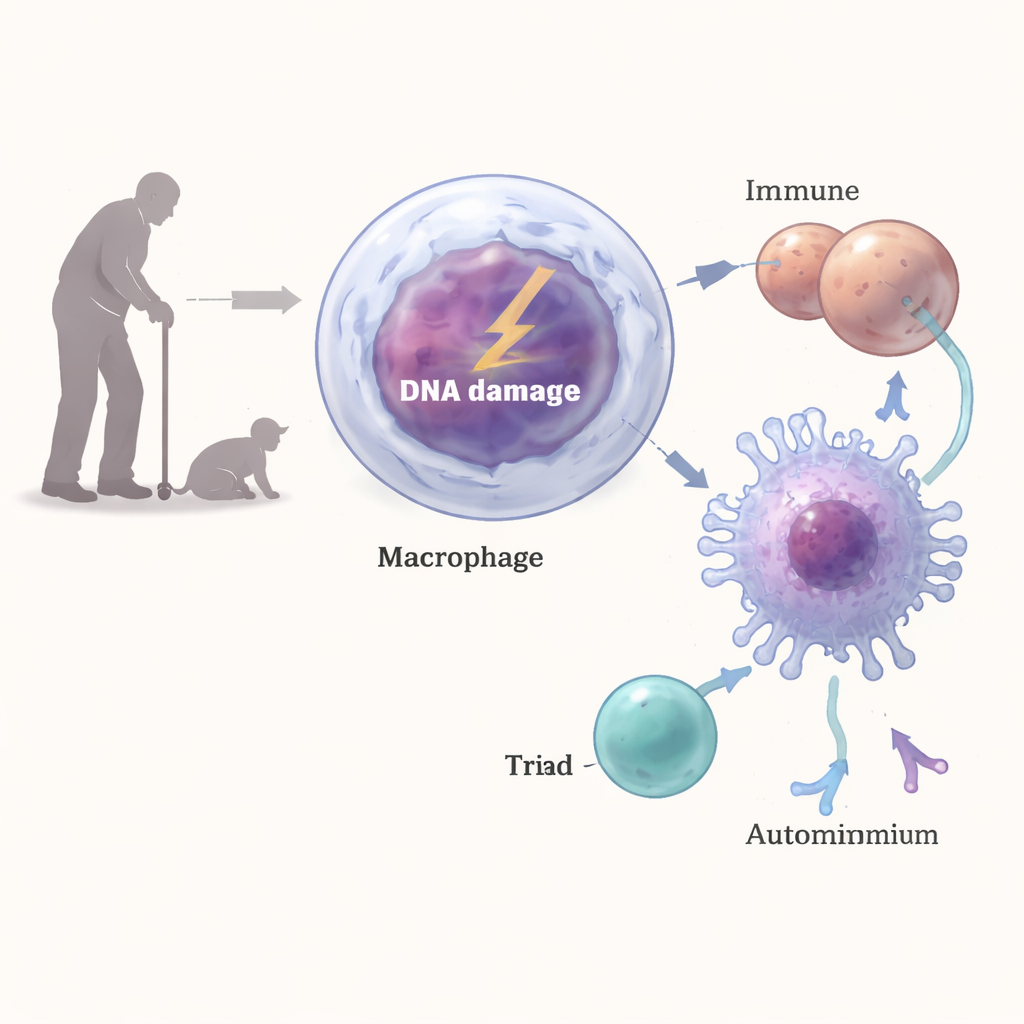
Från brutet DNA till själv‑riktade T‑celler
Hur kan skadat DNA i makrofager utlösa ett så starkt autoimmunliknande svar? Forskarna fann att DNA‑brott aktiverade en klassisk skaderesponsväg i dessa celler, med enzymer såsom ATM, ATR och DNA‑PK. Denna signalering ökade nivåerna av MHC klass II på cellytan, de molekylära skyltfönstren som används för att presentera proteindelar för CD4‑T‑celler. När makrofager med DNA‑skador blandades med T‑celler framkallade de starkare T‑cellsaktivering och produktion av interferon‑gamma än normala makrofager. Blockering av MHC‑II eller störning av DNA‑skaderesponsen reverserade mycket av denna effekt, och i levande djur minskade antikroppar som blockerade MHC‑II eller utarmade CD4‑T‑celler njurinflammation och nivåer av autoantikroppar.
Självproteiner från kärnan som ställs ut
För att exakt se vad skadade makrofager visade för T‑celler isolerade teamet peptider bundna till MHC‑II och analyserade dem med masspektrometri. Jämfört med normala eller lipopolysackarid‑stimulerade celler presenterade DNA‑skadade makrofager en påtagligt annorlunda meny av peptider. Istället för huvudsakligen membran‑ och extracellulära proteiner var deras MHC‑II‑molekyler berikade för fragment härledda från nukleära och ribosomala proteiner, inklusive histoner och andra komponenter tätt associerade med DNA. När några av dessa nukleära peptider syntetiserades och användes för att återstimulera immunceller från de konstruerade mössen utlöste de starka T‑cellsresponser, vilket tyder på att dessa själv‑härledda fragment faktiskt var immunogena.
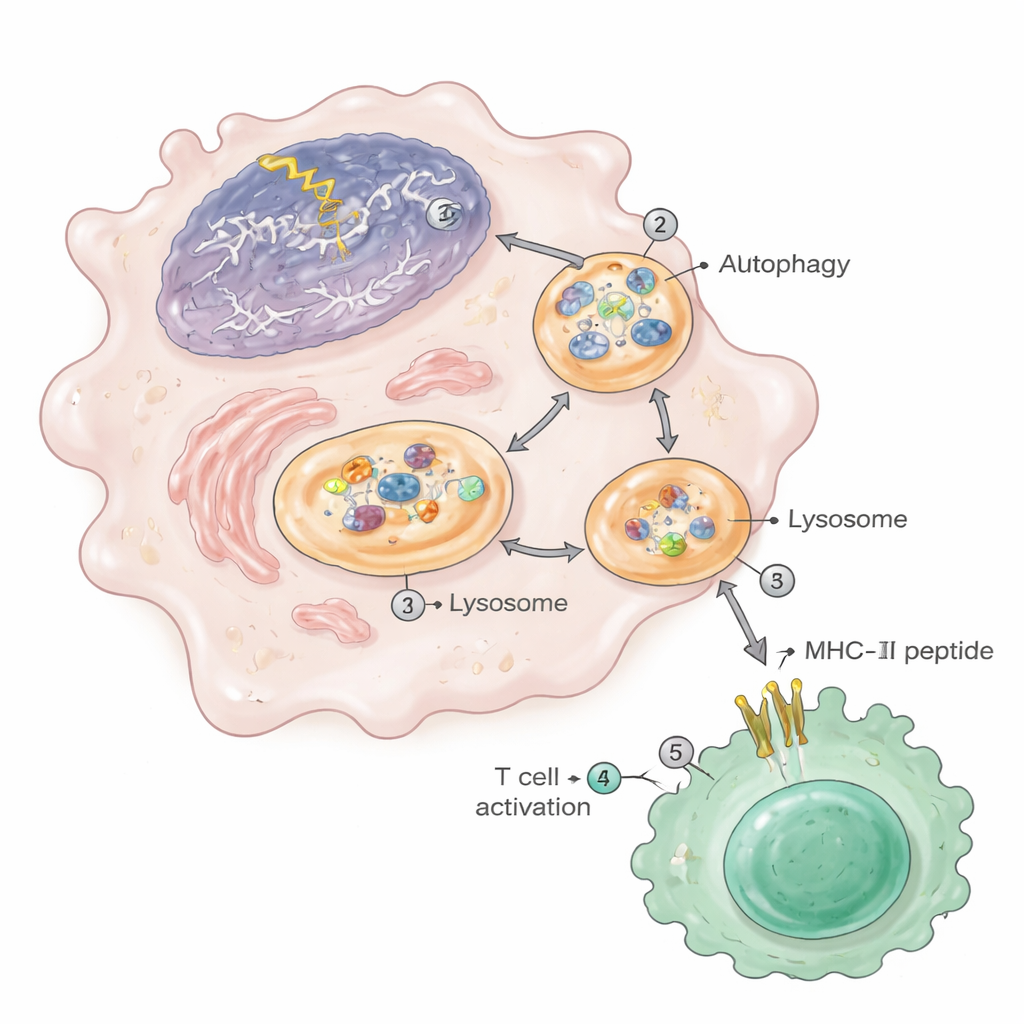
Autofagi: städningsvägen som matar autoimmunitet
Vägen för nukleärt material till MHC‑II‑skyltfönstret var starkt beroende av autofagi, cellens interna återvinningssystem. Vid DNA‑skada ökade autofagin och transporterade kromatinfragment — från cellens egen kärna — in i autofagosomer som sedan smälte samman med lysosomer, där proteiner bryts ner till peptider. Dessa lysosomer i skadade makrofager innehöll förhöjda nivåer av nukleära och ribosomala proteiner. När forskarna blockerade autofagi med läkemedel eller genetiskt avlägsnade en essentiell autofagigen (Atg5) i samma myeloida celler visade djuren färre njurlesioner, färre aktiverade T‑celler och plasmaceller, samt en dramatisk minskning av nukleära peptider på MHC‑II. Liknande kromatinfragment och ökad antigenpresentation sågs i makrofager från lupus‑benägna möss, humana monocytcellinjer utsatta för DNA‑skadande läkemedel och i makrofager från mycket gamla möss.
Varför detta är viktigt för åldrande och autoimmun sjukdom
Tillsammans föreslår fynden en enkel men kraftfull idé: när vi åldras ackumuleras DNA‑skador i makrofager, som i sin tur använder autofagi för att rensa nukleärt skräp. Genom detta klipper de oavsiktligt upp nukleärt material till peptider som laddas på MHC‑II och visas för T‑celler som om de vore främmande. Med tiden kan denna kroniska exponering för nukleära självantigener träna immunsystemet att reagera mot kroppen själv och främja autoimmunitet. Genom att peka ut denna väg — från DNA‑skada till autofagi till presentation av nukleära antigener — lyfter studien fram nya strategier för att dämpa åldersrelaterad autoimmunitet, såsom att förbättra DNA‑reparation, finjustera autofagi eller selektivt blockera presentationen av nukleära självpeptider utan att stänga ner immunsystemets viktiga försvar.
Citering: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Nyckelord: åldrande och autoimmunitet, DNA-skador, makrofager, autofagi, antinukleära antikroppar