Clear Sky Science · sv
Senotoxiner riktar in sig på senescens via lipidspecificitet, jonobalans och ombyggnad av lipidomet
Varför döda ”zombie”-celler kan skärpa cancerbehandlingen
När vi blir äldre — eller utsätts för tuffa behandlingar som kemoterapi — slutar vissa celler dela sig men vägrar dö. Dessa ”zombie”-celler, kända som senescenta celler, kan spilla ut inflammatoriska molekyler som skadar vävnader och kan hjälpa tumörer att komma tillbaka. Denna studie utforskar ett överraskande nytt sätt att selektivt eliminera sådana problematiska celler med ett giftinspirerat protein från ett djur, vilket potentiellt kan göra cancerbehandlingar både effektivare och säkrare.
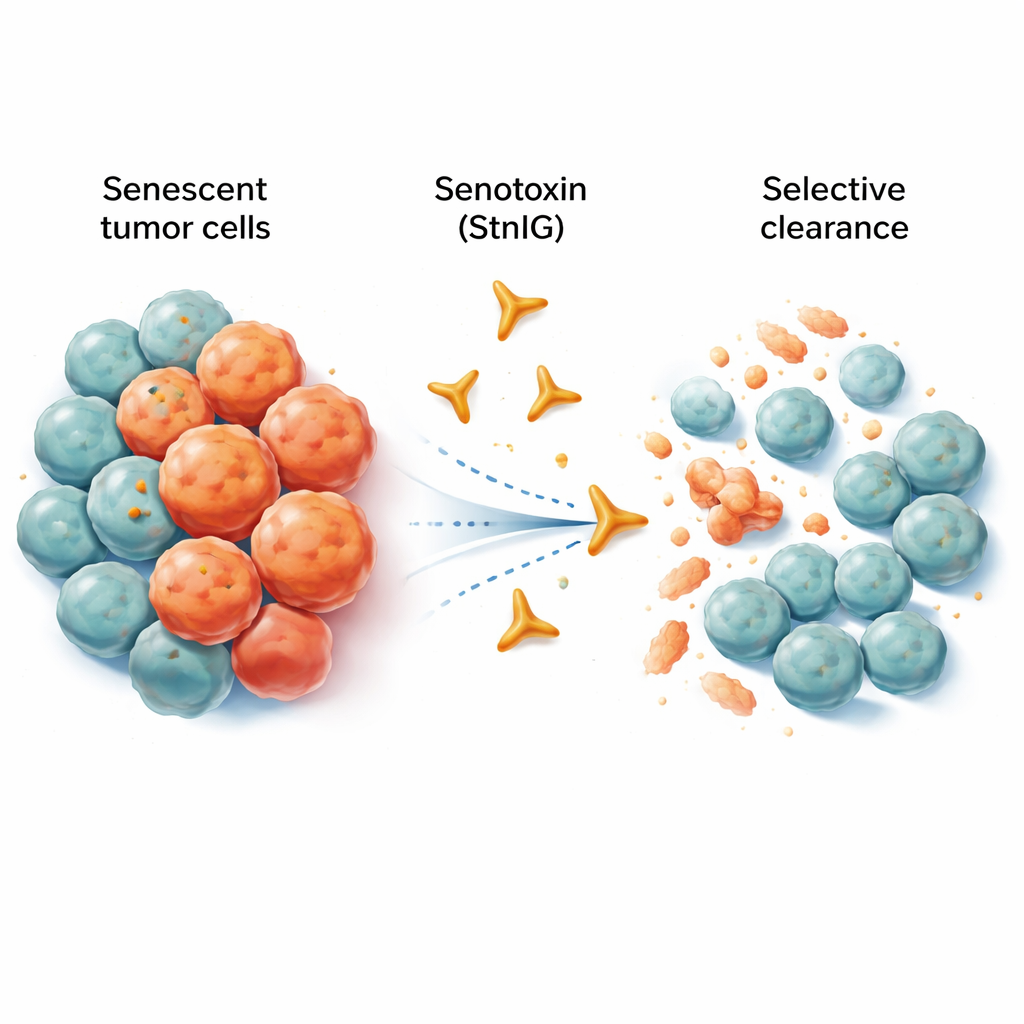
Gamla celler som vägrar ge sig
Senescenta celler liknar pensionerade arbetare som fortfarande sitter kvar vid sina skrivbord och ställer till problem på kontoret. De delar sig inte längre, men de utsöndrar en blandning av inflammatoriska signaler som kan försvaga omkringliggande vävnad, främja åldrande och till och med stödja tumörtillväxt och spridning. Kemoterapi dödar visserligen många cancerceller, men lämnar ofta kvar ett spår av senescenta celler i och runt tumören. Dessa kvarvarande celler kan driva kronisk inflammation, biverkningar och i slutändan återfall. Befintliga experimentella läkemedel, så kallade senolytika, syftar till att avlägsna senescenta celler, men många av dem angriper också friska celler, fungerar bara inom mycket snäva dosintervall eller är svåra för kroppen att ta upp.
Att förvandla havsanemongift till ett precist verktyg
Forskarlaget vände sig till naturens egna specialister på celldöd: djurgifter. De koncentrerade sig på ett porbildande protein kallat sticholysin I (StnI), som finns i en karibisk havsanemon. Detta protein kan slå små hål i cellmembran. Gruppen upptäckte att StnI, och en förfinad variant de konstruerade kallad StnIG, är anmärkningsvärt bättre på att döda senescenta cancerceller än deras icke-senescenta grannar. I flera typer av mänskliga cancerceller (melanom, lever, lung- och nervcellsderiverade tumörer) som tvingats in i senescens av kemoterapiläkemedel, utplånade StnI och särskilt StnIG de åldrade cellerna vid mycket lägre doser än vad som krävdes för att påverka aktivt växande celler. StnIG var mer selektivt än en ledande experimentell senolytika, navitoclax, vilket tyder på att noggrant stämda toxiner kan överträffa nuvarande metoder.
Hur förändrade cellmembran blir ett akilleshäl
Senescenta celler förändras inte bara inifrån; deras yttre membran — det fettiga skikt som omger varje cell — ombyggs också. I friska celler sitter vissa lipidmolekyler mest på membranets inre sida, skyddade från omvärlden. I senescenta celler kollapsar denna balans och dessa lipider blottas. Genom detaljerad kemisk analys och datorbaserade simuleringar visade teamet att StnIG känner igen och fäster vid detta förändrade lipidlanskap. Dess struktur är särskilt väl anpassad för att haka i specifika lipider som senescenta celler exponerar på sin yta. När den väl fäster bildar StnIG porer som tillåter laddade atomer, joner, att strömma in och ut på ett kraftigt obalanserat sätt.
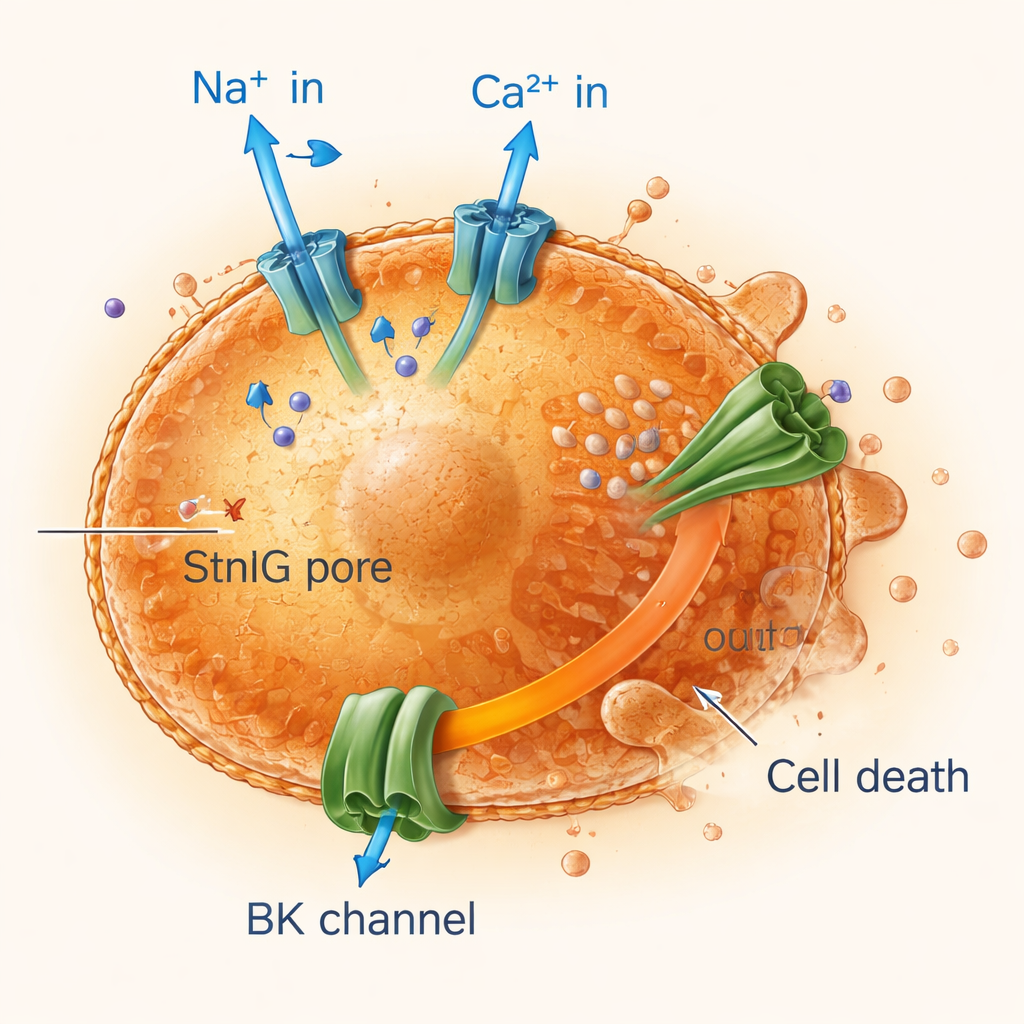
Kortslutning av åldrande celler med jonobalans
Genom att följa elektricitet och jonrörelser över cellmembran fann forskarna att StnIG-porer tillåter natrium- och kalciumjoner att strömma in i senescenta celler medan kalium kontinuerligt sipprar ut. Kalciumökningen aktiverar stora kaliumkanaler, vilket förstärker förlusten av kalium, vilket är avgörande för att upprätthålla cellvolym och överlevnad. Senescenta celler, redan mindre flexibla och mer sköra än friska celler, kan inte hantera denna ihållande jonstörning. Deras mitokondrier — cellernas kraftverk — förlorar sin elektriska potential, energiproduktionen sjunker och cellerna genomgår programmerade dödsformer, inklusive apoptos och en inflammatorisk, brännande död kallad pyroptos. Blockering av kalciuminflöde eller kaliumkanaler skyddade senescenta celler, vilket bekräftar att denna jonsstörning är central för toxinets verkan.
Från cellskålar till levande djur
Teamet testade sedan om denna strategi fungerar i levande organismer. I zebrafiskembryon som bar mänskliga senescenta melanomceller reducerade låga doser StnIG antalet av dessa celler lika effektivt som navitoclax, utan uppenbar toxicitet. I musmodeller av melanom och levercancer bromsade kemoterapi med ett cellcykelinhiberande läkemedel (palbociklib) tumörtillväxt genom att tvinga många cancerceller in i senescens. När forskarna tillsatte StnIG intermittenta gav tumörerna krympning eller remission mer effektivt än med enbart kemoterapi, och jämförbart med kombinationen kemoterapi–navitoclax. Viktigt är att StnIG-behandlade möss visade begränsade biverkningar och ingen tydlig skada i större organ, även om blodets kalium ökade i djur med senescenta tumörer — troligen en följd av den massiva frisättningen av kalium när tumörceller förstördes.
Vad detta betyder för framtidens cancervård
Detta arbete introducerar ”senotoxiner”: ingenjörsmässigt framtagna, giftinspirerade proteiner som utnyttjar senescenta cellers unika membran- och jonhanteringsegenskaper. Genom att rikta in sig på förändrade lipider och framkalla dödliga jonobalanser kan StnIG selektivt rensa bort skadliga senescenta celler samtidigt som majoriteten av frisk vävnad sparas. Använda tillsammans med kemoterapi kan sådana senotoxiner en dag hjälpa till att sopa undan de zombie-celler som driver återfall och kronisk inflammation, göra cancerbehandlingar mer hållbara och potentiellt lindra vissa långsiktiga biverkningar.
Citering: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Nyckelord: cellulär senescens, senolytika, cancerbehandling, gifter från djur som läkemedel, jonkanaler