Clear Sky Science · sv
Syntes och användning av silkefibroin-nanopartiklar för läkemedelsleverans
Silkesgrannens roll som en smartare läkemedelsbärare
Föreställ dig att samma material som bygger upp en silkesmaskens kokong skulle kunna hjälpa läkemedel att hitta sjuk vävnad samtidigt som resten av kroppen skonas. Denna översikt granskar hur silkefibroin — huvudproteinet i silkesmaskssilke — kan omvandlas till pyttesmå partiklar som för med sig läkemedel direkt till tumörer, inflammerade tarmar och sår. För läsaren är det en inblick i hur ett välbekant, naturligt material tyst kan förändra cancerbehandling, tarmhälsa och vävnadsreparation.
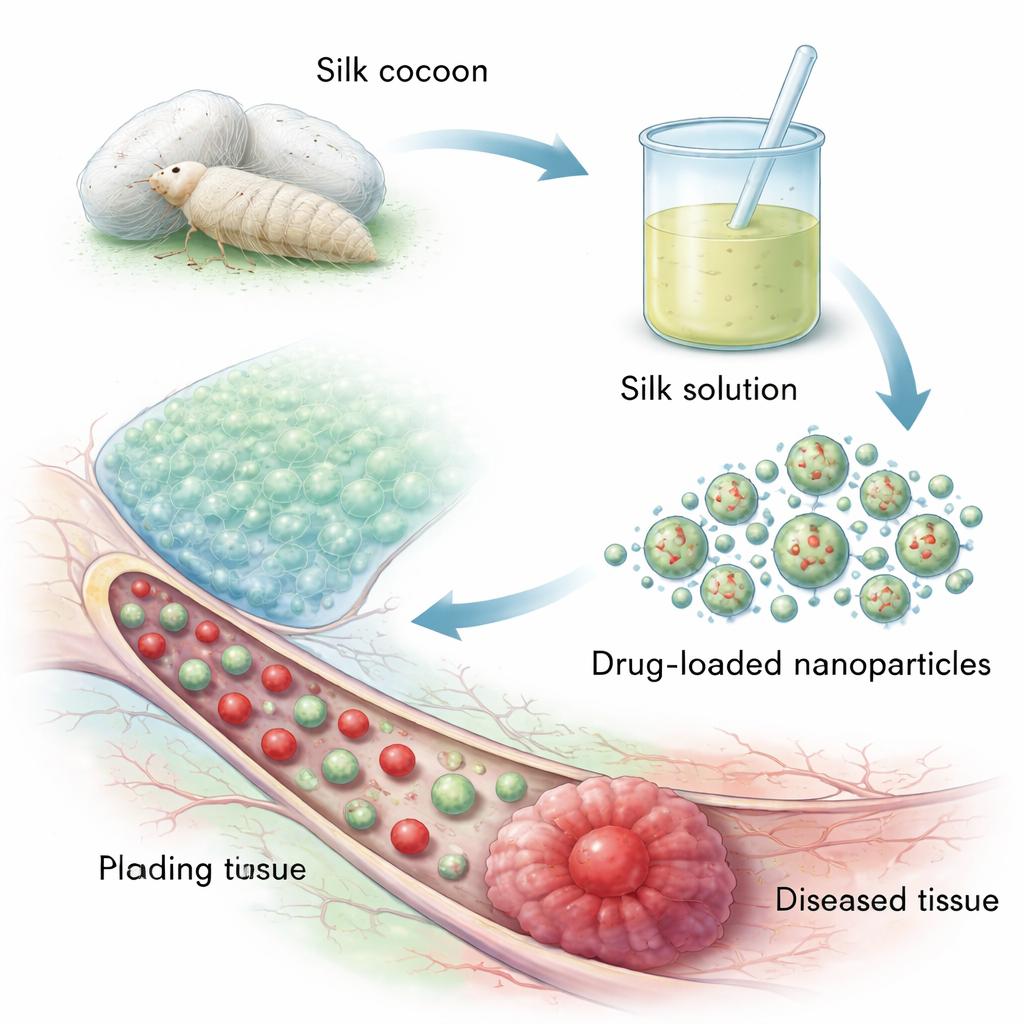
Från kokongtrådar till små medicinpaket
Silkefibroin kommer från kokongerna hos den domesticerade silkesmasken, en lättodlad källa jämfört med spindelsilke. Kokongen har en stark fibroinkärna omsluten av ett annat protein, sericin, som kan framkalla immunreaktioner. För att tillverka medicinskt silke tar man först bort sericinet i en process som kallas degumming, för att sedan lösa upp, rena och torka fibroinet. På molekylär nivå består silkefibroin av långa, repetitiva kedjor av enkla aminosyror som glycin och alanin som kan vikas till tätt packade "beta-sheet"-regioner. Dessa ordnade regioner ger silket dess styrka och gör att forskare kan finjustera hur snabbt det löser upp sig i kroppen — en nyckelfunktion för att kontrollera hur länge ett läkemedel frisätts.
Sätt att forma silke till nanopartiklar
Forskare har utvecklat flera metoder för att omvandla flytande sliklösningar till nanopartiklar som är bara tiotals till några hundra miljarddels meter i diameter. Vid desolvanteringsmetoder droppas silkekoncentrat i ett icke‑lösningsmedel som etanol, vilket får proteinkedjorna att vika sig till beta‑sheet och självmontera till solida sfärer. Emulsionstekniker skapar vatten‑i‑olja‑droppar som hårdnar till partiklar — användbart för att bära oljiga läkemedel men kräver noggrann borttagning av lösningsmedel. Elektrosprutning använder hög spänning för att bryta en sliklösning i fina laddade droppar som torkar i luften till partiklar, medan mikrofluidiska chip blandar silke och "antisolvent" i små kanaler för att generera mycket homogena, reproducerbara nanopartiklar. Varje angreppssätt väger kostnad, kontroll över partikelstorlek och lätthet att skala upp för massproduktion mot varandra.
Finjustering av silke för riktad och tidsstyrd frisättning
Eftersom silkefibroin är rik på reaktiva kemiska grupper kan det modifieras ungefär som ett legobygge med extra delar. Kemsiter fäster små molekyler, polymerer eller biologiska "taggar" för att ändra hur partiklarna interagerar med vatten, hur snabbt de bryts ner eller vilka celler de fäster vid. Till exempel kan tillsats av polyetylenglykol (PEG) göra partiklarna mer stabila i blodet och mindre synliga för immunsystemet, medan pålning av korta proteinfragment eller vitaminer kan hjälpa dem binda till tumörcellreceptorer. Viktigt är att beta‑sheet‑innehåll och tillsatta länkar kan justeras så att silkepartiklar reagerar på omgivningen: de kan lossna i sura förhållanden, i närvaro av vissa enzymer eller i oxiderade områden och därigenom frigöra mer läkemedel precis där vävnaden är sjuk.
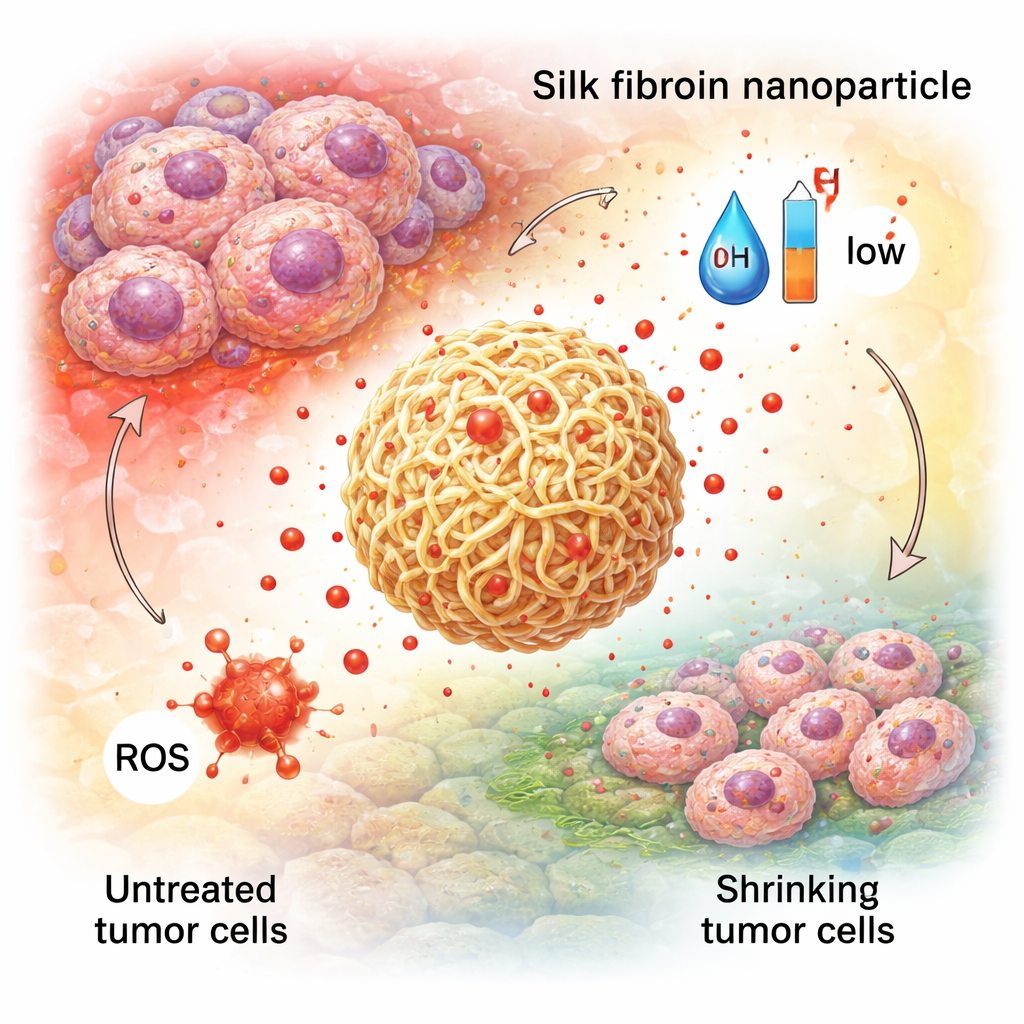
Tidiga framgångar vid cancer, tarmsjukdomar och sårreparation
Dessa designade partiklar har testats i många sjukdomsmodeller. Vid cancer har silkepartiklar bära cytostatika och till och med kombinationer av läkemedel plus ljusaktiverade ämnen, och visat bättre ansamling i tumörer, mer precis frisättning i den hårda tumörmiljön och färre biverkningar än fria läkemedel. Vid inflammatoriska tarmsjukdomar kan oralt administrerade silkepartiklar laddade med naturliga antioxidanter eller antiinflammatoriska föreningar fästa vid tarmens slemhinna, navigera genom den och frigöra sin last som svar på höga nivåer av reaktiva molekyler, vilket hjälper till att dämpa inflammation och reparera tarmbarriären. Inom vävnadsengineering och sårläkning blandas silkepartiklar in i stödstrukturer och hydrogel för att långsamt frigöra tillväxtfaktorer eller antibiotika, stärka benliknande material och snabba på tillslutningen och ren läkning av hudsår.
Att överbrygga klyftan från laboratorium till sjukhussäng
Trots lovande resultat befinner sig silkefibroin‑nanopartiklar fortfarande i preklinisk fas. Översikten belyser stora hinder: batch‑till‑batch‑skillnader beroende på hur silket bearbetas, spår av andra proteiner eller lösningsmedel som kan påverka säkerheten och svårigheten att producera stora volymer under strikta farmaceutiska kvalitetsregler. Mikrofluidisk tillverkning ger bättre kontroll men är i nuläget dyr och komplex att skala upp. Myndigheter kommer också att kräva tydlig förståelse för hur dessa partiklar bryts ner i kroppen, hur de elimineras och hur tillförlitligt de kan framställas. Författarna menar att grönare processer, standardiserade protokoll, kontinuerlig övervakning av partikelkvalitet och nära samarbete mellan akademiska laboratorier och industrin gradvis skulle kunna förvandla silkepartiklar från eleganta laboratoriedemonstrationer till vardagliga medicinska verktyg.
Vad detta kan innebära för patienterna
Enkelt uttryckt syftar silkefibroin‑nanopartiklar till att leverera mer läkemedel där det behövs och mindre där det inte gör det. Genom att använda ett biokompatibelt, biologiskt nedbrytbart protein som kan formas och finjusteras på flera nivåer hoppas forskare minska de hårda biverkningarna av cytostatika, erbjuda mer effektiv långtidshantering av tarminflammation och påskynda vävnadsreparation efter skada. Även om många tekniska och regulatoriska hinder kvarstår, tyder arbetet som sammanfattas i den här artikeln på att morgondagens "smarta" läkemedelsbärare kanske inte spunns av exotiska syntetiska material utan av samma silke som har klätt mänskligheten i tusentals år.
Citering: Bao, S., Yang, X., Reis, R.L. et al. Synthesis and application of silk fibroin nanoparticles for drug delivery. Commun Mater 7, 66 (2026). https://doi.org/10.1038/s43246-026-01108-x
Nyckelord: silkefibroin-nanopartiklar, målinriktad läkemedelsleverans, cancer-nanomedicin, inflammatorisk tarmsjukdom, vävnadsengineering