Clear Sky Science · sv
CAR‑anpassad PIK3CD‑basredigering förbättrar T‑cellers antitumorpotens
Omprogrammering av cancerbekämpande celler
Chimär antigenreceptor (CAR)‑T‑cellsterapi har revolutionerat behandlingen av vissa blodcancerformer, men många patienter drabbas fortfarande av återfall eller svarar aldrig. Ett grundläggande problem är att dessa konstruerade immunceller kan utmattas eller inte kvarstå i kroppen tillräckligt länge. Denna studie ställer en enkel men kraftfull fråga: istället för att helt redesigna CAR‑erna, vad händer om vi subtilt kan ”finjustera” T‑cellernas interna kopplingar så att de förblir kraftfulla längre, och göra det säkert?
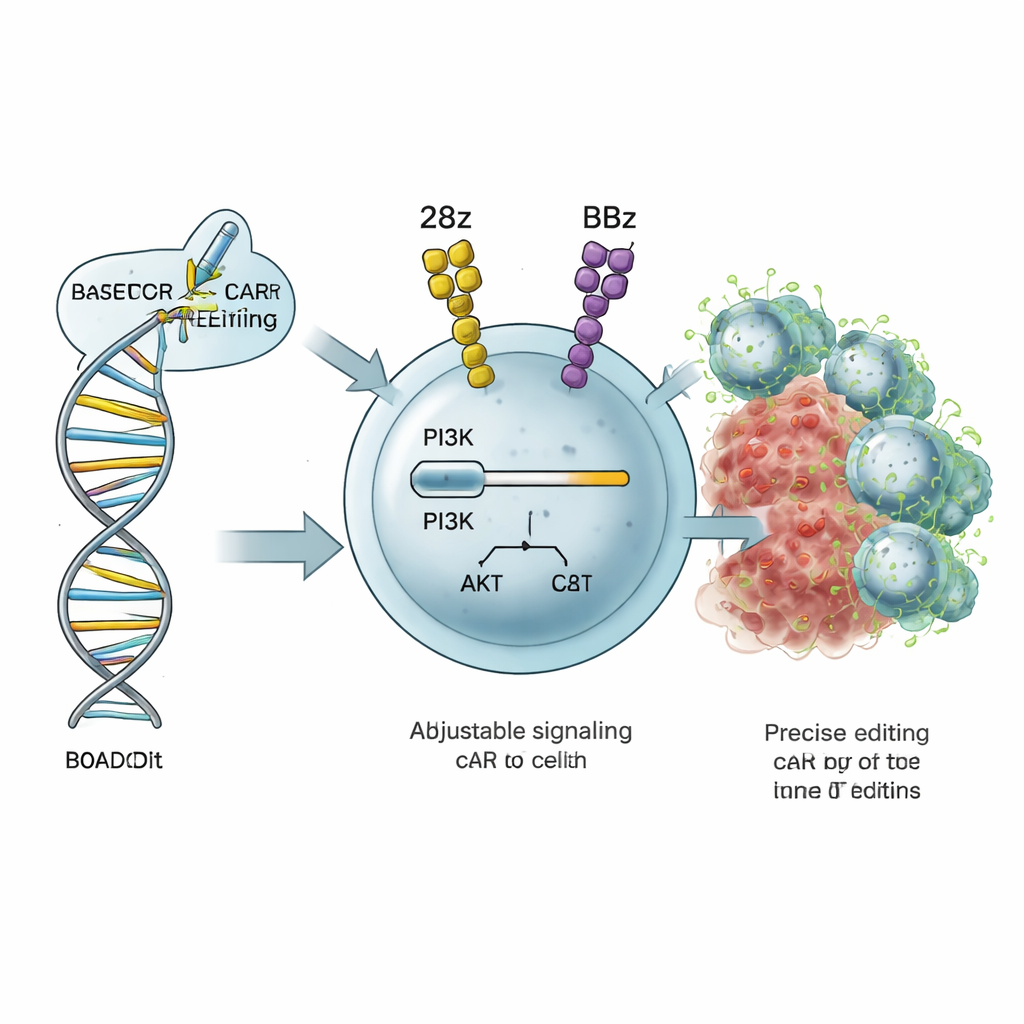
Sikta på T‑cellens volymknapp
De cancerbekämpande T‑cellerna är beroende av interna signalvägar som talar om hur starkt de ska aktiveras, hur snabbt de ska dela sig och om de blir kortlivade stridare eller långtidsminnesceller. En viktig krets är PI3K–AKT‑vägen, där ett protein kallat PI3Kδ—kodat av PIK3CD‑genen—fungerar som en volymknapp för aktivering och metabolism. Författarna utvecklade en strategi de kallar ROADSTAR, som använder basredigering, en mycket precis form av CRISPR‑genomteknik, för att ändra enstaka ”bokstäver” i PIK3CD. Istället för att slå på eller av vägen helt söker ROADSTAR efter små mutationer som milt ökar eller minskar signaleringen på ett sätt som bäst matchar den specifika CAR‑designen i T‑cellen.
Upptäcka nyttiga mutationer
Teamet byggde ett bibliotek med 34 olika enbokstavsändringar i den regulatoriska delen av PIK3CD och införlivade dem i humana T‑celler som redan bar en av två vanliga CAR‑designer: 28z (baserad på CD28‑molekylen) och BBz (baserad på 4‑1BB). Dessa CAR:er skiljer sig åt i hur de stimulerar T‑celler: 28z tenderar att driva en stark, snabb attack men också utmattning, medan BBz främjar bättre överlevnad och minne men kan vara mindre aggressiv. De redigerade CAR‑T‑cellerna utsattes för ett ”stressprov” genom upprepad exponering för leukemiceller. Med djupsekvensering följde forskarna vilka mutationer som gjorde att CAR‑T‑cellerna kunde konkurrera ut sina oredigerade motsvarigheter över flera veckor.
Två mutationer stack tydligt ut. I BBz CAR‑T‑celler ökade en förändring kallad E81K något PI3Kδ‑aktiviteten, vilket förstärkte signalerna nedströms i PI3K–AKT‑vägen. I 28z CAR‑T‑celler dämpade en annan förändring, L32P, PI3Kδ‑aktiviteten. Strukturell modellering antydde att båda ändringarna subtilt förändrar hur PI3Kδ interagerar med sin regulatoriska partner, och fintunade signalstyrkan snarare än att slå den helt på eller av. Viktigt är att den gynnsamma mutationen för en CAR‑design inte var densamma som för den andra, vilket understryker att varje CAR‑arkitektur kräver sin egen optimala interna inställning.
Starkare, fräschare och mer långlivade CAR‑T‑celler
När de lovande ändringarna testades individuellt gjorde E81K BBz CAR‑T‑celler mer aktiverade vid tumörkontakt, bättre på att proliferera och avsevärt mer effektiva på att döda cancermål, även sådana med låg antigenhalt. Dessa celler utvecklades till effektorminnes‑T‑celler som kombinerade kraftfull dödlighet med förmågan att bestå. I musmodeller för leukemi och metastaserande neuroblastom kontrollerade E81K‑redigerade BBz CAR‑T‑celler tumörer mer fullständigt och under betydligt längre tid än oredigerade BBz‑celler, och lyckades till och med hantera flera omgångar av tumörrechallenge. Detaljerad enskildcells‑RNA‑ och metabolisk profilering visade att E81K‑celler hade förbättrad mitokondriefunktion, högre reserverad respiratorisk och glykolytisk kapacitet och färre tecken på utmattning—i praktiken var de mer energiska och motståndskraftiga.
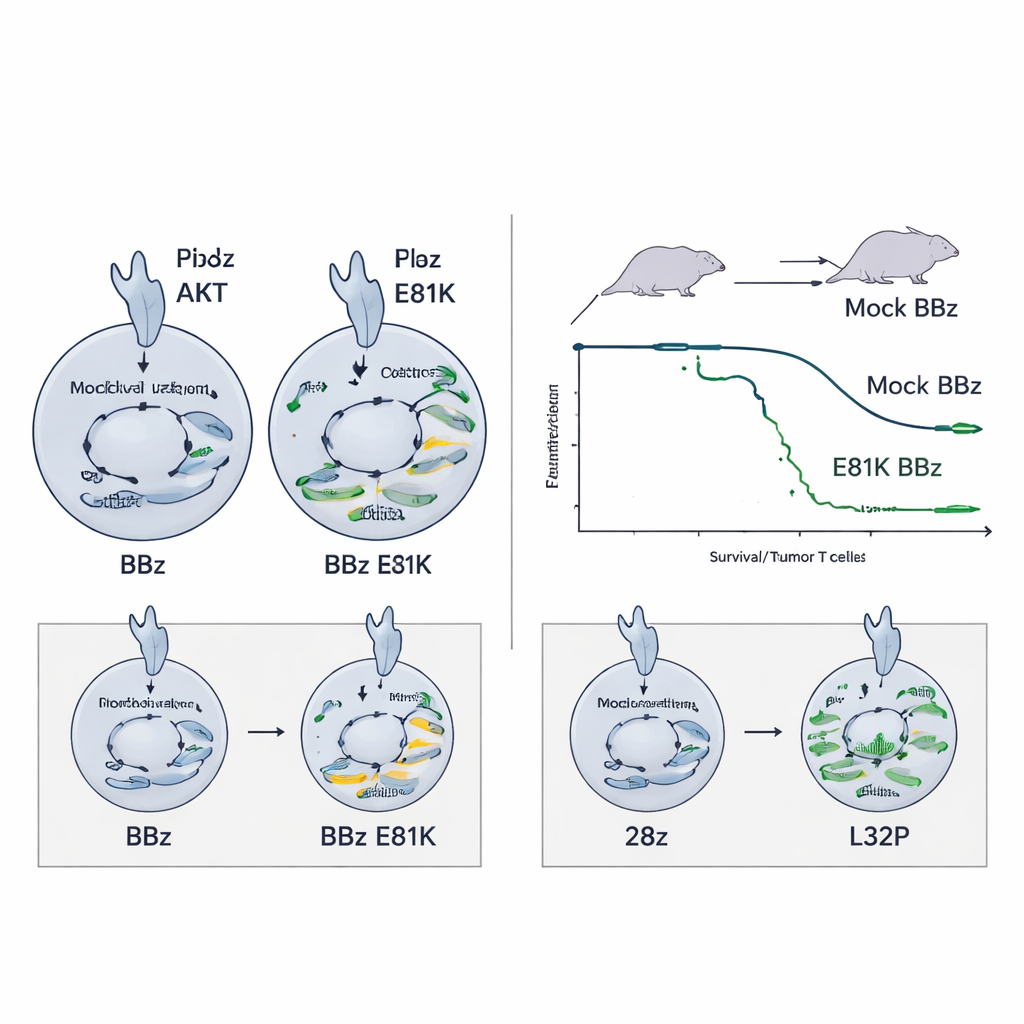
Förebygga utmattning i mycket aktiva CAR:er
Samma E81K‑förstärkning hjälpte inte—och kunde till och med skada—28z CAR‑T‑celler, som redan signalerar starkt. I det här sammanhanget ökade extra PI3K‑aktivitet markörer för utmattning utan att förbättra funktionen. Här visade sig L32P‑mutationen vara bättre lämpad: genom att dämpa PI3K–AKT‑signaleringen måttligt visade L32P‑redigerade 28z CAR‑T‑celler reducerad basal aktivering men bibehöll hög dödande kapacitet och prolifererade mer över tiden. De upprätthöll också ett mindre differentierat, minnesliknande tillstånd, inklusive en stamcellsliknande minnespool som tros stödja långsvar. I en krävande neuroblastommodell förbättrade L32P‑modifierade 28z CAR‑T‑celler överlevnaden jämfört med sina oredigerade motsvarigheter.
Säkerhet och framtida möjligheter
En central oro vid permanent förändring av immunsignalering är risken för okontrollerad tillväxt eller sekundära cancerformer. Författarna genomförde därför omfattande säkerhetskontroller. E81K‑redigerade BBz CAR‑T‑celler visade inte onormal tillväxt i kultur, orsakade inte organskada eller inflammatoriska kriser i möss och visade inga tecken på lymfom eller vävnadsinvasion månader efter infusion. Kliniska databaser visar också ingen överrepresentation av dessa specifika PIK3CD‑mutationer i T‑cellsleukemier. Sammantaget visar arbetet att noggrant utvalda enbokstavs‑genomändringar kan fungera som precisionsdimmrar för T‑cellsbeteende—som ökar antitumorstyrka och uthållighet samtidigt som varje CAR:s unika biologi respekteras. Denna ROADSTAR‑strategi kan bidra till att utforma nästa generationens CAR‑T‑terapier som är både effektivare och mer pålitliga vid blodcancer och potentiellt även solida tumörer.
Citering: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Nyckelord: CAR‑T‑celler, PI3K‑signalering, basredigering, cancerimmunterapi, T‑cellsmetabolism