Clear Sky Science · sv
De novo H3.3K27M-förändrad diffus mittlinjegliom i mänskliga hjärnstamsorganoider för att dissekera GD2 CAR-T-cellsfunktion
Varför denna studie av barndomshjärncancer är viktig
Diffust mittlinjegliom är en av de mest dödliga barndomscancerformerna i hjärnan, som drabbar mycket små barn i hjärnstammen och lämnar familjer med nästan inga effektiva behandlingsalternativ. Eftersom tumörerna sitter djupt i hjärnan och sällan opereras bort har forskare lite vävnad att studera och få säkra sätt att pröva nya terapier. Denna studie bygger en realistisk “mini-hjärnstam i en skål” och använder den för att följa hur en lovande immunterapi — GD2 CAR-T-celler — beter sig över veckor, inklusive varför den ibland misslyckas.
Att bygga en mini-hjärnstam i laboratoriet
Teamet började med mänskliga stamceller och styrde dem, steg för steg, att växa till tredimensionella hjärnorganoider som liknar hjärnstamsregionen pons, där dessa tumörer vanligtvis uppstår. Genom noggrann timing av tillväxtsignaler framställde de organoider som var rika på samma typer stödjeceller, eller glia, som normalt finns i detta område. Detaljerade genetiska analyser visade att celldifferentiering och mognad följde mönster som ses i tidig mänsklig hjärnutveckling, särskilt de gliala linjerna typiska för pons och närliggande medulla. Det innebar att organoiderna kan fungera som en realistisk bakgrund för att studera hur denna cancer startar och växer.
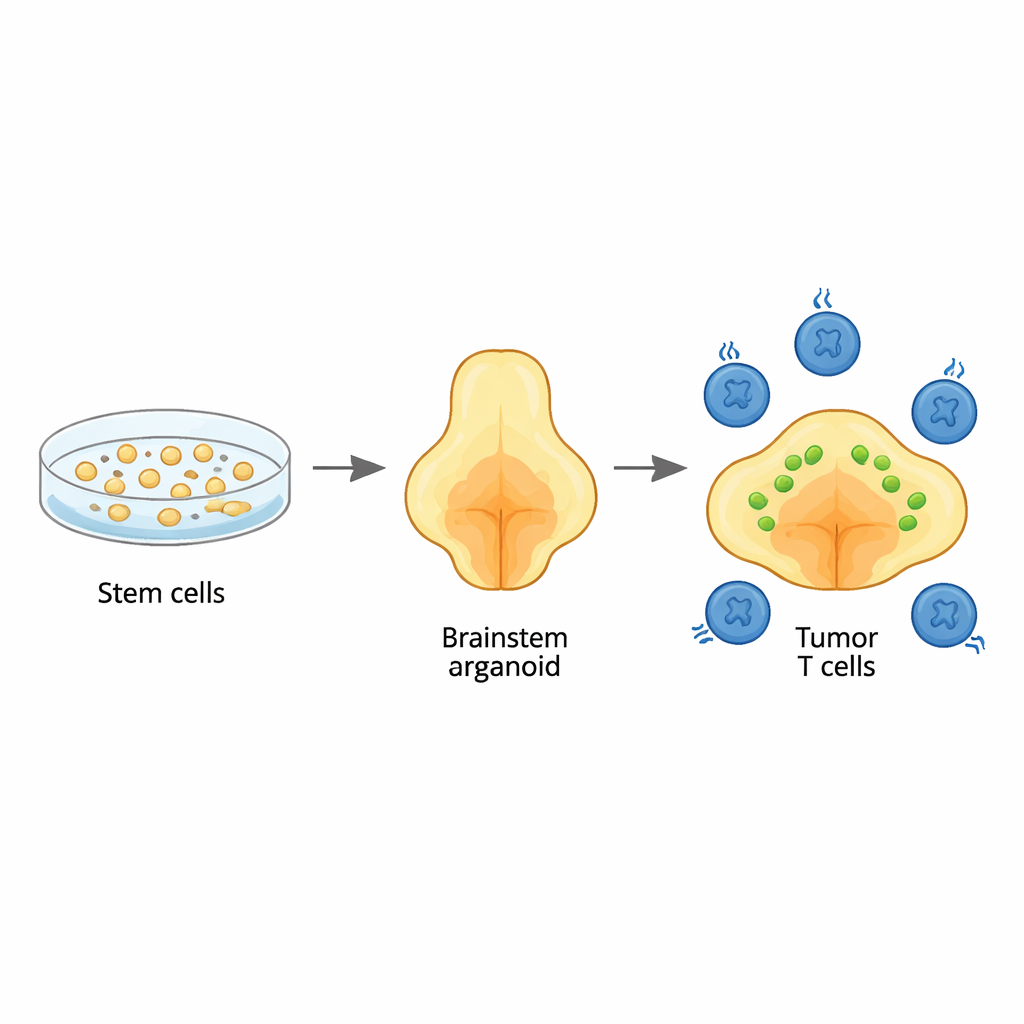
Återskapa barnets tumör inne i organoiden
För att efterlikna diffust mittlinjegliom införde forskarna tre centrala genetiska förändringar i unga organoider: en typisk mutation i ett histonprotein (H3.3K27M), förlust av tumörsuppressorn TP53 och en aktiverande förändring i tillväxtreceptorn PDGFRA. När dessa introducerades i ett mycket tidigt utvecklingsstadium blev utvalda glialiknande celler cancerösa. De resulterande tumörerna spred sig diffust genom organoiderna, precis som de gör i barns hjärnstammar, och bar samma breda DNA- och RNA-signaturer som ses i patienttumörer. Enkelcellssekvensering visade en blandning av cancercellstillstånd, inklusive omogna, pons-specifika glialceller som motsvarar dem som finns i verkliga pediatriska tumörer, vilket understryker att modellen troget återskapar den mänskliga sjukdomen.
Att se hur immunterapier bekämpar — och tröttas ut — över tid
Med denna tumör-i-hjärnstamsmodell på plats tillsatte teamet GD2 CAR-T-celler — patienters T-celler konstruerade för att känna igen en molekyl kallad GD2 på tumörceller — och följde både tumörstorlek och T-cellernas beteende i upp till en månad. Vissa organoider visade stark tumörkrympning, andra endast partiell kontroll, vilket speglar de blandade utfallen i kliniska prövningar. Enkelcells-RNA-sekvensering av mer än 20 000 CAR-T-celler exponerade för tumörerna avslöjade en oväntad mångfald av T-cellstillstånd. Vissa celler var högt cytotoxiska ”mördare”, andra var aktiverade men inte fullt dödande, och en distinkt grupp uppvisade kännetecken för utmattning, med nedreglerade cancerslukande gener och hög uttrycksnivå av hämmande ”bromsar”. De utmattade cellerna liknade starkt utarbetade T-celler sedda vid kroniska infektioner och i mänskliga tumörer, vilket tyder på att organoid-systemet fångar kliniskt relevanta T-cellsutmattningar drivet av fortsatt kontakt med cancer.
Att hitta kraftfulla men kortlivade T-celler
Vid närmare granskning identifierade forskarna en undergrupp av CAR-T-celler märkta av ett ytprotein kallat NCAM1 som var särskilt effektiva kortsiktiga mördare. När dessa NCAM1-positiva celler isolerades och användes ensamma kontrollerade de tumörerna starkare initialt än sina NCAM1-negativa motsvarigheter. De blev dock också utmattade och minskade snabbare, vilket ledde till svagare kontroll över tid. Denna avvägning mellan omedelbar kraft och uthållighet hjälper till att förklara varför CAR-T-terapier kan ge dramatiska men temporära svar och antyder att förval av eller omformning av T-cellsundergrupper kan optimera behandlingens varaktighet.
Hur hjärnans immunceller kan dämpa terapin
I den riktiga hjärnan omges tumörer inte bara av neuroner och glia utan också av mikroglia, hjärnans egna immunceller. För att fånga detta komplexitetslager tillsatte forskarna mikroglia härledda från stamceller i sina organoider. Dessa celler mognade, antar former och genuttrycksmönster specifika för mikroglia som hittas i diffust mittlinjegliom, och producerade molekyler förknippade med en immunosuppressiv miljö. När CAR-T-celler tillsattes till tumörbärande organoider som innehöll mikroglia skiftade T-cellerna ytterligare mot utmattade och lågeffektiva tillstånd, och tumörkontrollen försämrades. Samtidigt steg inflammatoriska faktorer kopplade till behandlingsbiverkningar, såsom IL-6, vilket tyder på att modellen också kan hjälpa till att studera CAR-T-relaterad toxicitet.
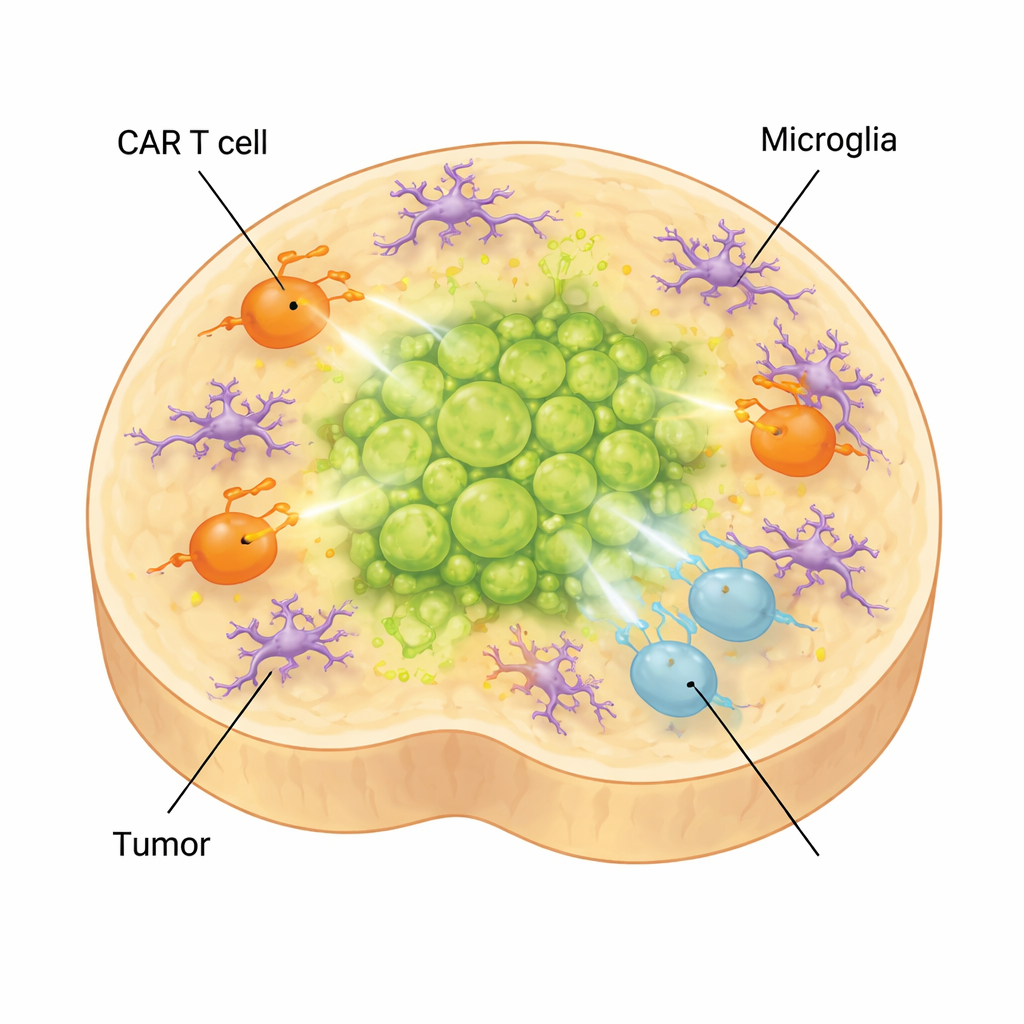
Vad detta betyder för barn med denna cancer
För familjer som står inför diffust mittlinjegliom erbjuder detta arbete ännu ingen ny bot, men det ger en kraftfull testplattform för att nå dit snabbare. Genom att återskapa ett barns hjärnstamsmiljö och tumör i en skål kan forskare nu i realtid observera hur olika tumörceller, CAR-T-cellstyper och mikroglia interagerar över veckor. Detta gör det möjligt att identifiera vilka konstruerade T-celler som är mest effektiva, hur och när de blir utmattade och hur hjärnans immunceller underminerar deras insatser. I slutändan kan sådana organoidmodeller bli personaliserade för enskilda patienter och användas för att finslipa immunterapier innan de ges, vilket förbättrar möjligheterna att framtida CAR-T-behandlingar blir både säkrare och mer effektiva för barn.
Citering: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Nyckelord: diffust mittlinjegliom, hjärnorganoider, CAR-T-celler, barnhjärncancer, mikroglia