Clear Sky Science · sv
Förutsäga och tolka celltypsspecifika läkemedelsresponser i små datamängder med induktiva priorer
Varför denna forskning är viktig för framtidens läkemedel
När ett nytt läkemedel testas är en av de största osäkerheterna hur olika det kommer att påverka de många celltyperna i våra kroppar. En förening som hjälper en celltyp kan göra lite för en annan eller till och med vara skadlig. Att experimentellt generera denna information för tusentals läkemedel och otaliga celltyper är både för långsamt och för dyrt. Denna artikel presenterar en datorbaserad metod, kallad PrePR-CT, som lär sig förutsäga hur enskilda celltyper svarar på läkemedel, även när endast begränsade data finns tillgängliga. Arbetet pekar mot snabbare, billigare och mer precisa sätt att utforska potentiella läkemedel i silico innan man satsar på kostsamma labb- och kliniska studier.
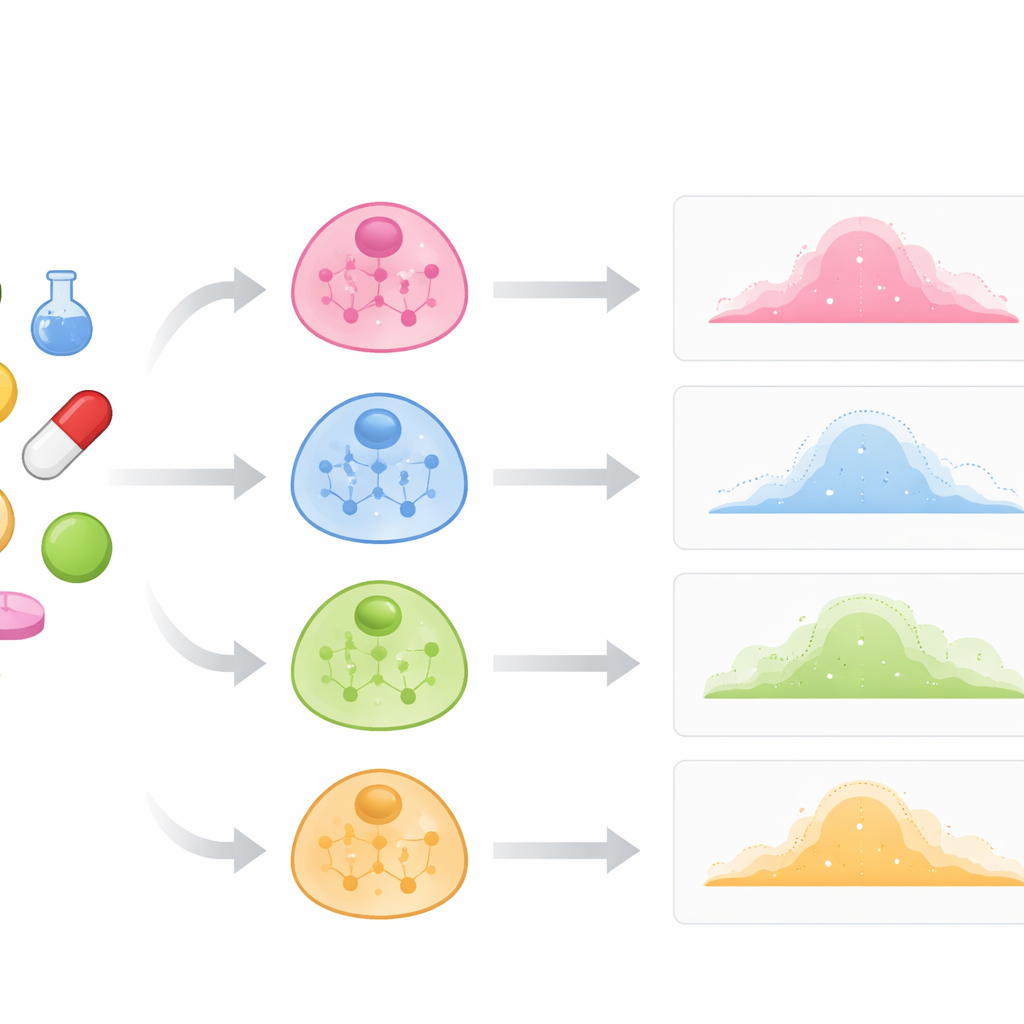
Att titta inne i cellerna istället för bara på läkemedlen
Traditionella läkemedelsscreeningar behandlar ofta celler som om de vore likadana och fokuserar främst på aggregerade medelvärden. I verkligheten kan immunceller, leverceller och cancerceller reagera mycket olika på samma förening. Författarna hävdar att för att förutsäga dessa skillnader måste en modell förstå varje celltyps interna kopplingar: vilka gener som tenderar att vara aktiva samtidigt och hur dessa mönster definierar cellens identitet. De bygger celltypens ”kartor” genom att undersöka vilka gener i opåverkade (kontroll-)celler som stiger och sjunker samtidigt. Varje karta representeras som ett nätverk där noder motsvarar gener och länkar speglar stark samaktivitet. Dessa nätverk fungerar som tidigare kunskap om hur en given celltyp är organiserad innan något läkemedel tillsätts.
En nätverksmedveten inlärningsmotor
PrePR-CT kombinerar tre ingredienser: en celltyps genaktivitetsnätverk, celltypens basala genuttryck och en kompakt beskrivning av läkemedlets kemiska struktur. Modellen använder en klass av neurala nätverk utformade för grafer för att bearbeta cellens gennätverk och extrahera en sammanfattning som fångar dess karakteristiska mönster. Parallellt omvandlas varje läkemedel till ett numeriskt fingeravtryck härlett från dess molekylära struktur. Dessa delar matas in i en efterföljande prediktionsmodul som från tillgängliga experiment lär sig hur ett givet läkemedel kommer att skifta fördelningen av genaktivitet i den celltypen. Istället för att producera ett enda tal per gen uppskattar metoden både genomsnittlig förändring och hur variabel responsen är över individuella celler, vilket är avgörande för att förstå såväl subtila som starka effekter.
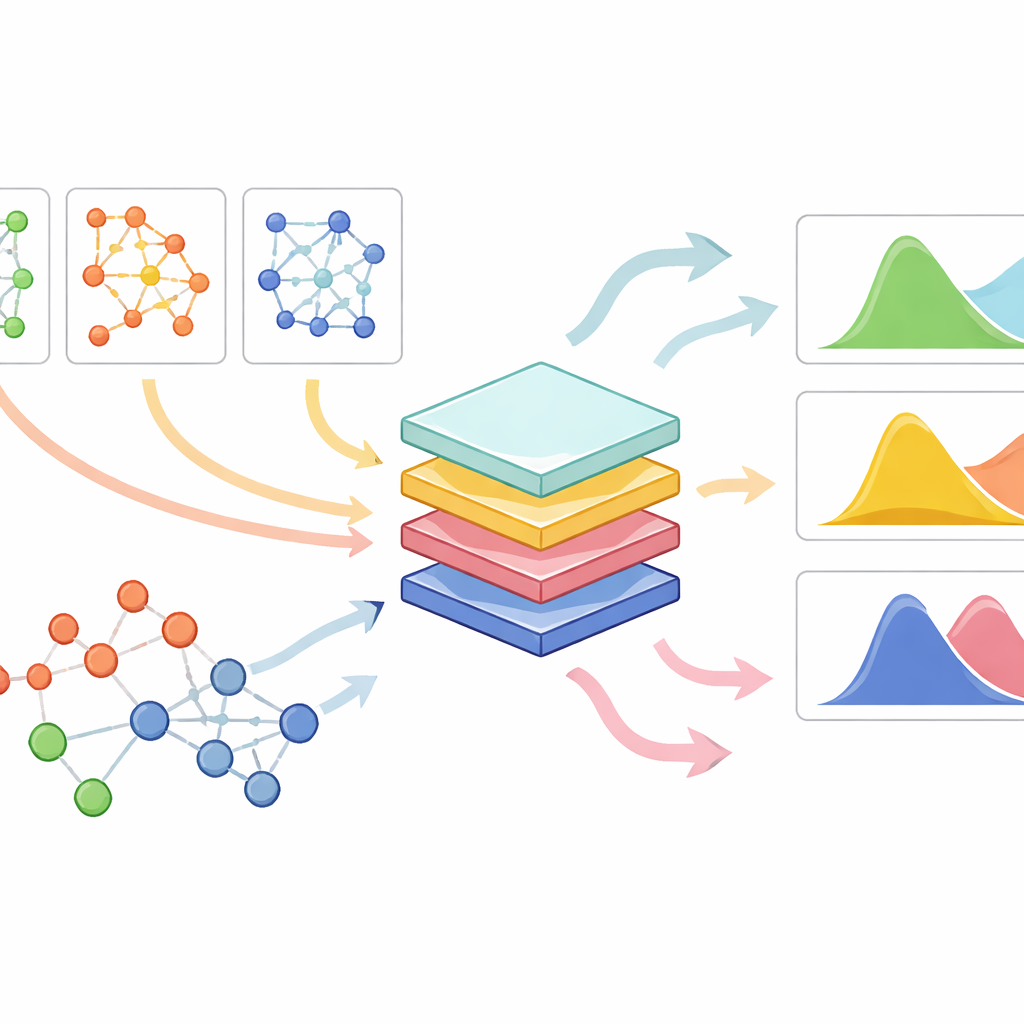
Att arbeta över många celltyper, läkemedel och små datamängder
Forskarna testade PrePR-CT på en bred samling dataset, inklusive mänskliga blodceller exponerade för immunsignaler, flera cancercellinjer behandlade med olika föreningar, musleverceller utsatta för en förorening och storskaliga läkemedelsscreeningar från offentliga resurser. I utmanande scenarier där en hel celltyp hölls utanför träningen kunde modellen ändå förutsäga hur den nya celltypen skulle svara på ett bekant läkemedel, ofta med bättre noggrannhet än tidigare generativa modeller. På samma sätt, när ett nytt läkemedel men en bekant celltyp hölls utanför, förutsåg metoden framgångsrikt dess påverkan enbart med hjälp av dess kemiska fingeravtryck. Viktigt är att modellen förblev effektiv när den tränades på relativt små antal celler — en situation där många djupa lärande-metoder har problem.
Från svart låda till ledtrådar om mekanism
Utöver rå förutsägelse ville författarna veta om deras modell kunde erbjuda insikt i vilka gener och vägar som driver en cells respons. Den grafbaserade arkitekturen inkluderar en attention-mekanism som lyfter fram gener som modellen bedömer vara särskilt inflytelserika i varje celltyp. Många av dessa ”hög-attention”-gener var inte de vanliga misstänkta som framhävs av standard analys av differentialuttryck, men de klustrade i immunsrelaterade vägar som är förenliga med biologin för de testade läkemedlen. När forskarna avsiktligt störde dessa inflytelserika gener i modellens input sjönk prediktionskvaliteten, särskilt för de mest responsiva generna, vilket tyder på att attention-poängen pekar på meningsfulla mekanistiska aktörer snarare än brus.
Vad detta betyder för att designa bättre läkemedel
Enkelt uttryckt visar detta arbete att när man ger artificiella intelligensmodeller en strukturerad bild av hur varje celltyp är kopplad — dess interna gennätverk — förbättras deras förmåga avsevärt att förutsäga hur läkemedel kommer att omforma dessa celler, även när bara måttliga datamängder finns. PrePR-CT ersätter inte experiment, men kan hjälpa till att begränsa vilka föreningar och celltyper som är värda att testa och ge ledtrådar om varför vissa celler reagerar som de gör. Allt eftersom dataset växer och ytterligare cellulära egenskaper inkluderas kan sådana tillvägagångssätt bli nyckelverktyg för att skräddarsy behandlingar till specifika vävnader eller patientcelltyper, minska prov-och-fel i labbet och föra mer precisa läkemedel närmare verklighet.
Citering: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Nyckelord: förutsägelse av läkemedelsrespons, single-cell-transkriptomik, grafneuronätverk, läkemedelsupptäckt, celltypsspecificitet