Clear Sky Science · sv
Återanvändbarhetsrapport: Utvärdering av prestandan hos en meta-lärande grundmodell för att förutsäga antibakteriell aktivitet hos naturliga produkter
Söka nya antibiotika — snabbare
Antibiotikaresistensen ökar, men upptäckten av nya läkemedel går smärtsamt långsamt och bygger ofta på trial-and-error i laboratoriet. Denna studie undersöker om en kraftfull form av artificiell intelligens, ursprungligen tränad på stora samlingar av läkemedelsdata, snabbt kan anpassas för att förutsäga vilka växtbaserade naturliga föreningar som kan bekämpa bakterier — med endast små mängder ny experimentell data. Om det fungerar kan sådana verktyg hjälpa forskare att fokusera värdefull labbtid på de mest lovande kandidaterna och påskynda sökandet efter nästa generation antibiotika.
Därför spelar växtkemikalier roll
Många av våra bästa antibiotika började som naturliga produkter från växter och mikrober. Dessa molekyler kan stoppa bakterietillväxt, men att hitta nya i naturen är lite som att leta efter nålar i en höstack. Forskare måste testa många föreningar mot många bakteriestammar, och varje test är kostsamt. Än värre är att stora, noggrant annoterade dataset — som moderna djupinlärningsmetoder behöver för att prestera väl — är sällsynta inom detta område. Det gör antibiotikaupptäckt till en idealisk prövningsplats för så kallade ”grundmodeller”: stora, allmänna AI-system som kan finkalibreras för specifika uppgifter med endast ett fåtal nya exempel.
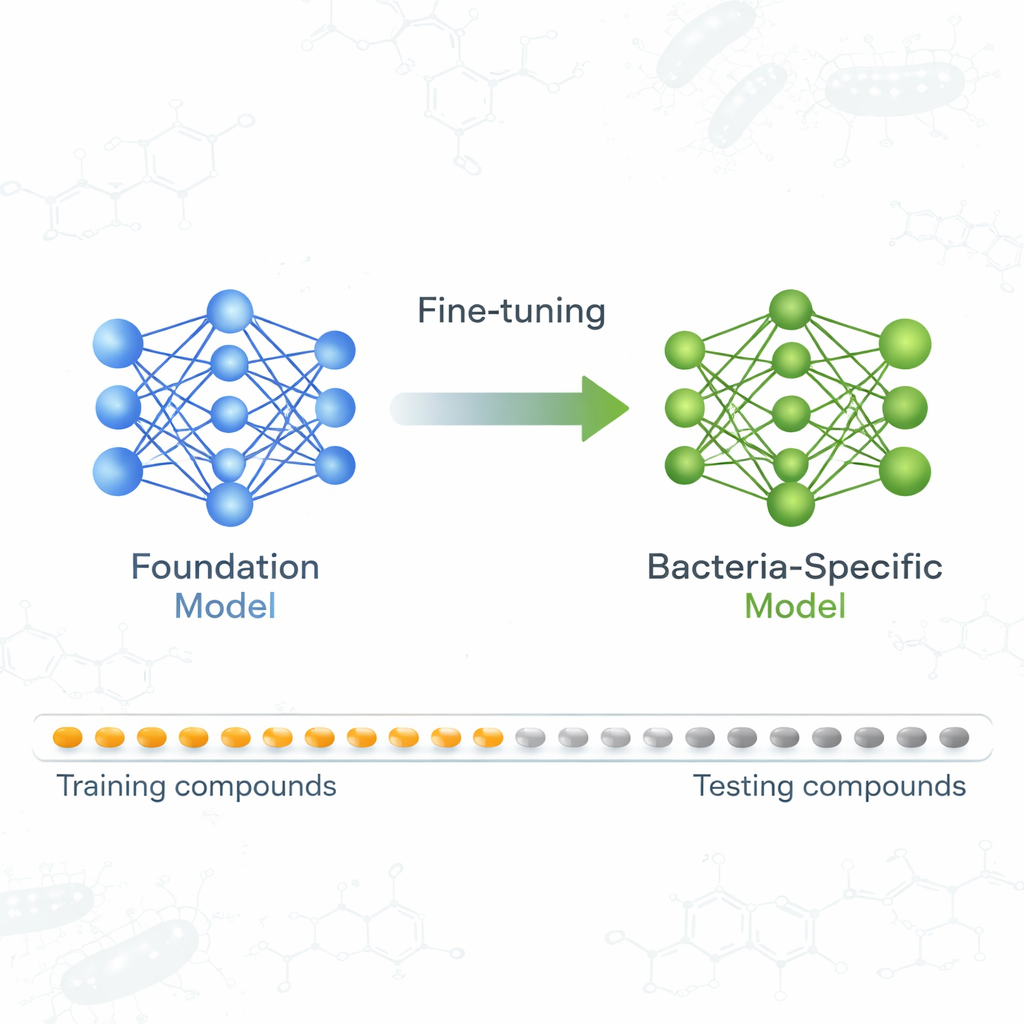
En grundmodell lär sig om bakteriedödare
Teamet fokuserade på en grundmodell kallad ActFound, ursprungligen tränad för att förutsäga hur starkt olika kemikalier påverkar biologiska mål, med hjälp av stora dataset från resurser som ChEMBL och BindingDB. Istället för att förutsäga ett enda tal för varje förening lär sig ActFound genom att jämföra par av föreningar inom samma experiment och uppskatta vilken som är mer aktiv. Detta ”parvisa” lärande, kombinerat med en träningsstrategi känd som meta-lärande, är avsett att hjälpa modellen att snabbt anpassa sig till nya förutsägelseuppgifter när endast ett litet antal annoterade exempel finns tillgängliga — precis den situation som gäller i många antibiotikascreeningar.
Test av modellen på verkliga växtdata
För att se hur återanvändbar ActFound verkligen är finjusterade författarna den på ett kurerat dataset av växtbaserade naturliga produkter testade för sin förmåga att hämma tillväxten hos olika bakterier. Varje bakteriestam behandlades som en egen uppgift, och modellen anpassades med endast 8 till 128 föreningar per stam, eller fasta procentandelar av den tillgängliga datan. De jämförde också ActFound med enklare meta-lärande- och transfer-lärande-modeller som inte använder parvisa jämförelser. I dessa tester nådde ActFound inte den noggrannhet som visats i tidigare arbete på andra typer av läkemedelsdata. Men när väldigt lite data fanns tillgängligt — ungefär endast ett fåtal föreningar per stam — matchade ActFound och dess transfer-lärande-variant generellt eller överträffade alternativa metoder.
När likhet hjälper — och när den stjälper
ActFound antar att liknande molekyler beter sig likartat, vilket fungerar bra när dataset byggs kring grupper av besläktade kemikalier. Det naturliga produktdatasetet var dock kemiskt mångsidigt och saknade ofta nära besläktade ”familjer” av föreningar. Denna mångfald, även om den är vetenskapligt värdefull, undergrävde den parvisa lärandestrategin: när föreningar inom ett experiment är mycket olika varandra får modellen svårt att lära sig stabila jämförelser. Författarna fann också att en enkel diagnostik, föreslagen i den ursprungliga ActFound-artikeln för att förutsäga i förväg hur väl modellen skulle prestera på en ny uppgift, inte höll för dessa data om naturliga produkter, vilket belyser en viktig begränsning vid överföring till nya kemiska områden.
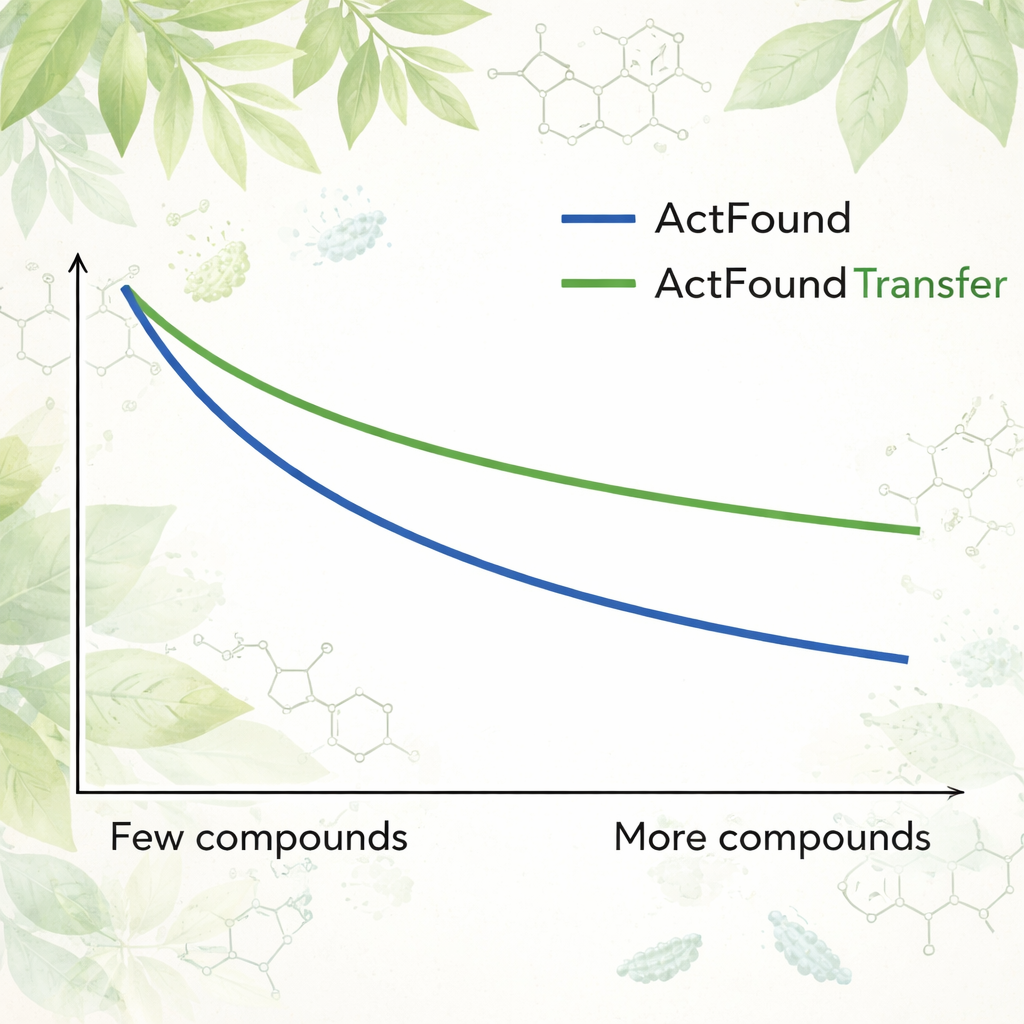
Vad detta betyder för framtida läkemedelsupptäckt
För icke-specialister är slutsatsen att grundmodeller som ActFound är lovande verktyg för läkemedelsupptäckt när data är knappa, men de är inga universallösningar. I denna studie presterade ActFound och dess transfer-lärande-version ofta lika bra som eller bättre än konkurrerande metoder när endast ett fåtal växtföreningar fanns tillgängliga för träning, men de hade svårt med denna mycket divergerande uppsättning naturliga produkter. Arbetet antyder att dessa AI-modeller är mest användbara när datan innehåller många kemiskt lika föreningar — till exempel i fokuserade studier av struktur–aktivitetssamband — men de förblir mindre tillförlitliga för att förutsäga hur helt nya typer av molekyler kommer att bete sig. Med andra ord kan AI hjälpa till att avgränsa sökningen, men den svåraste delen av att utforska verkligt ny kemisk mark återstår fortfarande.
Citering: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Nyckelord: antibiotikaupptäckt, naturliga produkter, djupinlärning, meta-lärande, läkemedelsscreening