Clear Sky Science · sv
Fosforylering av PLIN5 orkestrerar kopplingen mellan mitokondrier och lipiddroppar för att kontrollera leverns lipidflöde och steatos
Varför leverfett är viktigt
Många personer har extra fett i levern utan att känna sig sjuka, men denna tysta ansamling kan så småningom leda till inflammation, ärrbildning och till och med cancer. Denna studie ställer en enkel men avgörande fråga: när vågor av fett når levern under fasta eller via en fet "västerländsk" kost, hur bestämmer levercellerna om fettet ska förbrännas för energi eller lagras säkert, och när börjar detta skyddssystem att svikta?
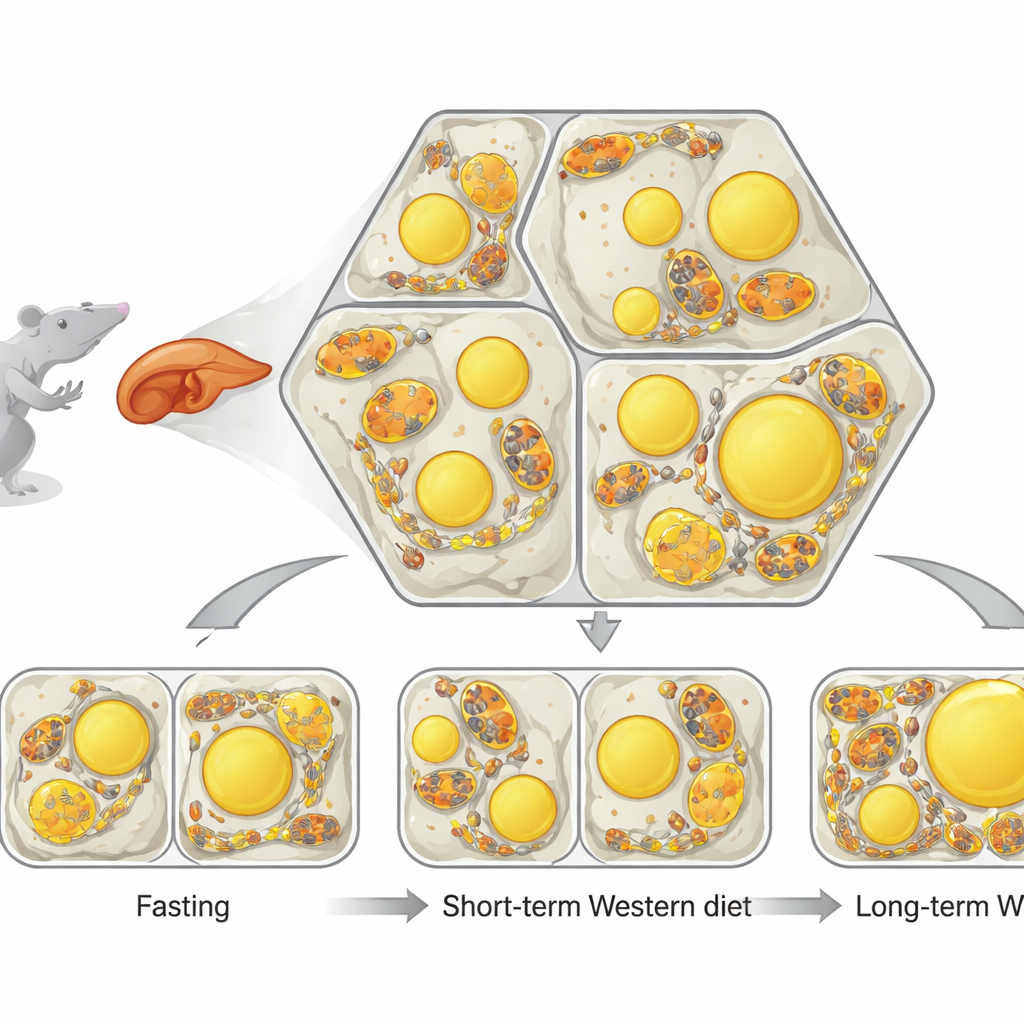
Små kraftverk och små fettbubblor
Levern är organiserad i upprepade, hexagonliknande enheter där blodet flyter från ena sidan till den andra. Längs denna väg specialiserar sig levercellerna: vissa förbränner mest fett för energi, medan andra främst tillverkar och lagrar fett. Inuti varje cell är två strukturer avgörande. Mitokondrierna är cellens kraftverk, och lipiddropparna är små fettfyllda bubblor för lagring. Forskarna utvecklade en kraftfull bild- och analysmetod, kallad single-cell phenotypic profiling (scPhenomics), för att kartlägga storlek, form och arrangemang av dessa strukturer i tusentals celler direkt i vävnadssnitt. De fann att även hos friska djur bildar mitokondriernas form och innehållet av lipiddroppar distinkta rumsliga mönster som speglar var förbränning respektive lagring normalt sker i levern.
Fasta kontra rik kost
Nästa fråga teamet ställde var vad som händer när levern plötsligt översvämmas av fett. Fasta driver ut fett från kroppens fettdepåer till levern, medan en kortvarig västerländsk kost levererar extra fett direkt från maten. Hos fastande möss ökade lipiddropparna i hela levern, och mitokondrierna blev längre och ofta tätt insvepta runt dessa fettbubblor, vilket bildade många kontaktpunkter. I möss som åt en västerländsk diet under flera veckor fylldes levern också med fett, men dropparna var arrangerade annorlunda och mitokondrierna förblev för det mesta separata och mer runda. Detta visade att sättet fettet anländer på — genom fasta eller kronisk rik mat — triggar mycket olika strukturella svar inne i levercellerna, även när den totala fettmängden ser liknande ut.
En molekylär strömbrytare för fettbehandling
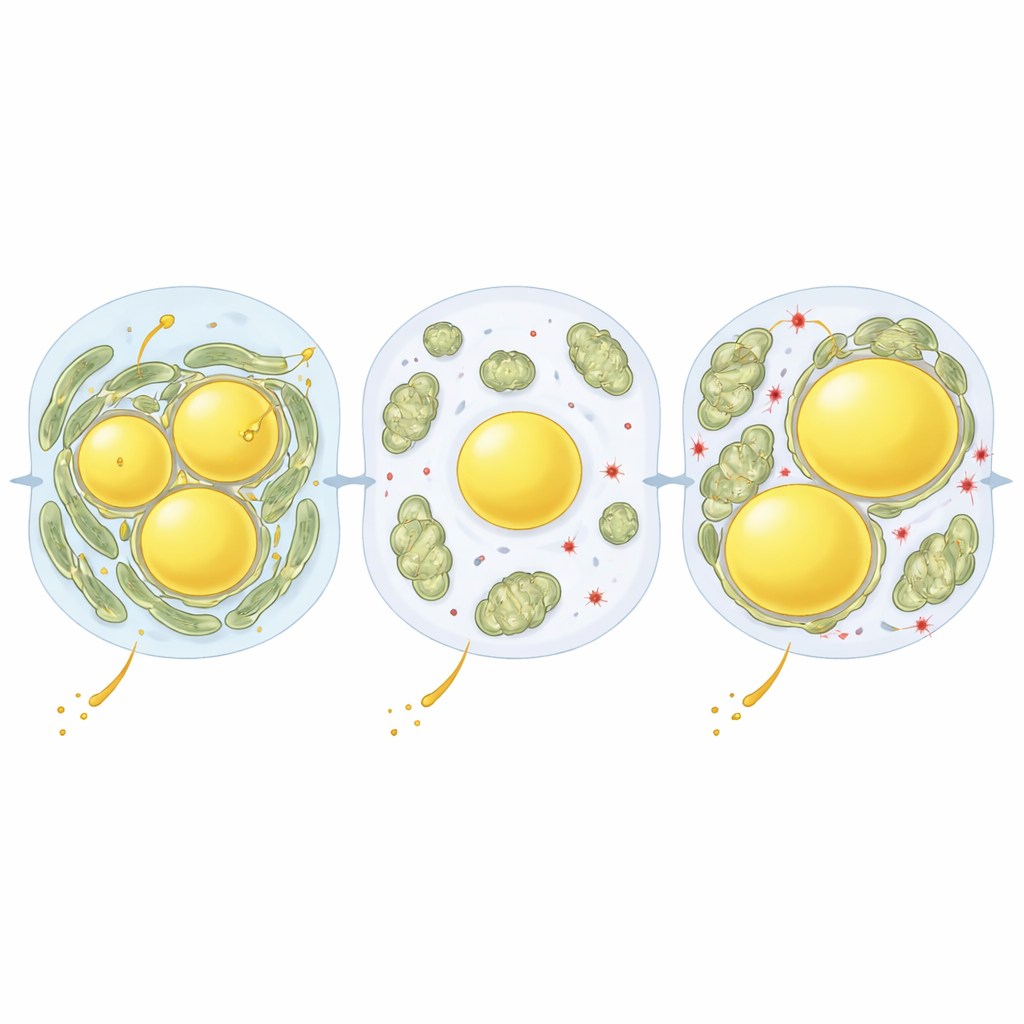
För att ta reda på vad som kontrollerar dessa organellkontakter kombinerade författarna sina bilder med proteinmätningar i leverceller tagna från olika zoner och kostförhållanden. Ett framträdande protein var perilipin‑5 (PLIN5), som täcker lipiddropparna och kan fästa mitokondrier vid dem. Fasta ökade PLIN5-nivåerna och placerade det precis i gränsytan mellan mitokondrier och droppar. Forskarna använde sedan ett leverriktat virus för att höja PLIN5-nivåerna och testa varianter av proteinet som efterliknar olika på/av-tillstånd för en enda kemisk märkning kallad fosforylering. En variant som inte kunde fosforyleras (S155A) ökade kraftigt kontakterna mellan mitokondrier och droppar och förstorade fett-dropparna, även vid normal kost. En variant som efterliknade konstant fosforylering (S155E) gjorde tvärtom: mitokondrier rörde sig sällan vid dropparna, som förblev färre och mindre.
Skydda celler från fettdriven skada
Teamet undersökte sedan vad detta betydde för leverhälsan under en västerländsk diet. När möss åt denna kost i flera veckor drev den icke-fosforylerbara PLIN5-varianten (S155A) mer fett in i dropparna och höjde leverns triglyceridinnehåll, ändå var markörer för skadlig oxidativ stress faktiskt lägre. Däremot lämnade fosfo-mimiken (S155E) mer fritt fett och tecken på en mer oxiderande, potentiellt skadlig miljö, med lägre antioxidativa reserver. I praktiken verkade nära partnerskap mellan mitokondrier och lipiddroppar fungera som en säkerhetsventil, som kanaliserar överskott av fettsyror till neutrala lagringsformer och begränsar de kemiska kedjereaktioner som skadar membran och proteiner. Vid längre perioder med västerländsk kost ökade dock mitokondrie–dropp-kontakter igen och var förknippade med tyngre fettbelastning i både möss och mänskliga leverprover, vilket antyder att samma skyddande koppling kan bli överbelastad och bidra till sjukdomsprogression.
En ny möjlighet vid leverfettssjukdom
Sammantaget visar detta arbete att leverceller aktivt omskriver de fysiska relationerna mellan sina kraftverk och sina fettlager för att hantera förändrade näringsförhållanden. PLIN5, och särskilt dess fosforyleringsstatus vid en enda plats, fungerar som en finjusteringsknapp som stärker eller lösgör kopplingen mellan mitokondrier och lipiddroppar. Tät koppling främjar inpackningen av potentiellt toxiskt fritt fett i säkrare triglyceridförråd och hjälper till att buffra kortvariga näringsstressorer, som fasta eller kort exponering för en rik diet. När detta adaptiva program dämpas, eller när exponering för hög fetthalt kvarstår i månader eller år, tippar balansen mot lipotoxicitet och oxidativ skada. Genom att avslöja denna strukturella "krets" inne i levercellerna antyder studien att läkemedel som modulerar PLIN5-aktivitet eller mitokondrie–dropp-kontakter skulle kunna erbjuda ett nytt sätt att sakta ner eller förebygga fettlever hos människor.
Citering: Kang, S.W.S., Brown, L.A., Miller, C.B. et al. PLIN5 phosphorylation orchestrates mitochondria lipid-droplet coupling to control hepatic lipid flux and steatosis. Nat Metab 8, 587–603 (2026). https://doi.org/10.1038/s42255-026-01476-1
Nyckelord: fettlever, levermetabolism, mitokondrier, lipiddroppar, perilipin 5