Clear Sky Science · sv
Matningsreglerad glykogenmetabolism driver rytmisk leverproteinsekretion
Varför leverns dagliga rytm är viktig
De flesta av oss tänker på vad vi äter, men inte på när vår lever tyst paketerar och skickar ut livsviktiga proteiner i blodomloppet. Denna studie visar att leverns ”fraktschema” för proteiner långt ifrån är konstant: det följer en daglig rytm som starkt beror på när vi äter och på hur levern använder lagrat socker, så kallat glykogen. Att förstå detta tidshållningssystem hjälper till att förklara varför måltidstiming, fetma och vissa sällsynta genetiska sjukdomar kan rubba hormoner, koagulationsfaktorer och många andra blodproteiner som håller kroppen i balans.
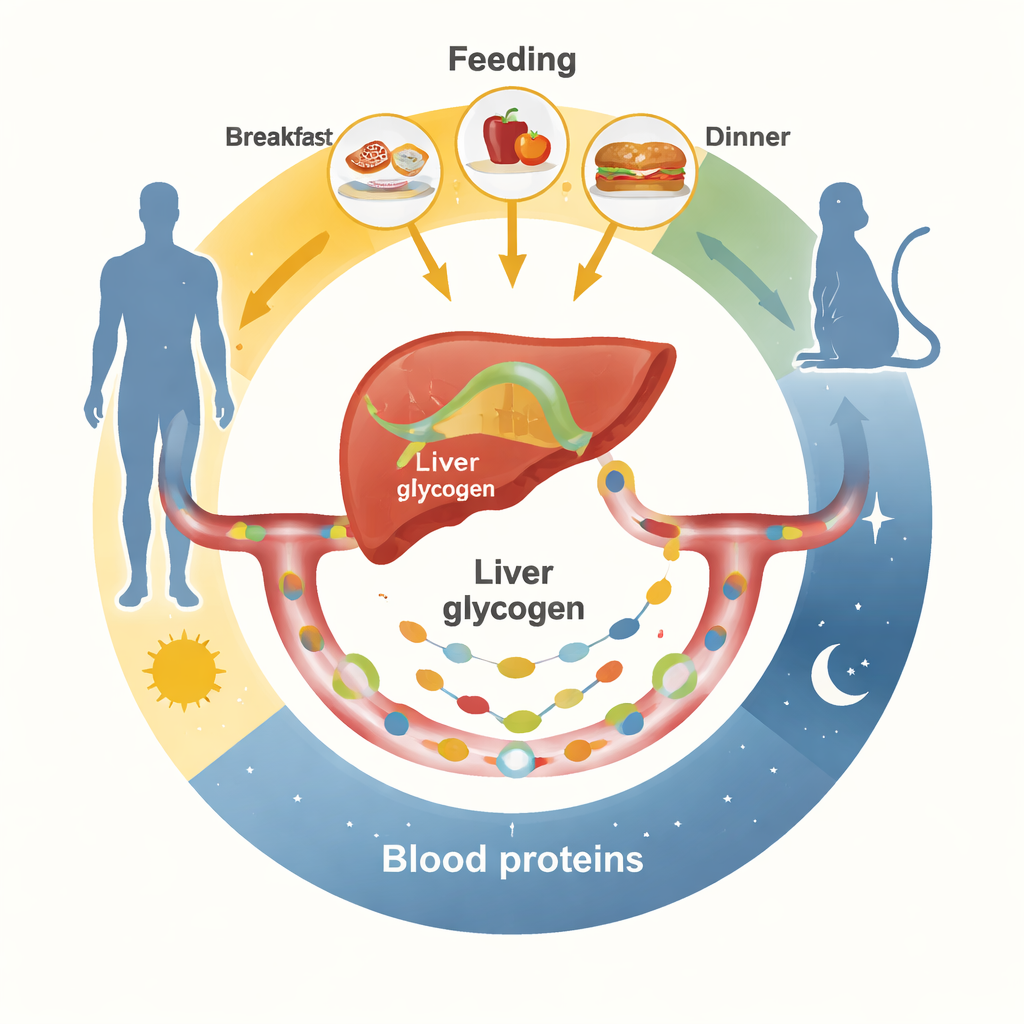
Måltider sätter takten för blodproteiner
Forskarna följde först hundratals blodproteiner över 24 timmar hos friska män under två kontrollerade ätmönster. I det ena åt försökspersonerna regelbundna måltider; i det andra fördelades samma totala kaloriintag jämnt över vakna timmar. Vid regelbundna måltider steg och föll många blodproteiner i tydliga dagliga vågor, ofta med toppar tidigt på morgonen och sent på eftermiddagen. Dessa inkluderade metabola hormoner, koagulationsfaktorer, immunsystemets proteiner och transportproteiner som till stor del tillverkas i levern. När maten istället sippades långsamt och kontinuerligt jämnades de flesta av dessa rytmer ut. Liknande experiment i möss, där mat fanns antingen hela tiden eller endast under bestämda dag- eller nattfönster, visade att ändrade matningsscheman kraftigt omformade vilka proteiner i blodet som var rytmiska och när de nådde toppar.
Levern hemliga sekretionslinje drivs av en klocka
För att ta reda på hur dessa mönster uppstår tittade teamet inuti levern. De fann att de proteiner som deltar i den klassiska ”sekretoriska vägen” — där nybildade proteiner går in i det endoplasmatiska retiklet (ER), modifieras i Golgiapparaten och sedan släpps ut — också steg och föll över dagen. I stället för att vara ett konstant transportband är denna väg inställd efter tid på dygnet. De flesta rytmiska blodproteiner bar de molekylära ”signalsekvenser” som markerar dem för denna väg, och att blockera ER–Golgi-transport i museleverbitar minskade proteinfrisättningen kraftigt. Däremot visade markörer för cellskada och proteinnedbrytning inte starka dagliga förändringar, vilket indikerar att det är sekretion, inte nedbrytning, som i första hand driver de observerade blodrytmerna.
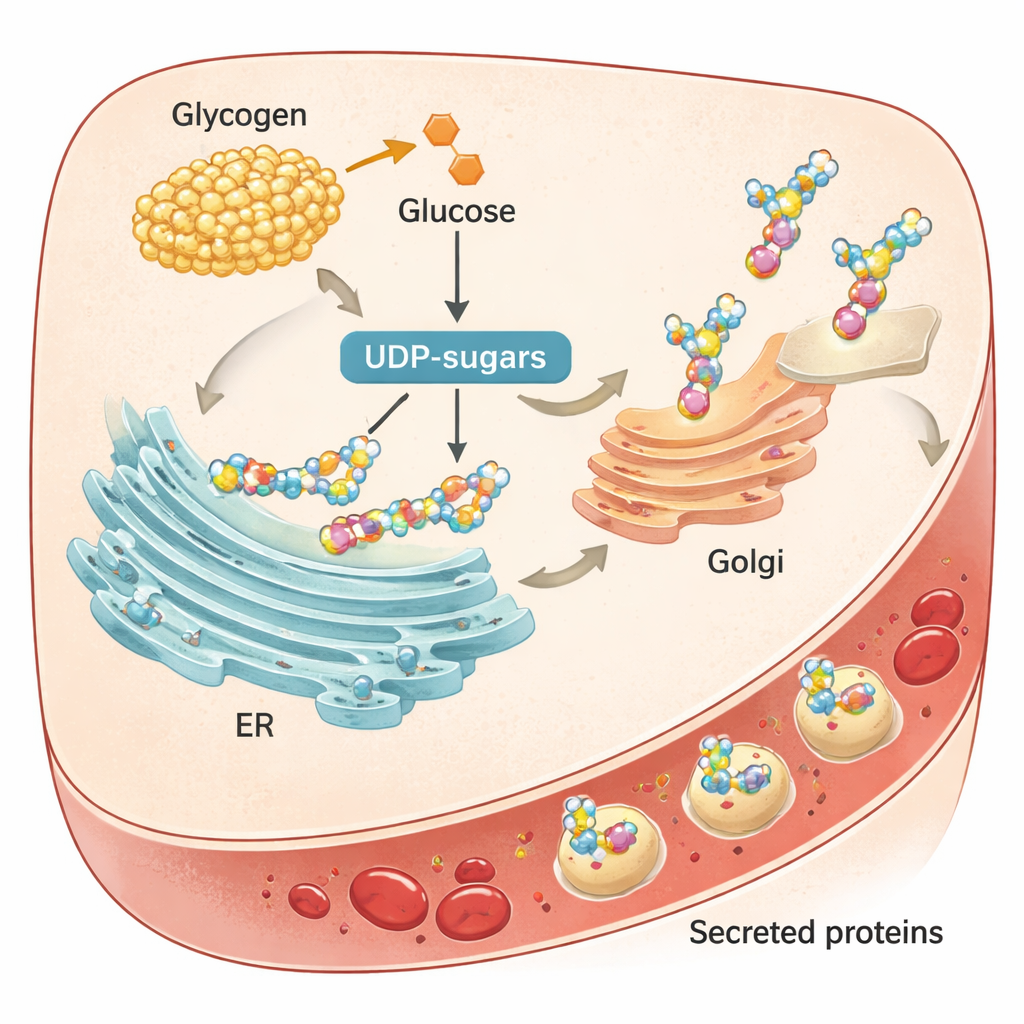
Glykogen: lagrat socker som driver proteinpackning
Författarna kopplade sedan dessa tids effekter till hur levern hanterar glykogen, dess huvudsakliga kolhydratlager. Efter måltider bygger levern upp glykogen; under fasta bryts glykogen ner, en process som kallas glykogenolys. Nedbrytningsprodukterna förs in i ”UDP-socker”, de aktiverade sockerenheter som används för att låta proteiner få sockerkedjor, en modifiering som kallas glykosylering. Hos möss oscillerade nivåerna av UDP-socker starkt över dygnet, i takt med aktiviteten hos enzymer som bygger upp och bryter ner glykogen. När teamet blockerade det centrala leverenzymet för glykogenolys, PYGL, med ett läkemedel, samlades glykogen upp, blodsockret sjönk under fasta och tillgången på UDP-socker föll. Detta ledde till mindre glykosylering av leverproteiner, tecken på stress i ER och minskad utsöndring av flera viktiga proteiner till blodet.
Stressignaler och kopplingar till sjukdom
Att störa glykogennedbrytning gjorde mer än att bara sakta ner proteinexporten; det utlöste cellens kvalitetssäkringslarm. Leverceller som behandlats med det PYGL-blockerande läkemedlet aktiverade den ofoltade proteinresponsen, en serie ER-stressvägar som kan öka proteinnedbrytning och selektivt förändra vilka proteiner som sekretorieras. I feta möss, som naturligtvis har förändrad glykogenhantering, dämpades de normala dagliga svängningarna i glykogen och antalet rytmiska blodproteiner minskade. Detsamma gällde när normala möss utsattes för tidsbegränsad matning som effektivt minskade kalorierna. Slutligen visade en stor genetisk studie hos människor att personer som bär varianter i gener kopplade till glykogenlagringssjukdomar eller kongenitala glykosyleringsrubbningar hade förändrade nivåer av många blodproteiner, vilket förstärker länken mellan glykogenmetabolism, proteinglykosylering och sekretion.
Vad detta betyder för vardaglig hälsa
För den icke-experten är budskapet att levern driver en tidsstyrd exportverksamhet för blodproteiner och använder lagrat socker som bränsle för att möjliggöra korrekt paketering och utsläpp. När ätmönster, interna klockor eller glykogenbearbetande gener störs, sviktar detta schema och förändrar nivåerna av hormoner, koagulationsfaktorer och immunsystemets proteiner i blodomloppet. Dessa förändringar kan bidra till att förklara varför måltidstiming, fetma och vissa sällsynta metabola tillstånd är kopplade till vittomspännande hälsoproblem. Arbetet antyder att inte bara vad vi äter, utan också när vi äter, kan påverka leverns dagliga fraktrytm — och att läkare kan behöva ta hänsyn till tid på dygnet och ätmönster när de tolkar blodprov.
Citering: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
Nyckelord: dygnsrytm, leverglykogen, proteinsekretion, måltidstiming, metabolism