Clear Sky Science · sv
Lamin A/C‑reglerad cystein‑katabol flux styr stamcellsöde genom epigenomomprogrammering
Hur cellens skelett pratar med dess metabolism
Varför förblir vissa celler ungdomliga och flexibla i vad de kan bli, medan andra åldras eller låser sig i fel identitet? Denna studie avslöjar en överraskande kommunikation inne i våra celler mellan den nukleära ”stommen” som formar DNA och en svavelhaltig näringsämne, cystein. Genom att visa hur denna dialog styr stamceller mot hälsosamma öden — eller mot för tidigt åldrande — antyder arbetet att vad celler ”äter” och hur de bearbetar det en dag skulle kunna justeras för att förebygga vissa genetiska sjukdomar och kanske även sakta vissa aspekter av åldrandet.
Den dolda rollen hos den nukleära skalet
Långt inne i varje cell ligger DNA pressat mot ett proteinnät kallat den nukleära lamina, delvis uppbyggt av proteiner som lamin A och C. Dessa lamininer ger inte bara kärnan dess form; de hjälper också till att avgöra vilka gener som är låsta och vilka som förblir åtkomliga. Författarna studerade musembryonala stamceller i deras mest flexibla, eller ”naiva”, tillstånd och fann att lamin A/C normalt håller tillbaka två metabola enzymer, CBS och CTH, som hjälper till att bygga upp och bryta ner cystein. När lamin A/C är närvarande och aktiv hålls dessa enzymer tillbaka och cysteinhanteringen förblir låg, vilket stödjer ett stabilt, ungdomligt stamcellstillstånd. 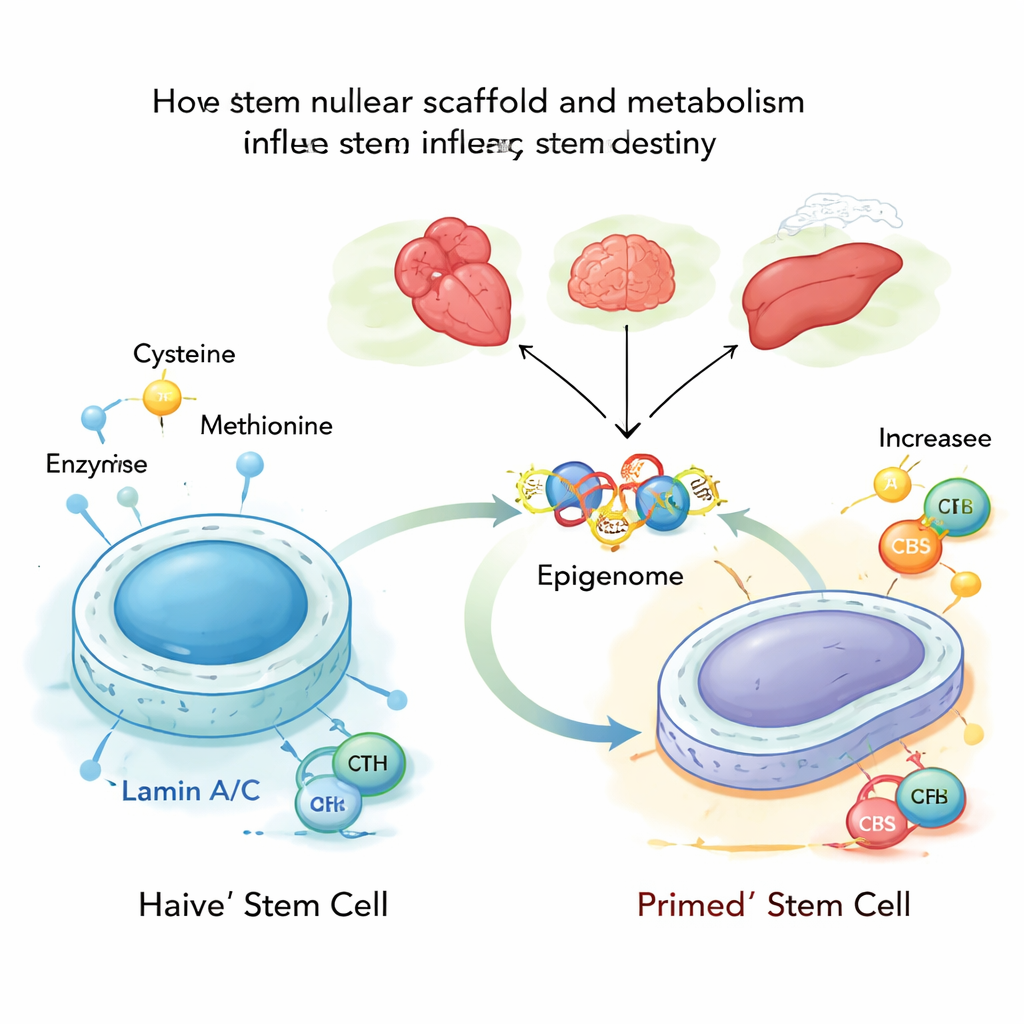
När strukturen sviktar ökar metabolismen
Nästa steg var att forskarna tog bort lamin A/C eller införde en sjukdomsassocierad mutation som efterliknar en mänsklig för tidig‑åldrandesjukdom kallad Hutchinson–Gilford progeria. Utan normalt lamin A/C blir CBS‑ och CTH‑generna mer åtkomliga och mer starkt bundna av en transkriptionsfaktor kallad SP1, vilket slår på dem. Den förändringen skjuter mer cystein genom en metabol väg som slutar i acetyl‑CoA, en liten molekyl som bär acetylgrupper som används för att lossa DNA‑packningen. När cystein i ökande grad kanaliseras in i acetyl‑CoA läggs acetylgrupperna i första hand till specifika platser på histonproteiner — särskilt två positioner på histon H3 kända som K9 och K27 — vilket gör att närliggande gener blir lättare att aktivera.
Från kemiska märken till beslut om cellöde
Dessa skift i histonens ”märken” fungerar som en global omstämning av cellens kontrollpanel. I naiva stamceller driver ökad aktivitet av CBS och CTH, eller helt enkelt tillförseln av mer cystein, cellerna mot ett mer avancerat, ”primat” tillstånd som ligger närmare att bilda verklig vävnad. Gener involverade i hjärtutveckling och andra linjer blir mer aktiva, och DNA:s tredimensionella veckning förändras för att gynna dessa program. Omvänt hjälper nedreglering av CBS och CTH eller begränsning av cystein till att återställa en mer naiv, ungdomlig identitet även när den nukleära lamina är skadad. I embryonala modeller ledde denna metabola felkoppling till snedvriden bildning av de tre groddbladen — de tidiga byggstenarna för alla organ — och en onormal förskjutning mot hjärtmuskelceller om inte CBS och CTH balanserades om. 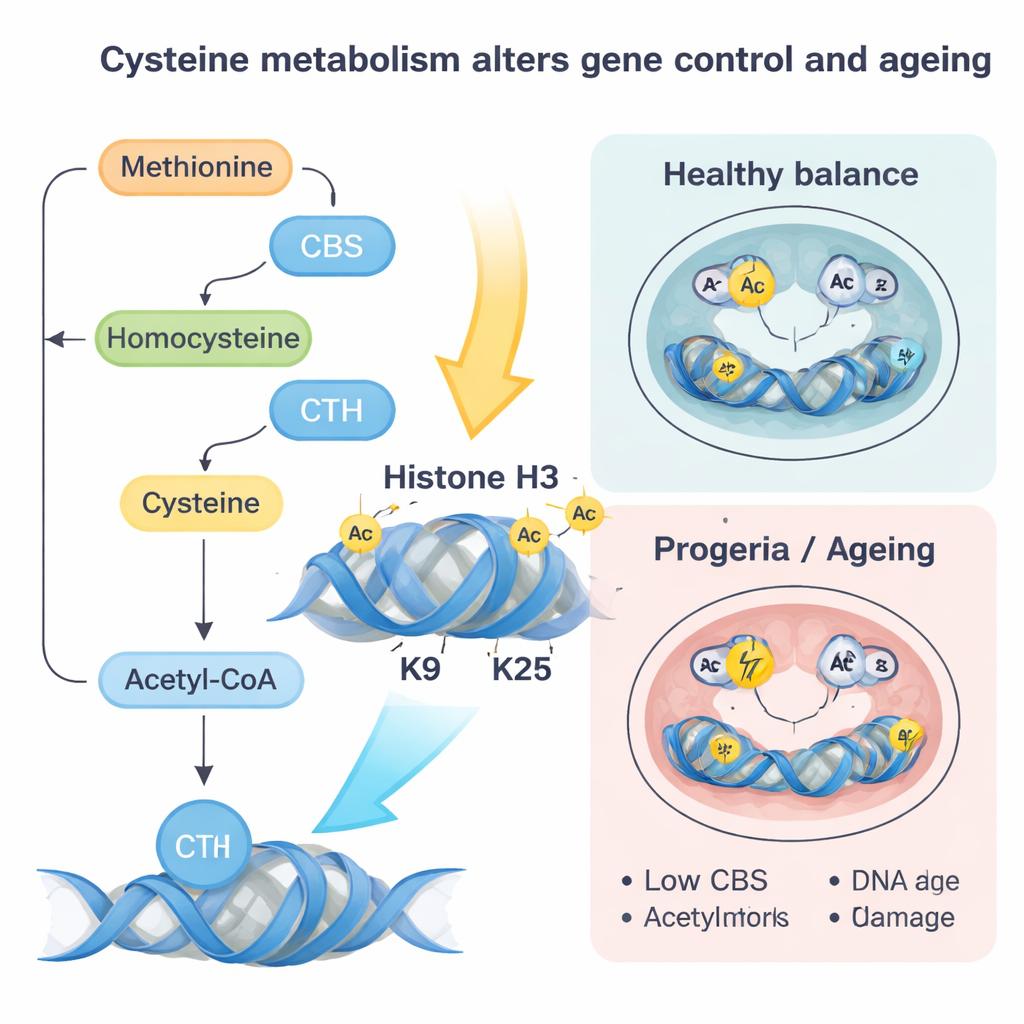
Metabolism, DNA‑märken och för tidigt åldrande
Den progeria‑lika laminmutationen berättade en kompletterande historia. Här sjunker nivåerna av CBS och CTH, vilket minskar cysteinflödet och acetyl‑CoA från denna väg. Samtidigt skjuts homocystein tillbaka in i metionincykeln, vilket ökar nivåerna av SAM, den universella donatorn av metylgrupper. Det gynnar extra metylmärken, särskilt ett märke kallat H3K9me3 som sätts dit av enzymet SUV39H1, vilket tätar kromatin och är kopplat till försämrad DNA‑reparation. Författarna visade att en försiktig återställning av CBS eller begränsning av metionin sänkte SAM, minskade dessa repressiva metylmärken, förbättrade DNA‑reparation, minskade oxidativ stress och senescensmarkörer samt delvis räddade differentieringen till hjärtceller. Liknande minskningar av CBS och ökningar i repressiva märken observerades i normala åldrande mus‑hjärtan och i humana fibroblaster från äldre personer och progeripatienter, vilket tyder på att denna krets också fungerar vid naturligt åldrande.
Vad detta betyder för hälsa och åldrande
För en icke‑specialist är budskapet att cellens strukturella ramverk och dess metabolism är tätt kopplade: när det nukleära skalet av lamin A/C störs ändras hur cystein används, vilket i sin tur omskriver kemiska märken på DNA‑paketerande proteiner. Dessa märken avgör vilka gener som slås på när stamceller bygger kroppen och hjälper till att bestämma hur väl celler reparerar skador över en livstid. Genom att noggrant justera enzymer som CBS och CTH — eller genom att reglera tillgången på näringsämnen som metionin och cystein — kan det vara möjligt att korrigera viss felaktig märkning i lamin‑baserade sjukdomar och kanske mildra aspekter av för tidigt eller normalt åldrande.
Citering: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Nyckelord: stamceller, nukleär lamina, cysteinmetabolism, epigenetik, åldrandе