Clear Sky Science · sv
ABEL‑FRET överbryggar tidsskalan i enkelmolekylmätningar av strukturdynamiken hos A2A‑adenosinreceptorn
Att följa små cellulära strömbrytare i realtid
Många av dagens läkemedel verkar genom att slå om molekylära ”strömbrytare” på cellens yta, så kallade receptorer. Dessa strömbrytare ändrar ständigt form när de slår på och av signaler, men de flesta verktyg kan bara se de allra snabbaste eller de allra långsammaste rörelserna — inte båda. Denna artikel presenterar ett sätt att i lösning följa en enskild, läkemedelsmålande receptor mycket längre än tidigare, vilket avslöjar hur den dröjer kvar i särskilda former som är avgörande för läkemedelseffekter.
Varför dessa formskiftande proteiner är viktiga
Studien fokuserar på en stor klass av cellmembranproteiner som kallas G‑protein‑kopplade receptorer, eller GPCR:er. Dessa proteiner styr viktiga processer som syn, stämningsläge, blodtryck och immunsvar, och mer än en tredjedel av godkända läkemedel verkar på dem. En välstuderad medlem, A2A‑adenosinreceptorn, hjälper till att reglera sömn, smärta, inflammation och hjärnsignalering, och är ett lovande mål för behandling av sjukdomar som Parkinson och cancer. GPCR:er är mycket flexibla: när olika molekyler binder trycks receptorn in i distinkta former som gynnar vissa signalvägar framför andra. Just den flexibiliteten gör det svårt att designa läkemedel utifrån statiska ögonblicksbilder från röntgen eller kryoelektronmikroskopi.
Följa en enskild receptor utan att fästa den
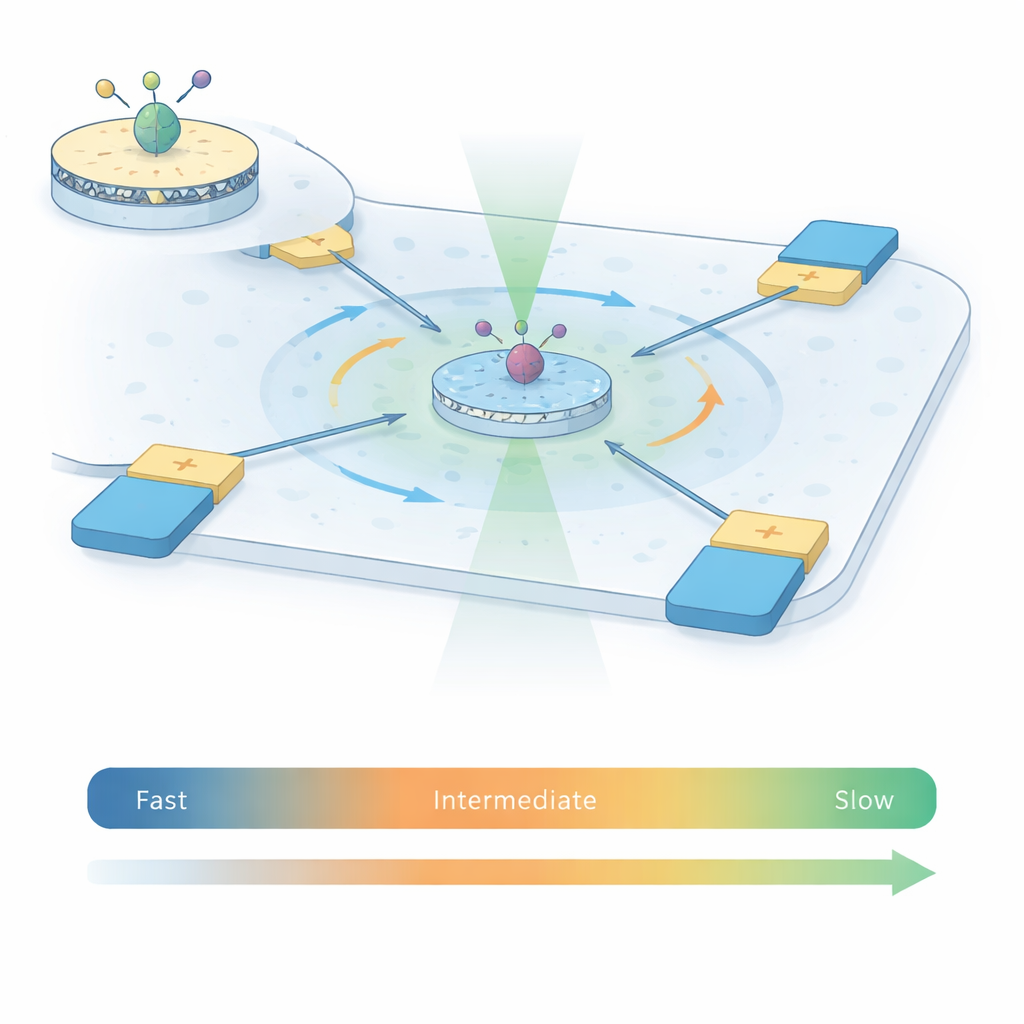
För att fånga hur A2A‑receptorer rör sig kombinerar författarna två kraftfulla tekniker till det de kallar ABEL‑FRET. Först rekonstituerar de enskilda receptorer i små fragment av artificiellt membran kallade nanodiskar, vilket ger varje protein en mer naturlig omgivning än enbart detergent. De fäster ett par fluorescerande färgämnen på två rörliga delar inne i receptorn. När receptorn ändrar form förändras avståndet och den relativa orienteringen mellan dessa färgämnen, vilket påverkar energitransfer mellan dem — ett fenomen känt som Förster‑resonansenergitransfer (FRET). För det andra, istället för att fästa receptorn på en yta använder de en Anti‑Brownsk Elektrokinetisk (ABEL) fälla: en mikrofluidisk kammare med elektroder som känner av var en fluorescerande partikel befinner sig och varsamt pressar tillbaka den mot centrum, för att motverka slumpmässig Brownsk rörelse.
Överbrygga det saknade tidsfönstret
Traditionella enkelmolekyl‑FRET‑experiment antingen observerar fritt diffunderande receptorer bara i några tusendels sekund, eller immobiliserade receptorer på en yta i sekunder till minuter. Varje metod täcker ett annat tidsfönster. Med hjälp av ABEL‑fällan håller detta arbete enskilda A2A‑receptorer i sikte i en till två sekunder medan de förblir fria i lösning — ungefär 100 gånger längre än i diffusionbegränsade experiment. Denna förlängda observationstid gör det möjligt för teamet att mäta hur FRET‑signalen fluktuerar inom varje infångat burst och över tusentals receptorer, under fyra förhållanden: utan ligand, med en antagonist, och med två olika aktiverande molekyler (agonister). Statistiska verktyg lånade från signalanalys — varians, korrelation och återkomstanalys — låter dem skilja slumpmässigt fotonbrus från verkliga, långsamma strukturella förändringar i receptorn.
Dolda långlivade former avslöjade
FRET‑avläsningarna visar att receptorer uppehåller flera distinkta konformationer som inte fullt ut växlar mellan varandra under typiska observationstider på några hundra millisekunder. I alla förhållanden är spridningen av FRET‑värden mycket bredare än vad som kan förklaras av enbart brus, vilket avslöjar strukturell heterogenitet: olika molekyler sitter i olika långlivade former. När aktiverande molekyler binder förskjuts det genomsnittliga FRET‑nivån uppåt, vilket indikerar att receptorn tillbringar mer tid i en ”aktivlik” arrangement av sina inre helixar. Ändå visar korrelationsanalyserna att när en receptor väl är i ett högt eller intermediärt FRET‑tillstånd finns en stark sannolikhet att den stannar där i åtminstone hundratals millisekunder. Dessa resultat uppdaterar tidigare uppskattningar baserade på snabbare experiment och förlänger karakteristiska ”uppehållstider” i långlivade tillstånd från bara millisekunder till långt över en tiondels sekund.
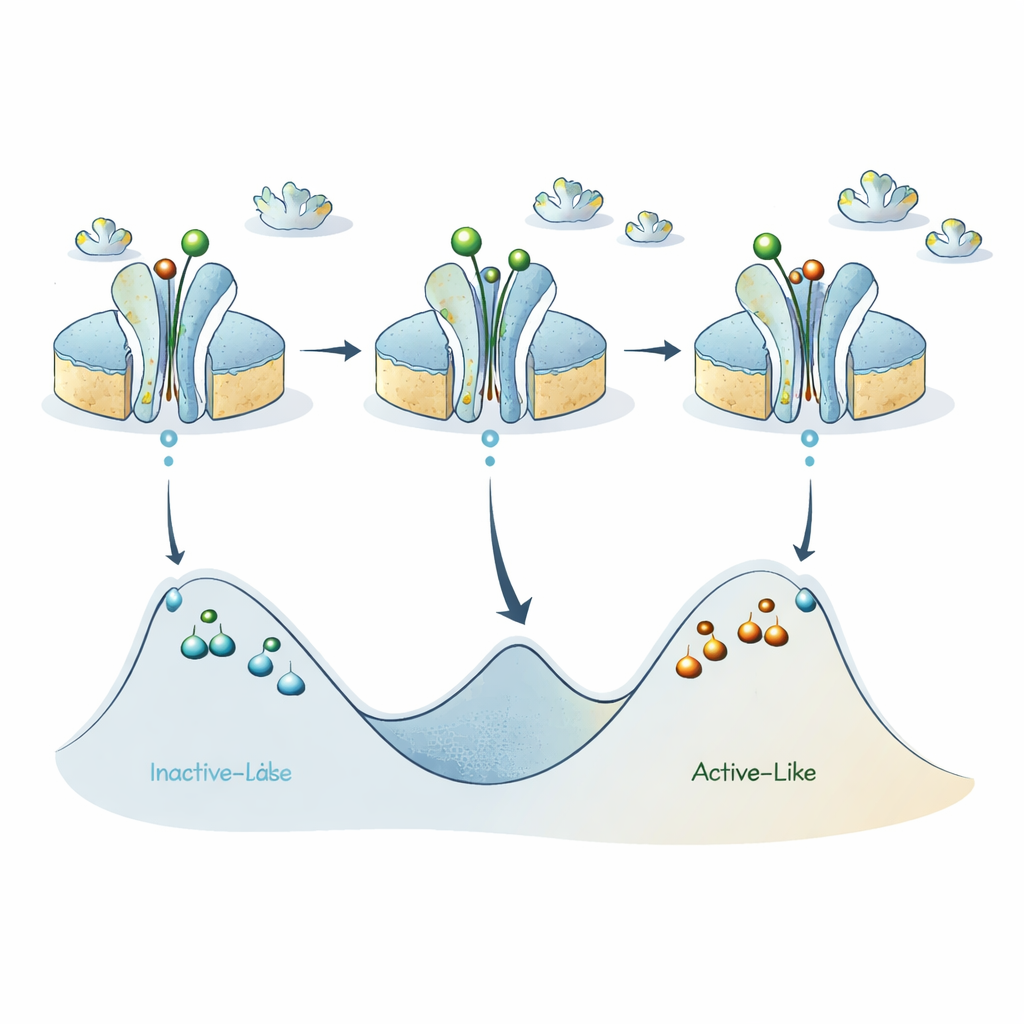
En ny karta över receptorernas energilandskap
Sammantaget förfinar författarna en tidigare modell där A2A‑receptorn växlar huvudsakligen mellan ett inaktivlikt tillstånd och ett aktivlikt tillstånd. Deras nya data tyder på att vardera av dessa två breda kategorier egentligen döljer flera del‑tillstånd separerade av betydande energibarriärer, så att enskilda receptorer kan förbli ”fastnade” i en given version av aktivlikt eller inaktivlikt under förvånansvärt långa tider. Aktiverande ligander sänker barriären mellan huvudbassängerna för inaktivt och aktivt, vilket främjar snabb växling på submillisekundskala, men de interna barriärerna inom varje bassäng förblir höga och ger upphov till de långlivade del‑tillstånden som ABEL‑FRET upptäcker.
Vad detta betyder för framtida läkemedel
För icke‑specialister är huvudbudskapet att ett läkemedelsmål som A2A‑receptorn inte enkelt växlar mellan ”av” och ”på”. I stället utforskar det ett skrovligt landskap av former, varav några består tillräckligt länge för att påverka hur signaler överförs inne i cellerna och hur läkemedel verkar över tid. Genom att förlänga hur länge enskilda receptorer kan observeras i sitt naturliga, ofästa tillstånd fyller ABEL‑FRET en avgörande lucka mellan ultrarapida och mycket långsamma mätningar. Denna metod kan nu tillämpas på många membranproteiner och erbjuder en mer heltäckande, tidsupplöst bild av hur potentiella läkemedelsmål andas, skiftar form och svarar på terapeutiska föreningar.
Citering: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Nyckelord: G‑protein‑kopplade receptorer, enkelmolekyl‑FRET, adenosin A2A‑receptor, proteiners konformationsdynamik, ABEL‑fälla