Clear Sky Science · sv
Mekanistisk studie av sulfatmigration i glykosaminoglykaner under MS-fragmentering
Varför förflyttning av kemiska markörer på socker spelar roll
Våra celler är täckta av långa sockerkedjor som hjälper till att styra processer så skilda som blodkoagulering, immunförsvar och hur virus fäster vid celler. Många av dessa kedjor bär små kemiska markörer kallade sulfatgrupper vars exakta positioner längs sockerstommen fungerar som en molekylär streckkod och talar om för proteiner när och var de ska binda. Forskare förlitar sig i hög grad på masspektrometri, en kraftfull vägningsteknik, för att läsa dessa streckkoder. Denna studie visar att sulfatmarkörer under sådana mätningar tyst kan förflytta sig, vilket potentiellt kan vilseleda forskare om hur dessa biologiskt viktiga socker faktiskt är uppbyggda.
Komplexa sockerkedjor med kritiska markörer
Glykosaminoglykaner är långa, linjära sockerkedjor som ofta är bundna till proteiner på cellytor. Deras sulfatdekorationer är inte slumpmässiga; små förändringar i var en sulfatgrupp sitter på en viss sockerenhet kan radikalt förändra hur kedjan interagerar med tillväxtfaktorer, koagulationsproteiner eller patogener. På grund av detta försöker forskare avgöra inte bara hur många sulfater som finns utan exakt var de är placerade. Masspektrometri, ofta i kombination med kontrollerad nedbrytning av sockerkedjorna, är en av huvudmetoderna för detta. Tidigare indikationer antydde dock att laddade grupper som sulfater kan flytta runt under mätningen, vilket komplicerar försök att läsa ut det verkliga modifieringsmönstret.
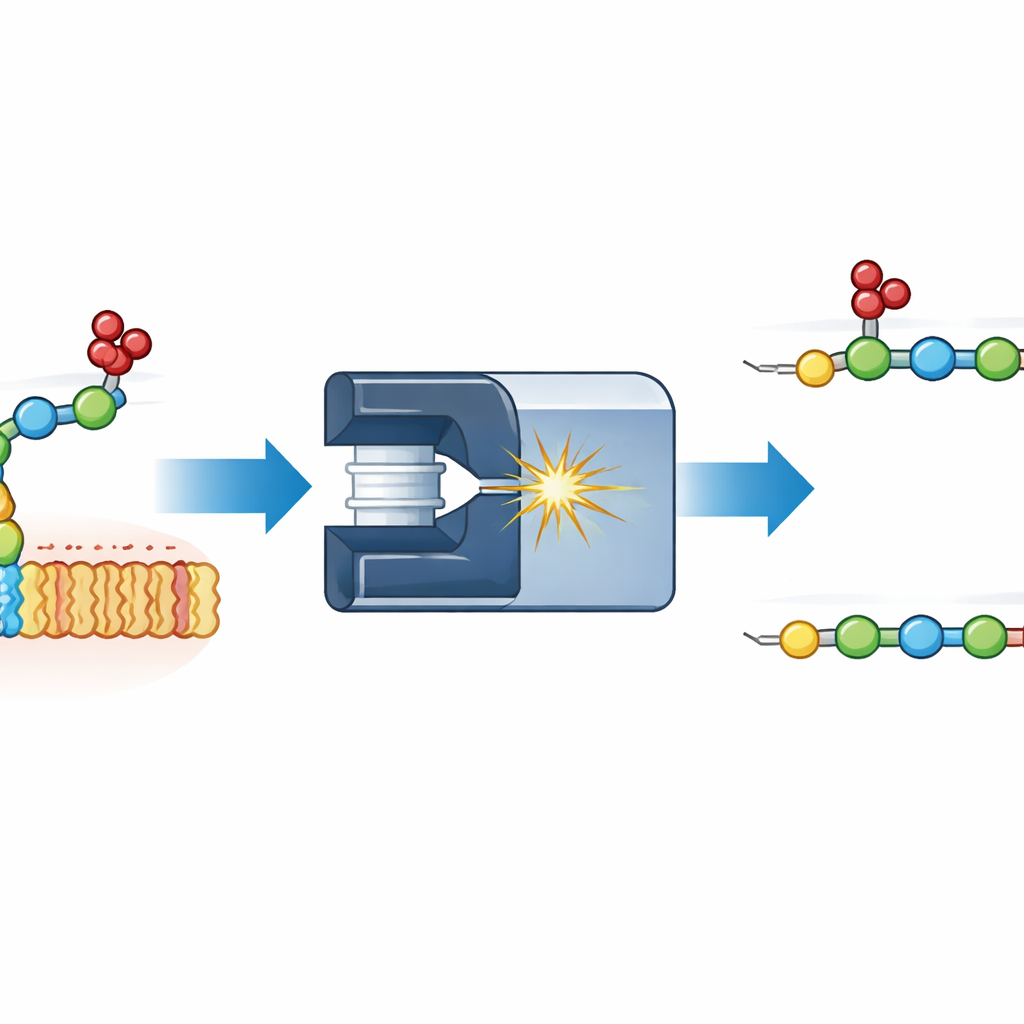
Att iaktta sulfater som rör sig under mätningen
Författarna fokuserade på en enkel modell: en tvåsockerenhet från heparansulfat, en av de mest välkända glykosaminoglykanerna. De fäste olika fluorescerande märken i ena änden av disackariden och fragmenterade den inne i en masspektrometer. Genom att mäta hur de resulterande bitarna dröjde sig genom en gas under ett elektriskt fält — en teknik kallad jonmobilitet — kunde de skilja former som annars har samma massa. Ett oväntat fragment dök upp som var tyngre med exakt en sulfatgrupp på fel plats: istället för att stanna på det första sockret hade sulfaten migrerat till det andra. Jämförelser med noggrant syntetiserade referensföreningar visade att den migrerande sulfaten kunde hamna på två distinkta positioner på det andra sockret, vilket gav två olika former som tydligt kunde separeras med jonmobilitet.
För att peka ut nya landningsplatser och testa märken
För att bättre förstå var sulfaten landade och om andra positioner var möjliga, kombinerade teamet sina mätningar med detaljerade datorbaserade simuleringar. De beräknade många möjliga tredimensionella former för kandidatstrukturerna och förutsade hur var och en skulle förflytta sig genom gasfasen. Endast sulfater placerade vid två specifika ställen på det andra sockret — kända för specialister som 6O- och 3O-positionerna — stämde överens med det experimentella beteendet, medan andra hypotetiska lägen verkade osannolika. Forskarna testade sedan om de fästa märkena i sig kunde driva omflyttningen genom att byta ut det ursprungliga märket mot tre enklare sådana. I samtliga fall kvarstod sulfatmigrationen och gav liknande typer av fragment, vilket visar att valet av märke har liten effekt på om migration sker, även om det kan påverka hur lätt de olika produkterna kan särskiljas.
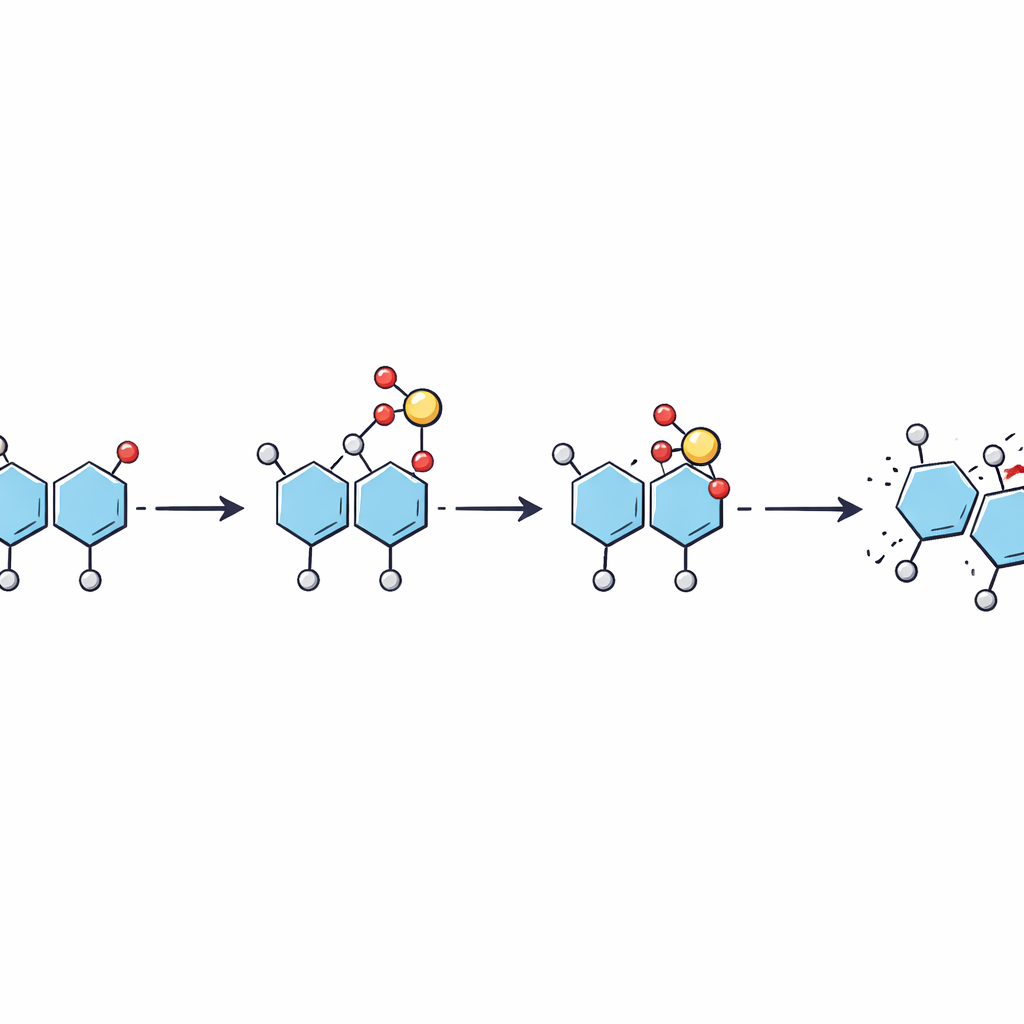
Stegvis hoppande istället för ett enda språng
Med hjälp av energijusterade fragmenteringsexperiment tillsammans med ytterligare simuleringar sammanställde författarna en steg-för-steg-bild av hur sulfaten rör sig. När jonen energiseras i masspektrometern aktiverar en mobil proton först sulfatgruppen, som sedan hoppar från originalsockret till en viss plats på det närliggande sockret i samband med att bindningen mellan dem bryts. Detta producerar ett fragment där sulfaten sitter i en intermediär position. Med ytterligare energi kan sulfaten skifta igen längs samma socker till en mer stabil plats. Arbetet tyder på att dessa omarrangemang kan ske vid lägre energier än de som krävs för att bryta sockerstommen, vilket innebär att de kan inträffa tyst i bakgrunden vid rutinanalyser.
Vad detta betyder för avkodning av sockerstrukturer
För icke-specialister är huvudbudskapet att de kemiska märkena på viktiga biologiska socker inte alltid är frusna i sina positioner under analys; de kan glida längs kedjan medan molekylen färdas genom masspektrometern. Studien visar i detalj att åtminstone för en representativ heparansulfatfraktion kan en sulfatgrupp migrera från en sockerenhet till en annan och sedan slå sig ner på nya positioner, vilket ger vilseledande fragment som efterliknar genuina strukturella egenskaper. Det betyder att vissa tidigare och framtida mätningar kan misstolka sulfatkoden om inte kompletterande tekniker—såsom jonmobilitet och avancerad modellering—används för att fånga dessa dolda rörelser. Arbetet efterlyser mer systematiska studier för att ta reda på hur utbredd sådan sulfatmigration är, så att forskare kan koppla mönster på cellytors socker mer tillförlitligt till hälsa och sjukdom.
Citering: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Nyckelord: heparansulfat, glykosaminoglykaner, masspektrometri, sulfatmigration, jonmobilitet