Clear Sky Science · sv
Bindningspositionens djup påverkar fotoomkopplande liganders effektivitet vid 5-HT2A-receptorn
Lys över omkopplbara hjärnläkemedel
Föreställ dig ett läkemedel du kan slå på och av med ett ljusblixt, som exakt styr hjärnans receptorer samtidigt som biverkningar undviks. Denna studie undersöker precis den idén för en central serotoninreceptor kopplad till stämning, perception och psykedelia. Forskarna grävde i varför två nästan identiska ljuskänsliga molekyler beter sig så olika—en agerar nästan som en perfekt av/på-brytare, den andra vägrar envist att stänga av helt. Svaret handlar om en överraskande enkel faktor: hur djupt molekylen sitter inne i receptorn.
Ljusstyrda läkemedel i hjärnan
Ljusstyrda läkemedel, även kallade fotofarmakologiska verktyg, är utformade så att en ljusstråle vrider en del av molekylen mellan två former, som en böjd och en rak version. Dessa former kan ändra hur hårt läkemedlet binder sitt mål. I det här arbetet är målet den mänskliga 5-HT2A-receptorn, ett protein på hjärnceller som svarar på serotonin och är centralt för både antipsykotiska och psykedeliarelaterade effekter. De studerade molekylerna är derivat av N,N-dimetyltryptamin (DMT), modifierade med en ljuskänslig azobenzen-enhet. Två varianter skiljer sig endast i var en liten metoxigrupp sitter på en ring—antingen i en "para"- eller "meta"-position—ändå är deras biologiska beteende under ljus dramatiskt olika.
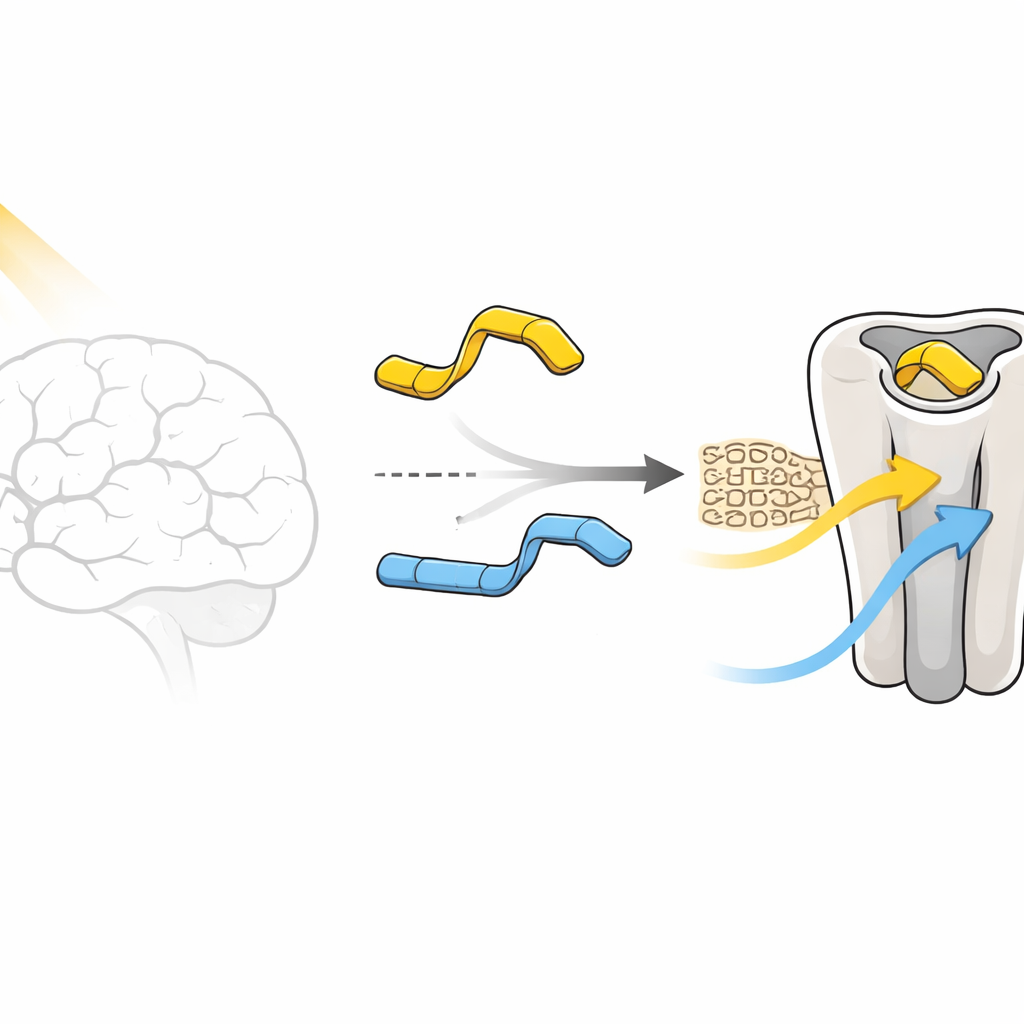
Två nästan identiska molekyler, mycket olika brytare
I celltester beter sig para-varianten, kallad förening 1, nästan som en digital omkopplare. I mörker aktiverar dess "trans"-form knappt receptorn och blockerar den till och med något, vilket liknar en svag antagonism. När ljus omvandlar den till "cis"-formen blir samma molekyl en måttlig aktivator och slår delvis på receptorn. Meta-varianten, förening 2, vägrar samarbeta på detta sätt: både dess ljus- och mörkerformer håller receptorn relativt aktiv, utan att någonsin leverera ett verkligt "av"-tillstånd. Pusslet i den här artikeln är varför en så minimal kemisk förändring—att bara flytta en liten grupp runt en ring—ändrar hur receptorn svarar så starkt.
Insyn med atomnivåfilmer
För att lösa detta använde teamet omfattande all-atom molekylär dynamik-simuleringar, vilket effektivt kör detaljerade filmer av varje atom i receptorn, det omgivande membranet, vatten och varje ligand över totalt cirka 80 mikrosekunder. De simulerade båda molekylerna i respektive ljusstyrda former, och i både inaktiva och aktiva former av 5-HT2A-receptorn. Genom att följa kända strukturella "mikrobrytare" inuti proteinet—såsom en nyckel-tryptofan som vänder, en saltbrygga som bryts och rörelsen av natrium och vatten djupt i kärnan—kunde de avgöra när receptorn lutade mot ett av- eller på-tillstånd. De jämförde också hur nära de nya molekylerna efterliknade bindningsposturen hos LSD, en välstuderad partiell aktivator, genom överlappningen av deras ringsystem som riktmärke.
Djupet betyder mer än formen ensam
Huvudinsikten är att molekylernas effektivitet styrs främst av hur djupt de skjuter in i receptorernas bindningsficka. I den inaktiva receptorn gör para-föreningens trans-form en speciell uppsättning vätebindningar som drar den ovanligt djupt, nedanför det område där typiska aktiverande kontakter finns. Denna "överinsättning" hindrar den från att nå nyckelpolära restgrupper som hjälper till att slå på receptorn, så den stabiliserar av-läget. Meta-föreningens trans-form kan inte göra samma förankrande kontakter och ligger istället högre upp i en mer LSD-liknande position som är kompatibel med aktivering, vilket förklarar dess kvarvarande aktivitet. När ljuset vänder båda molekylerna till deras cis-former rör de sig generellt till grundare, mer aktivatorlika positioner. Ändå spelar geometrin fortfarande roll: i den aktiva receptorn kan cis-förening 2 glida djupare in i en hydrofob tunnel mellan två helixar och bilda en ihållande vätebindning som förstärker dess starka agonistbeteende, medan cis-förening 1 steriskt blockeras från att göra detta.
Finkontroll över internt vatten och joner
Simuleringarna visar också att bindningsdjup subtilt justerar en intern natriumficka och en vattenväg som är kända för att påverka receptoraktivering. Djup, stel bindning av para-föreningen i dess trans-form håller en natriumjon tätt inkapslad och området runt relativt torrt, egenskaper kopplade till ett av-läge. I kontrast tillåter den mer rörliga bindningen hos meta-föreningen eller cis-formerna att mer vatten tränger in och lossar natriumomgivningen, vilket förbereder receptorn för aktivering. En viktig aromatisk "toggle switch"-rest kan ändra orientering lättare när ligandernas bindning är flexibel och inte över-förankrad, vilket ytterligare skjuter receptorn mot ett på-liknande tillstånd, särskilt med cis-förening 2.
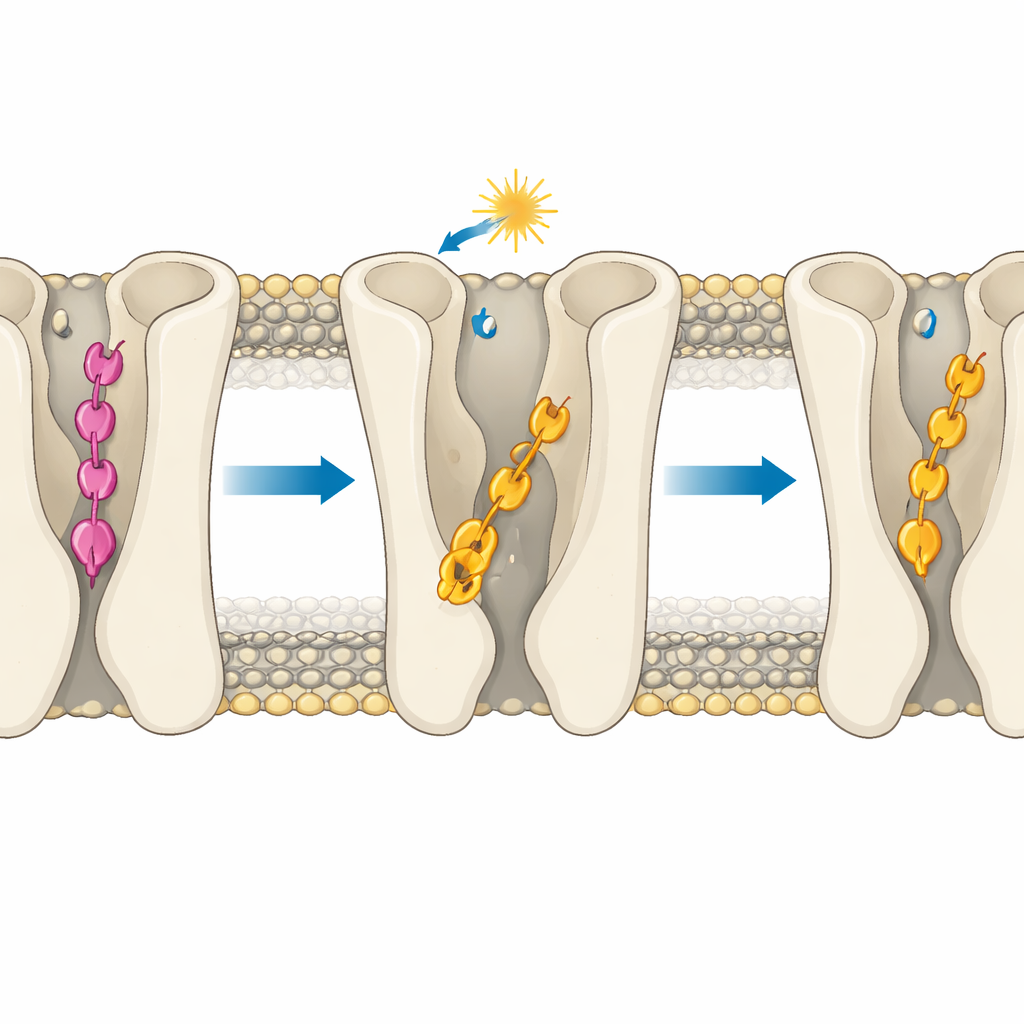
Designregler för framtida ljuskontrollerade läkemedel
För icke-specialisten är budskapet att den exakta djupet som ett läkemedel sitter i sin receptorficka kan göra skillnaden mellan av, delvis på och starkt på—även när den kemiska förändringen ser försumbar ut på papperet. Genom att visa hur en fotoswitchbar ligand kan överinsättas och låsa receptorn i av-läget, medan en nära besläktad ligand stannar på ett aktiveringsvänligt djup, erbjuder studien en tydlig designregel: kontrollera insättningsdjupet lika noggrant som du kontrollerar ljusstyrda formförändringar. Dessa insikter kan vägleda skapandet av nästa generation ljuskänsliga föreningar som behandlar hjärnsjukdomar med enastående precision, genom att höja eller sänka signalvägar på ett kontrollerat, reversibelt sätt samtidigt som biverkningar minimeras.
Citering: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Nyckelord: fotofarmakologi, serotonin 5-HT2A-receptor, fotoswitchbara ligander, GPCR-aktivering, molekylära dynamiksimuleringar