Clear Sky Science · sv
Scaffold-klientbeteende och strukturell organisation i flersammansatta proteinkondensat som avslöjas genom studier av tau/TDP-43-droppar
Proteiner som beter sig som små oljedroppar
Inne i våra celler förblir många proteiner inte jämnt blandade i den vattenrika inre miljön. Istället samlas de i små flytande droppar, ungefär som olja i vatten. Denna studie undersöker hur två sådana proteiner, tau och TDP-43 — som är starkt kopplade till Alzheimers sjukdom och andra demenser — samlas i droppar tillsammans. Genom att klarlägga hur dessa droppar bildas, blandas och organiseras ger arbetet ledtrådar till varför skadliga proteinaggregat uppträder i åldrande hjärnor och hur vi en dag kan kontrollera dem.
Varför dessa två hjärnproteiner är viktiga
Tau och TDP-43 är båda kända för att bilda giftiga aggregat vid neurodegenerativa sjukdomar. Traditionellt har forskare studerat dem var för sig, men obduktioner av mänskliga hjärnor visar i allt större utsträckning att båda proteinerna kan finnas i samma skadade områden. Det väcker en viktig fråga: när tau och TDP-43 förekommer tillsammans i celler, hur delar de utrymmet inne i dropparna, och uppmuntrar denna gemensamma miljö sjukdomsrelaterad aggregering? Författarna valde en förenklad men realistisk modell med tau och TDP-43:s lågkomplexa svans (LCD), den del som i hög grad ansvarar för droppbildning och slutlig försolidifiering.
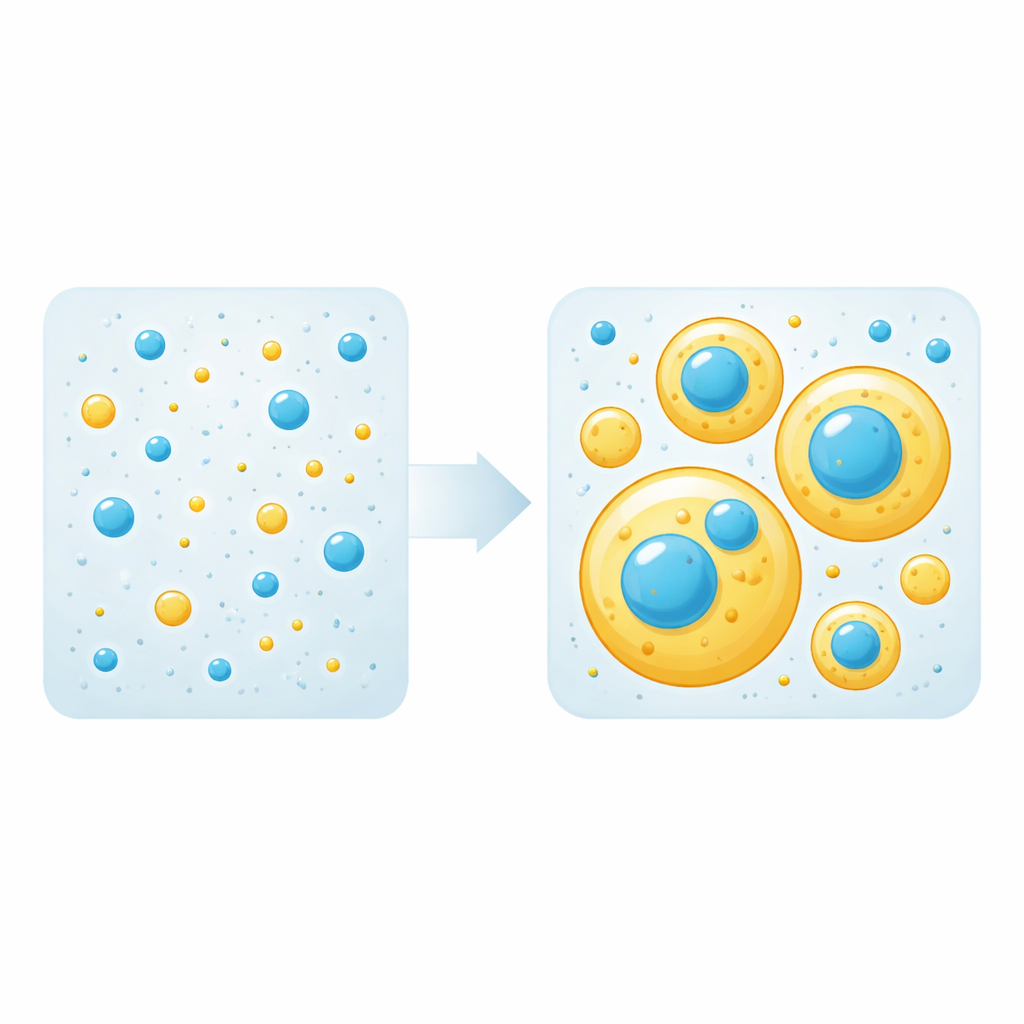
Droppar, “scaffolds” och “clients”
Flytande droppar som dessa bildas när protein–proteinattraktioner överstiger protein–vattenattraktioner, vilket får en lösning att dela sig i en tät fas (droppar) och en utspädd fas. I blandningar krävs bara vissa proteiner för att bygga droppar; dessa kallas “scaffolds” (stommar). Andra hakar bara på som “clients” (klienter). Teamet mätte först koncentrationströskeln vid vilken varje protein ensamt börjar bilda droppar. De blandade sedan olika mängder tau och TDP-43 LCD och observerade med fluorescensmikroskopi om droppar uppstod och hur proteinerna arrangerade sig. Slående nog fann de att antingen protein kan spela rollen som scaffold eller client enbart beroende på dess koncentration: över sin egen tröskel bygger det droppar, under den tröskeln rekryteras det passivt in i droppar som bildas av det andra proteinet.
Lagerbildade droppar och en mystisk gloria
När båda proteinerna fanns i tillräcklig mängd för att bilda droppar på egen hand blandades de inte till en enda homogen droppe. Istället omslöt större tau-rika droppar mindre TDP-43–rika droppar och skapade en lagerindelad, mångfasig struktur. Mätningar av hur dropparna sprider sig på glas visade att TDP-43-droppar har högre ytspänning, så det är energimässigt fördelaktigt för dem att sitta inuti de mer våtande tau-dropparna. Ett slående fenomen uppträdde vid dessa gränssnitt: tau ansamlades i särskilt höga nivåer som en ljus “gloria” som täckte ytan på TDP-43-dropparna, även när tau själv låg under sin egen droppbildande tröskel. Med tiden tenderade TDP-43–rika regioner att stelna till ett mer solidliknande material, medan tau-rika regioner förblev flytande, vilket tyder på olika benägenheter att övergå till långlivade aggregat.
Justera interaktioner och utforska den mikroskopiska mekanismen
Författarna testade därefter hur specifika molekylära krafter styr vilket protein som fungerar som scaffold eller client. De försvagade selektivt hydrofoba (vattenavstötande) interaktioner som driver TDP-43 LCD-kondensation med 1,6-hexandiol, och försvagade separat de elektrostatiska (laddningsbaserade) interaktioner som driver tau-kondensation genom att höja salthalten. I båda fallen förhindrade avstängning av ett proteins nyckelinteraktioner att det bildade droppar och förvandlade det till en client inuti det andra proteinets droppar, vilket efterliknar vad som händer när dess koncentration sänks. För att förstå glorian djupare varierade de salt för att se hur mycket tau som gick in i TDP-43-droppar och använde datorbaserade simuleringar som behandlar varje aminosyra som en förenklad pärla. Dessa simuleringar reproducerade glorian och visade att de första ~40 aminosyrorna i taus negativt laddade N-terminala region förankrar vid droppens yta, medan resten av molekylen sträcker sig ut i den omgivande vätskan och skapar ett ”amfifilt” (delvis droppvänligt, delvis vattenvänligt) skal. Experiment med ett förkortat tauförekomstfragment som saknade denna N-terminala sträcka bekräftade att utan den försvinner glorian.

Vad detta betyder för hjärnsjukdom
Tillsammans avslöjar resultaten en generell uppsättning regler för hur flersammansatta proteindroppar monteras och organiseras. I detta tau/TDP-43-system, som speglar situationer i sjuka neuroner, bestämmer koncentration och interaktionsstyrka tillsammans vilka proteiner som bygger droppar och vilka som enbart fyller dem. Ytspänning och amfifila arrangemang formar därefter lagerbildade droppar och gloriorsom kan koncentrera flera sjukdomsassocierade proteiner i samma avgränsade utrymme, vilket potentiellt uppmuntrar dem att hårdna till aggregat. För en allmän läsare är huvudbudskapet att tau och TDP-43 inte bara klumpas ihop slumpmässigt; de självor-ganiserar till strukturerade flytande droppar vars arkitektur styrs av enkla fysiska principer. Att förstå och slutligen kunna manipulera dessa principer kan öppna nya vägar för att bromsa eller förebygga skadlig proteinansamling vid neurodegenerativa sjukdomar.
Citering: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Nyckelord: proteinkondensat, vätske-vätske fasseparation, tau, TDP-43, neurodegeneration