Clear Sky Science · sv
Synergistiska kation‑yta‑effekter förbättrar alkaliska vätgasbildningskinetiker på trappstegsformade Pt‑ytor
Varför detta är viktigt för ren energi
Att producera ren vätgas från vatten är en nyckelkomponent i många netto‑noll energiplaner, men dagens mest praktiska enheter slösar energi eftersom reaktionen som bildar vätgasbubblor kan vara förvånansvärt långsam i alkaliska (basiska) lösningar. Denna studie granskar nivån av enskilda atomer och vattenmolekyler för att förklara varför vissa platinaytor fungerar bättre än andra, och hur vanliga lösta joner i vätskan kan samarbeta med metallytan för att påskynda vätgasproduktionen.
Formning av metallytor för att styra vatten
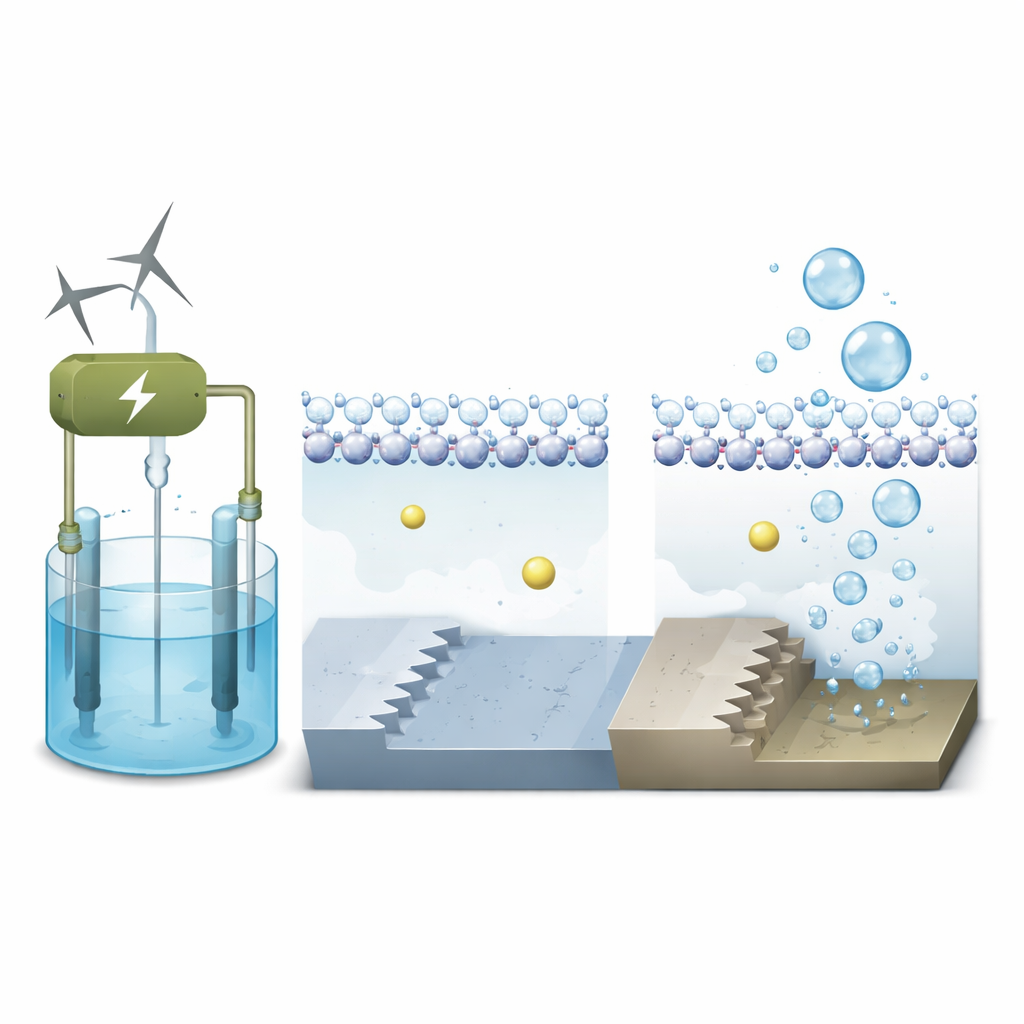
Forskarna fokuserar på platina, referensmaterialet för att dela vatten, och jämför två typer av atomära landskap på dess yta. Den ena är platt, som en slät terrass (kallad Pt(111)); den andra är trappstegsformad, som en liten trappa (Pt(311)). Med avancerade kvantmekaniska simuleringar som inkluderar både elektroner och rörliga vattenmolekyler modellerar de hur dessa olika ytor beter sig under realistiska driftspänningar i en alkalisk elektrolysör. Målet är att se hur den lokala miljön alldeles intill metallen — där vatten, joner och elektroner möts — kontrollerar hastigheten i det första steget vid bildandet av vätgas.
Saltjoner som dolda medhjälpare
I alkalisk elektrolys innehåller vätskan alkalimetalljoner såsom natrium. Dessa positivt laddade joner gör mer än att bara flyta omkring; de kan klustra nära elektroden och subtilt omforma det elektriska fältet vid gränsytan. Simuleringarna visar att på den platta platinaterrassen bildar vattnet ett tätt, ordnat lager med väteatomer som pekar ned mot den negativt laddade ytan. Natriumjonerna håller sig längre bort, separerade från metallen av detta vattenskikt, så deras påverkan på reaktionen är måttlig. På den trappstegsformade ytan binder däremot de underkoordinerade atomerna vid stegkanten vatten starkare och skapar en ojämnare, mer oordnad lokal vattenstruktur.
En särskild när‑ytkluster som drar joner närmare
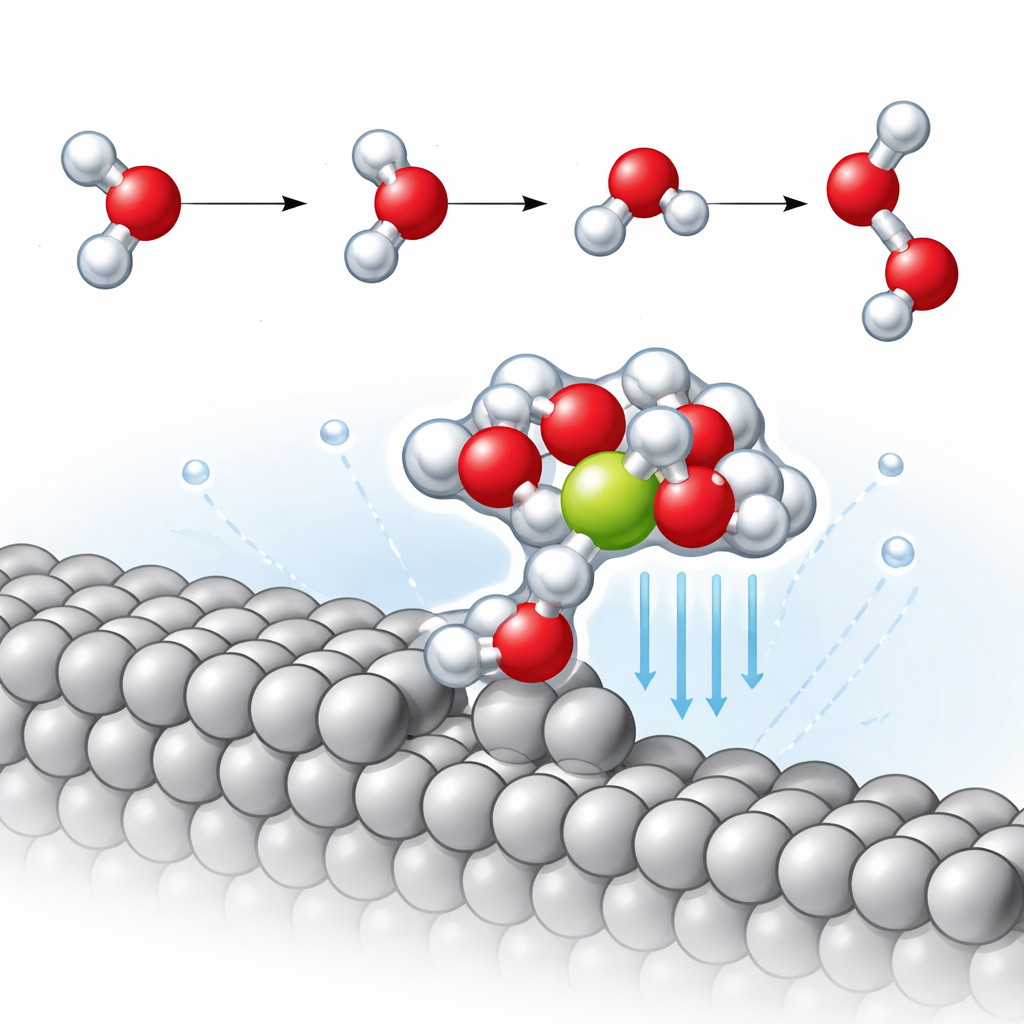
Vid dessa stegkanter upptäcker teamet ett återkommande strukturellt motiv: en vattenmolekyl fäst direkt vid platinasteget som i sin tur håller en närliggande natriumjon omgiven av fler vattenmolekyler. Denna kompakta platina–vatten–natrium‑kluster drar effektivt jonen cirka 2,3 ångström närmare metallen än på den plana ytan. Att vara närmare förstärker det lokala elektriska fältet i denna lilla region avsevärt, vilket starkt polariserar närliggande vattenmolekyler. Simuleringarna visar att en O–H‑bindning i dessa vattenmolekyler sträcks mer än vanligt, vilket indikerar att den delvis håller på att brytas redan innan reaktionen formellt fortskrider.
Sänker barriären för vätgasbildning
Det viktiga långsamma steget i alkalisk vätgasutveckling är känt som Volmer‑steget, där en vattenmolekyl splittras: väte binder till metallen medan den kvarvarande hydroxiden driver ut i vätskan. Genom att följa reaktionsvägen med lägst energi finner författarna att natrium på den plana platinaytan bara har en liten effekt på energi barriären för detta steg. I kontrast sänker den närliggande natrium‑stabiliserade klustern på den trappstegsformade ytan aktiveringsenergin med cirka 0,14 elektronvolt — ungefär tre gånger förbättringen som ses på den plana fasetten. En detaljerad analys av vibrationella rörelser visar att O–H‑bindningen som pekar mot ytan blir avsevärt svagare i närvaro av den nära liggande jonen, vilket gör den lättare att bryta och därigenom påskyndar vätgasbildningen.
En designregel för bättre vätgaskatalysatorer
Sammanfattningsvis konstaterar studien att den bästa prestandan i alkalisk vätgasproduktion inte kommer från metallytan eller elektrolyten ensam, utan från deras synergi. Trappstegsformade platinasiter som kan förankra särskilda vatten–jon‑kluster drar alkalikationer nära, intensifierar det lokala elektriska fältet, för‑bryter delvis vattenbindningar och accelererar starkt det avgörande första steget i vätgasutvecklingen. För en allmän läsare är slutsatsen att genom att noggrant forma katalysytors mikroskopiska geometri och välja elektrolyter som för in rätt joner på rätt platser kan ingenjörer övervinna några av de fundamentala fördröjningarna i alkaliska enheter och utforma mer effektiva, energisparande system för produktion av ren vätgas.
Citering: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Nyckelord: vätgasutveckling, alkalisk elektrolys, platina‑katalysator, gränsytvatten, alkalimetallkationer