Clear Sky Science · sv
Strukturell grund för bildandet av mänskliga RegⅢα-filament
Hur våra tarmar bekämpar mikrober
Våra tarmar är ständigt utsatta för miljarder bakterier, varav många är ofarliga eller till och med nyttiga. Men när farliga mikrober dyker upp behöver kroppen snabba, precisa sätt att angripa dem utan att skada egen vävnad. Denna studie granskar noggrant ett sådant försvarsprotein, kallat RegIIIα, och visar hur det ändrar form för att döda bakterier och sedan övergår till en säkrare, mindre skadlig form. Att förstå denna formförändring kan hjälpa forskare att bättre begripa hur vi håller tarmfloran i balans och vad som går fel vid sjukdom.
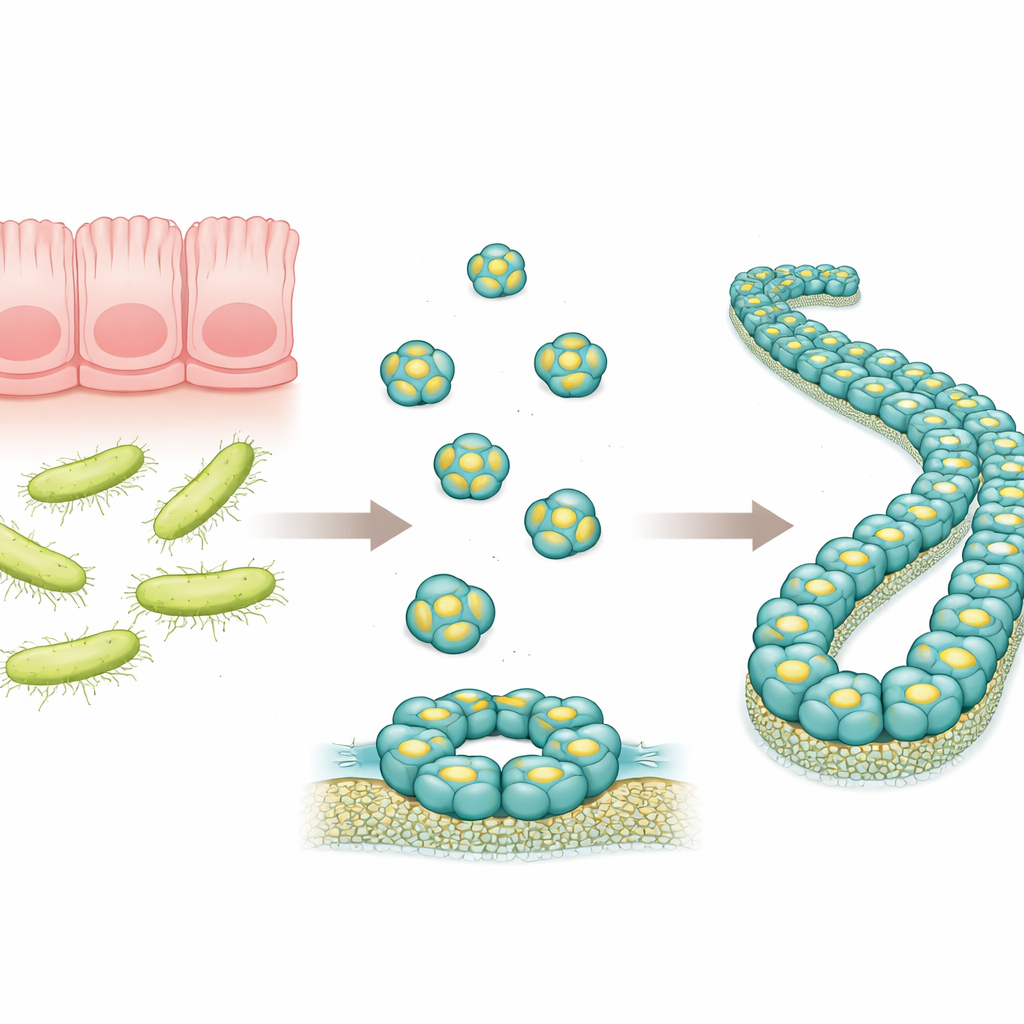
En liten försvarare i tarmen
RegIIIα är ett protein som produceras i matsmältningskanalen och riktar sig mot vissa bakterier, särskilt de med tjocka ytterväggar som kallas Gram-positiva bakterier. Tidigare arbete har föreslagit att RegIIIα kan göra hål i bakteriella membran genom att bilda ringliknande strukturer, vilket tillåter mikrobernas innehåll att läcka ut och leder till död. Forskare har också sett att dessa ringstrukturer med tiden kan staplas till långa filament, som tycks minska proteinets dödande effekt. Exakt hur RegIIIα-molekylerna är ordnade i dessa större sammankomster var dock inte känt i detalj, vilket försvårade förståelsen av hur proteinet fungerar och hur dess aktivitet regleras.
Att se filamentet i atomär detalj
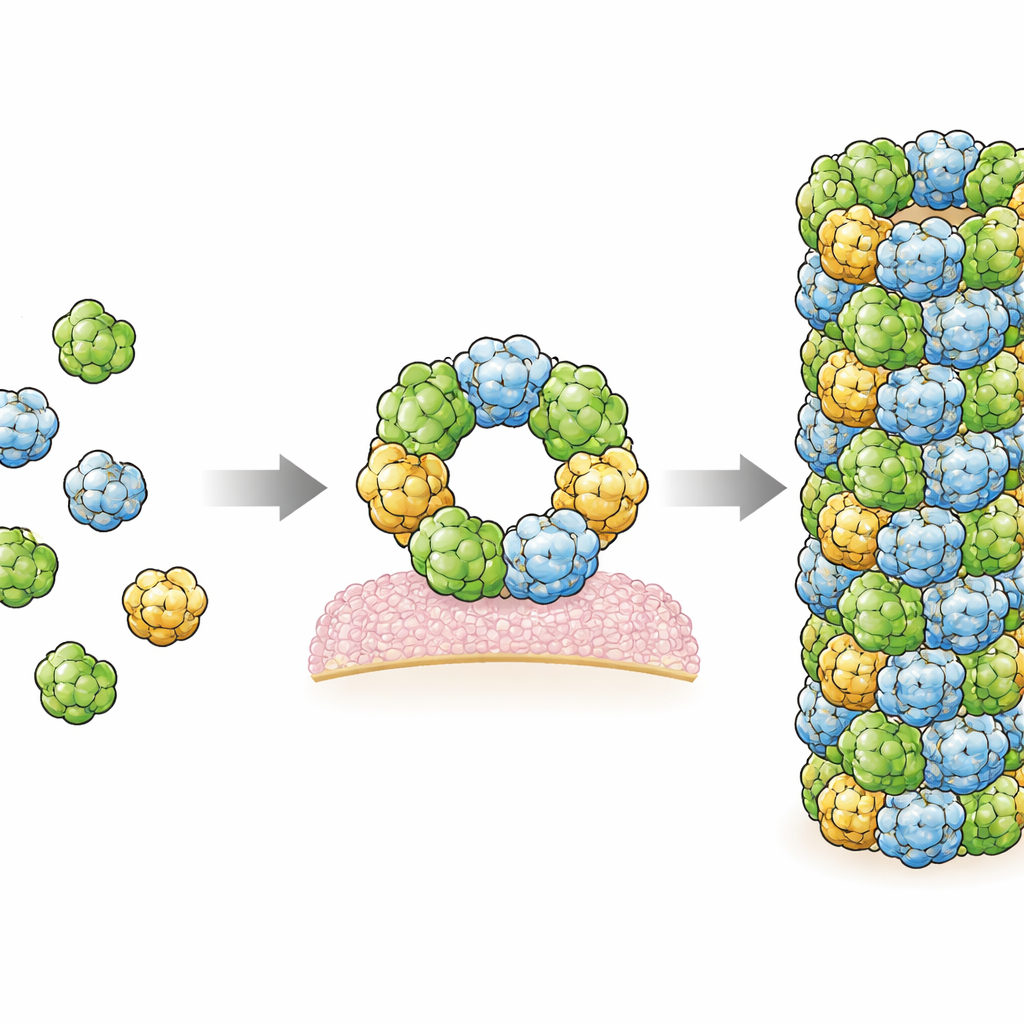
I denna studie framställde författarna mänskligt RegIIIα i bakterier och fick det att montera sig till filament under kontrollerade förhållanden. De använde en kraftfull bildteknik kallad kryo-elektronmikroskopi, som kan visualisera biologiska molekyler frysta i ett tunt iskikt vid nästan atomär upplösning. De fann att filamenten byggs upp av upprepade enheter om tre identiska RegIIIα-molekyler, så kallade trimrar, som staplas i ett regelbundet helixmönster. Varje individuell RegIIIα-molekyl liknar mycket det som tidigare setts i kristallstrukturer, men deras orientering inom filamentet skiljer sig från en tidigare modell med lägre upplösning. Denna korrigerade orientering ändrar hur forskare tänker om proteinets interaktion med bakteriella membran och med dess egen regulatoriska del.
Hur proteiner länkas och varför lipider spelar roll
Genom att granska strukturen noggrant identifierade forskarna två huvudkontaktområden, eller gränssnitt, där intilliggande RegIIIα-molekyler rör vid varandra och håller ihop filamentet. De alternerade sedan specifika aminosyror vid dessa gränssnitt och visade att dessa förändringar förhindrade filamentbildning, vilket bekräftar att kontaktställena är avgörande. Intressant nog visade kryo-EM-kartorna extra suddiga regioner i båda gränssnitten som sannolikt representerar små, långsträckta molekyler inpassade mellan proteiny torna. Deras form och kemiska miljö tyder på att det kan vara lipider, samma typ av oljiga molekyler som utgör cellmembran. Detta stöder tidigare antydningar om att lipider främjar RegIIIα-assemblage, möjligen genom att fungera som molekylärt lim som stabiliserar förbindelserna mellan subenheterna.
På/av-brytaren: pH och en dold segment
Teamet undersökte också vad som styr när RegIIIα kan montera sig. Innan det blir aktivt bär proteinet en kort ”pro-sekvens” som måste klippas av av matsmältningsenzymer. I deras högupplösta filamentstruktur finns det inget utrymme i mitten av komplexet för denna extra bit, vilket antyder att pro-sekvensen blockerar RegIIIα:s förmåga att bilda de porbildande ringarna och filamenten från början. De fann att benägenheten att bilda filament också beror på surhetsgrad: filament bildas lätt vid ett pH liknande tunntarmens men dåligt vid ett mer surt pH. En enda aminosyra, histidin 50, verkar fungera som en pH-känslig brytare; när den ändras till en annan rest blir filamentbildningen mycket mindre känslig för pH. Tillsammans skapar dessa egenskaper—enzymatiskt klippande, lipidbindning och pH—ett flerskiktat kontrollsystem som finjusterar när och var RegIIIα är aktivt.
Vad detta betyder för tarmsundhet
Sammanfattningsvis ger detta arbete den mest detaljerade bilden hittills av hur RegIIIα-molekyler monteras till större strukturer som relaterar både till deras antibakteriella verkan och deras självbegränsande beteende. De samma gränssnitt som bygger filamenten bygger också de hexameriska ringarna som tros bilda porer i bakteriella membran, vilket antyder en fin balans mellan en potent dödande form och ett säkrare, nedtonat tillstånd. Att kartlägga sjukdomsrelaterade mutationer på denna struktur visar att många ligger vid nyckelkontaktpunkter, vilket tyder på att störningar i assemblage kan ligga bakom vissa tarm- eller bukspottkörtelstörningar. Genom att klargöra hur detta naturliga antibiotikum aktiveras, styrt av lipider och format av lokalt pH, lägger studien grunden för framtida försök att modulera vårt medfödda försvar—antingen genom att stärka det mot infektion eller dämpa det när det blir felreglerat.
Citering: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Nyckelord: RegIIIα, intestinalt immunförsvar, kryo-elektronmikroskopi, proteinfilament, antibakteriella peptider