Clear Sky Science · sv
Azobensen-broförsedda joniserbara amfifila Janus-glykosider för ljusstyrd, enkeldels och organ-modulerbar pDNA-leverans
Lyser upp vägen för smartare genleverans
Genterapier lovar att behandla sjukdomar vid deras rot genom att leverera genetisk information direkt in i våra celler. Men att styra detta känsliga innehåll säkert genom blodomloppet, till rätt organ och in i målcellerna är fortfarande en stor utmaning. Denna studie presenterar en ny klass små, sockerbaserade partiklar vars beteende kan växlas med ljus innan de ens kommer in i kroppen, vilket gör det möjligt för forskare att omdirigera var en terapeutisk gen hamnar och hur starkt den uttrycks — samtidigt som cellerna i huvudsak förblir oskadade. 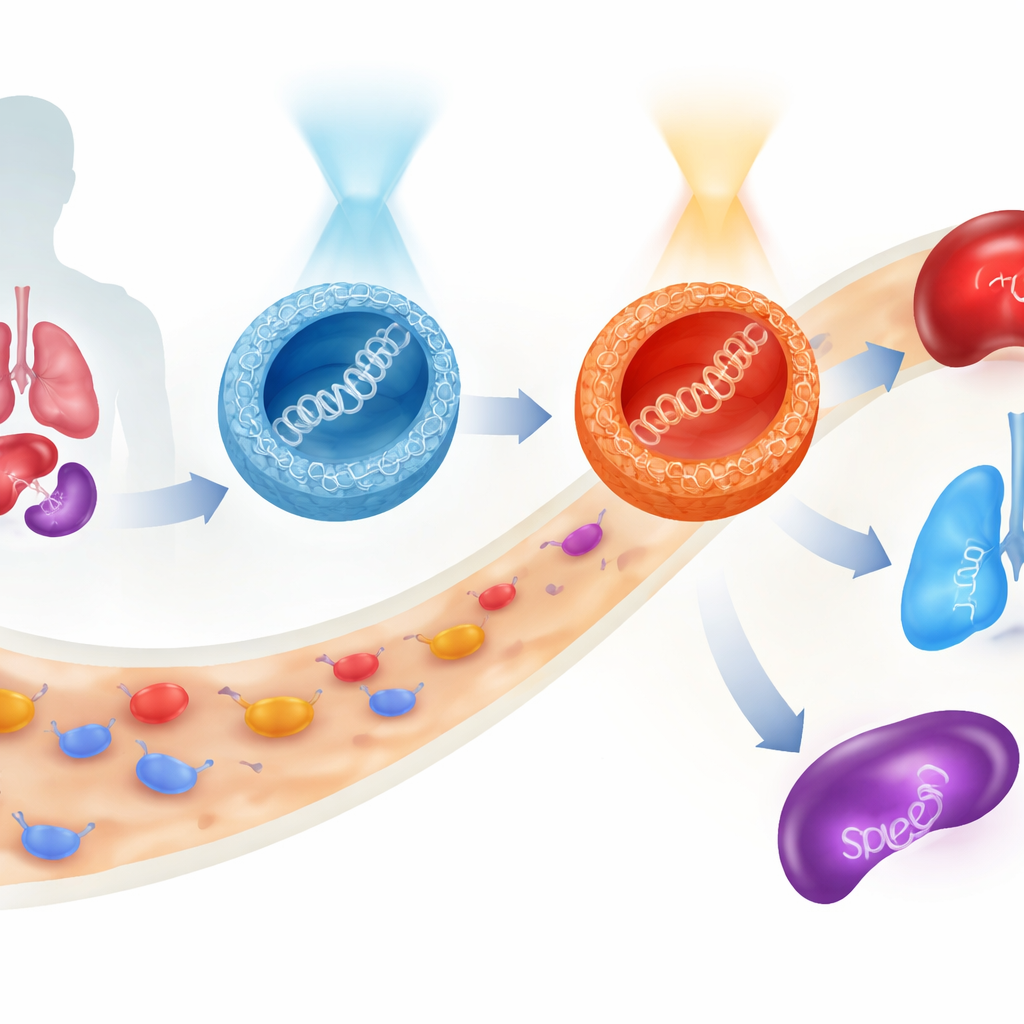
Behov av precisa genetiska budbärare
Dagens mest framgångsrika vektorer för genleverans är lipidnanopartiklar, som bidrog till att göra mRNA-vaccinen mot COVID-19 möjliga. Dessa mångkomponentdroppar omsluter och skyddar nukleinsyror, men tenderar att ackumuleras huvudsakligen i levern och släppa ut bara en liten andel av sitt innehåll inne i cellerna. Att finjustera deras sammansättningar kan ändra vilka organ de föredrar, men blandningarna är komplexa och svåra att kontrollera exakt. Forskarna bakom detta arbete bestämde sig istället för att utforma enkla, väldefinierade molekyler som sätter ihop sig till nanopartiklar med förutsägbara former och beteenden — och som kan aktivt justeras utifrån med en enkel ljusutlösare.
En molekylär gungbräda styrd av ljus
I kärnan av det nya systemet finns tvilling-Janus-glykosider: molekyler byggda av två glukosenheter, försedda med vattenälskande laddade huvuden och fettälskande svansar, och förenade genom en central azobensen-"gångjärn." Azobensen kan växla mellan två spegelvända former, kallade E och Z, när den utsätts för olika färger av ljus. I vatten med DNA närvarande samlas många kopior av dessa molekyler spontant till mjuka, lager-på-lager-partiklar som omsluter plasmid-DNA-strängar. Forskarna framställde två versioner — en med syrebroar och en med svavelbroar mellan sockret och gångjärnet — för att subtilt stämma av stabilitet och biologiskt beteende. Genom att förbelysta lösningarna kunde de berika antingen E- eller Z-formen och studera hur varje tillstånd formar de resulterande genleveranspartiklarna.
Hur formskiftande partiklar beter sig
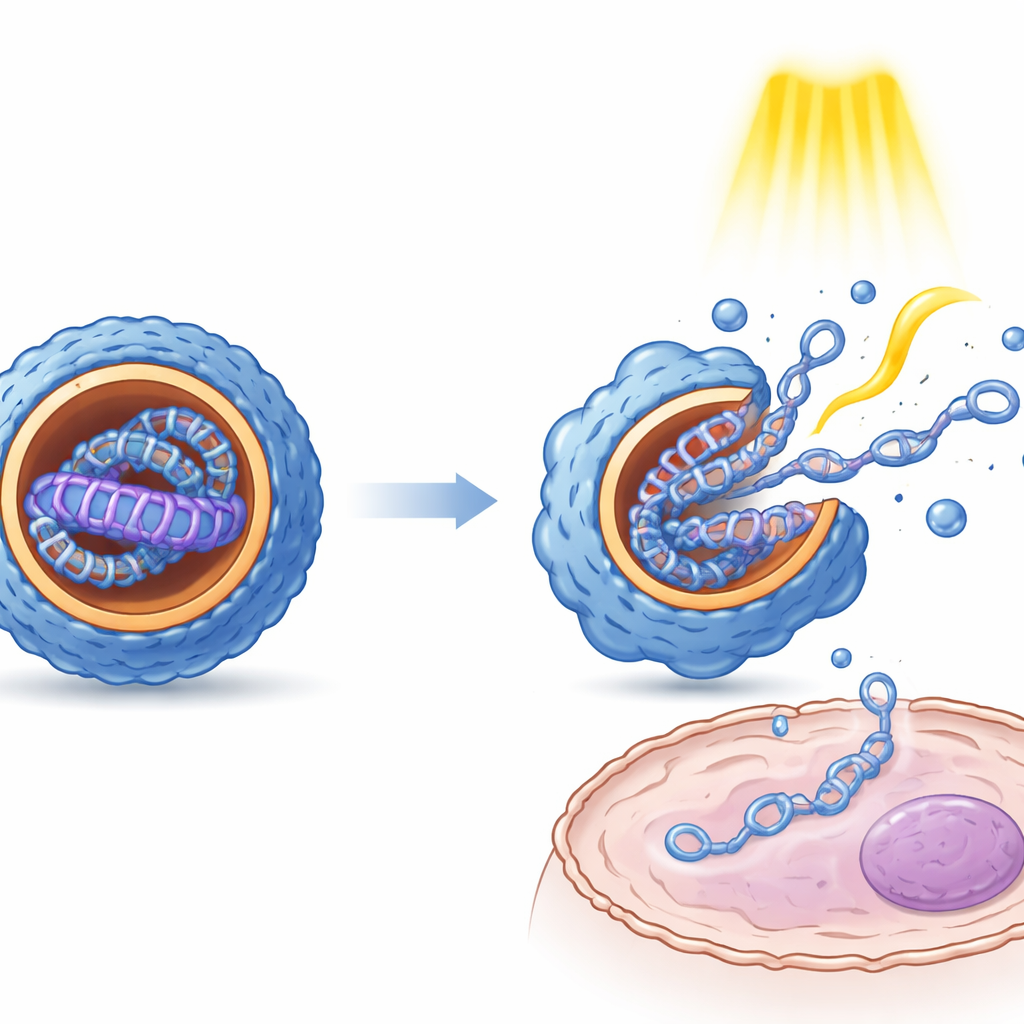
Mätningar av partiklarens storlek, ytladdning och inre struktur visade att ljusstyrd växling mellan E- och Z-tillstånden får tydliga fysiska konsekvenser. Generellt gav Z-formen mindre, mer enhetligt formade nanopartiklar med ett mer ordnat, lagerlikt inre än E-formen. Mikroskopi visade att dessa interna arrangemang liknar alternerande skikt av lipidlikt material och DNA. Viktigt är att båda tillstånden skyddade DNA från enzymatisk nedbrytning. I odlade celler från njure, lever och immunt vävnad gav de olika isomertillstånden påtagligt olika nivåer av genuttryck, trots att det underliggande DNA:t var identiskt. Upprepade ljuspulser applicerade efter att partiklarna hade tagit sig in i cellerna ökade genuttrycket flera gånger om, vilket tyder på att den mekaniska stöt som uppstår vid växling hjälper partiklarna att luckra upp sig och frigöra sitt innehåll, och möjligen också hjälper dem att undkomma intracellulära compartment.
Vägleda gener till specifika organ
Det mest överraskande beteendet framträdde hos möss. När de syre-bridgade partiklarna gavs i sin E-rika form uppstod uttryck av en markörgen mestadels i levern med en del i lungorna. Genom att förväxla dem till Z-form innan injektion ökade inte bara det totala uttrycket, utan balansen skiftade också mot lungorna. De svavel-bridgade partiklarna visade en annan bild: deras Z-form favoriserade mjälten, ett centralt immunsystemorgan. Således, med samma grundläggande molekylära ramverk — och utan att ändra DNA-lasten — kunde forskarna rikta genaktivitet främst till lever, lunga eller mjälte enbart genom att välja länkningstyp (syre eller svavel) och den ljusaktiverade formen (E eller Z) av bäraren. Under dessa tester förblev cellernas livskraft hög, vilket tyder på att systemet är relativt milt.
En ljusjusterbar väg mot framtida genläkemedel
I vardagliga termer har teamet byggt en liten, ljusbrytbar transportör för DNA. Före injektion "programmeras" transportörerna med en kort ljusbehandling till en av två former. Varje form bygger upp nanopartiklar med karakteristisk storlek och ytegenskap, vilket i sin tur bestämmer hur starkt de fäster vid olika celltyper och var de hamnar i kroppen. Eftersom samma kemiska stomme kan modifieras på många små sätt, och eftersom växlingen är reversibel och inte ändrar DNA:t självt, erbjuder denna plattform ett flexibelt sätt att finjustera var och hur genterapier verkar. Mycket återstår innan klinisk användning, men studien visar att noggrant designade, en-molekylära bärare kontrollerade av ljus kan bli kraftfulla verktyg för säkrare, mer precisa genetiska läkemedel.
Citering: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Nyckelord: genleverans, ljusresponsiva nanopartiklar, azobensenbrytare, riktad DNA-terapi, nanomedicin