Clear Sky Science · sv
S9‑proteaset WprP2 katalyserar enhetlig klyvning av prekursorpeptiden i RiPP‑biosyntes
Varför små skärverktyg i celler spelar roll
Inuti bakterier skär specialiserade molekylära saxar långa kedjor av aminosyror till mindre, aktiva bitar som ofta blir antibiotika eller andra användbara naturprodukter. Denna studie avslöjar ett tidigare okänt skärverktyg — ett proteas kallat WprP2 — som trimar sitt målpeptid med ovanlig precision. Att förstå hur detta enzym fungerar kan hjälpa forskare att designa nya bioaktiva peptider och nästa generations antibiotika.
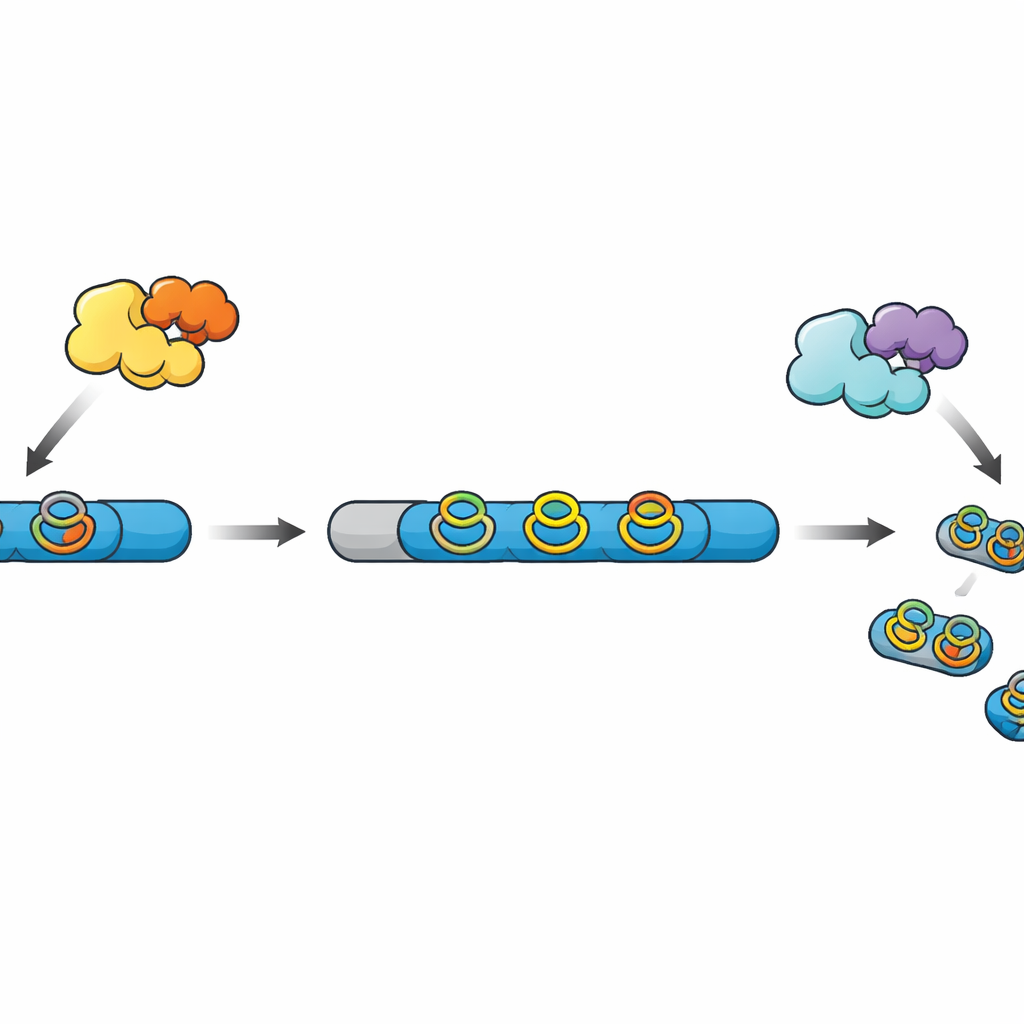
Från råa kedjor till färdiga mini‑mediciner
Många moderna peptidbaserade naturprodukter, som samlas under beteckningen RiPPs, börjar som enkla kedjor syntetiserade på ribosomen. Dessa kedjor innehåller en leader‑region som fungerar som ett handtag och en core‑region som efter en serie kemiska modifieringar blir den slutliga produkten. Andra enzymer lägger till korslänkar och ringar som gör peptiden mer stabil och mer aktiv, och slutligen skär ett proteas bort leadern och frigör den mogna molekylen. I en nyligen upptäckt familj av RiPPs bygger radikal‑SAM‑enzymer kompakta ”cyklofan”‑ringar som involverar aromatiska aminosyror, men i de flesta kända genkluster saknas det matchande proteaset, vilket lämnar de sista bearbetningsstegen mystiska.
Spåra upp en saknad partnerenzym
Författarna studerade tidigare ett radikal‑SAM‑enzym kallat WprB1 som installerade identiska korslänkar vid tre upprepade WPR‑segment i en prekursorpeptid. I det nya arbetet sökte de i bakteriella genom efter släktingar till detta enzym och letade i närheten efter gener som kunde koda för ett proteas. I Streptomyces venezuelae fann de ett lovande kluster som innehöll ett liknande korslänkningsenzym, dess hjälpprotein, en matchande prekursorpeptid med tre WPR‑upprepningar och ett kandidatserinproteas av S9‑familjen, som de namngav WprP2. Det gjorde systemet till en idealisk testbädd för att ta reda på hur peptiden slutligen skärs för att frigöra de aktiva fragmenten.
Följa peptiden när den skivas
För att undersöka WprP2 producerade teamet prekursorpeptiden i bakterier, både med och utan korslänkningsenzymet, renade den och blandade den sedan med proteaset i kontrollerade in vitro‑reaktioner. Masspektrometri visade att WprP2 först klipper kedjan omedelbart efter varje WPR‑segment, och sedan utför en andra klyvning på ett fast avstånd före en viss prolinrest längre fram i sekvensen. Dessa två steg skapar en serie mindre, enhetliga fragment. Anmärkningsvärt nog utförde WprP2 detta mönster av klyvningar oavsett om korslänkningsenzymet redan hade installerat cyklofanringarna, vilket visar att ringarna inte krävs för igenkänning. Jämfört med kommersiellt trypsin, som inte kan klyva vid vissa korslänkade positioner, fungerade WprP2 fortfarande, vilket understryker dess ovanliga robusthet.
Avkoda vad enzymet känner igen
Forskarna frågade därefter vilka egenskaper hos peptiden WprP2 faktiskt läser av. Genom att systematiskt byta ut enskilda aminosyror runt klyvningsställena fann de att ändringar av många närliggande rester hade liten effekt, men att ändring av en nyckel‑arginin inom WPR‑segmentet eller glutaminet eller prolinet vid det andra klyvningsstället kunde blockera just det steget. Experiment med en relaterad prekursorpeptid med olika flankrester visade att proteaset fortfarande klippte efter WPR‑upprepningar men endast utförde den andra klyvningen när ett glutamin‑prolin‑par var närvarande. Datorgenererade strukturella modeller med AlphaFold3 stödde denna bild: i de predikterade komplexen linjerade WPR‑baserade och glutamin‑prolin‑ställena vardera i tur med enzymets katalytiska centrum, förenligt med en sekventiell tvåstegs‑mekanism.
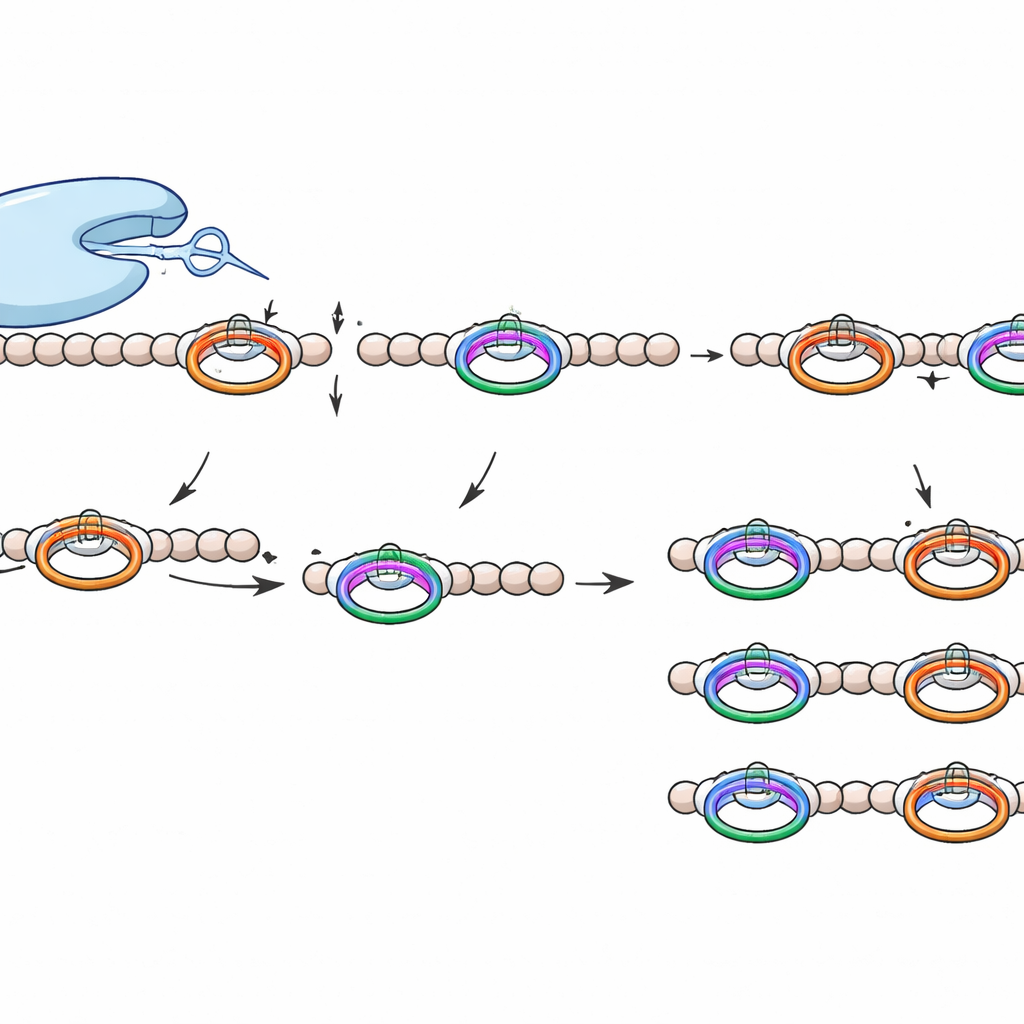
Vad som gör detta skärverktyg speciellt
WprP2 tillhör en bredare S9‑familj av proteaser som redan inkluderar medicinskt relevanta enzymer, men det sticker ut på flera sätt. Det klyver på N-terminal sida om en prolinrest snarare än efter den, det verkar på ett upprepande motiv för att generera jämnt stora fragment över hela prekursor‑kedjan, och det visar bred tolerans för de aminosyror som ligger mellan dess två igenkänningsställen. Denna kombination av precision och flexibilitet har inte tidigare observerats hos RiPP‑relaterade proteaser.
Hur denna upptäckt kan användas
Genom att avslöja ett proteas som känner igen enkla sekvensledtrådar och utför enhetliga, upprepade klyvningar tillför detta arbete ett kraftfullt nytt verktyg till den växande verktygslådan för peptidteknik. I praktiska termer skulle WprP2 kunna utnyttjas för att frigöra eller omforma designade peptider, inklusive sådana med komplexa korslänkar som står emot standardenzymer som trypsin. För icke‑specialister är huvudpoängen att forskare har upptäckt en ny typ av molekylära saxar som skär långa peptidkedjor i precisa, jämn‑stora bitar, vilket öppnar dörren för mer kontrollerad produktion av potentiella antibiotika och andra bioaktiva molekyler.
Citering: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Nyckelord: RiPP‑peptider, serinproteas, WprP2, cyklofan‑naturliga produkter, peptidteknik