Clear Sky Science · sv
Steriskt konformationsinducerat emissionsprob för att övervaka proteiners konformation i levande celler
Att iaktta formförändrande proteiner i realtid
Inne i varje levande cell ändrar proteiner ständigt form när de vidarebefordrar signaler, känner av sin omgivning och utför viktiga uppgifter. Många sjukdomar uppstår när dessa formförändringar misslyckas, men det har varit anmärkningsvärt svårt att direkt följa sådana rörelser i levande celler, särskilt över både mycket snabba och långsamma tidskalor. Denna artikel introducerar en ny ljusemitterande prob, kallad BIOSCE, som omvandlar små proteinrörelser till synliga ljusförändringar, vilket gör det möjligt för forskare att följa enskilda proteiner när de böjer sig, vrider sig och interagerar i realtid inne i levande celler. 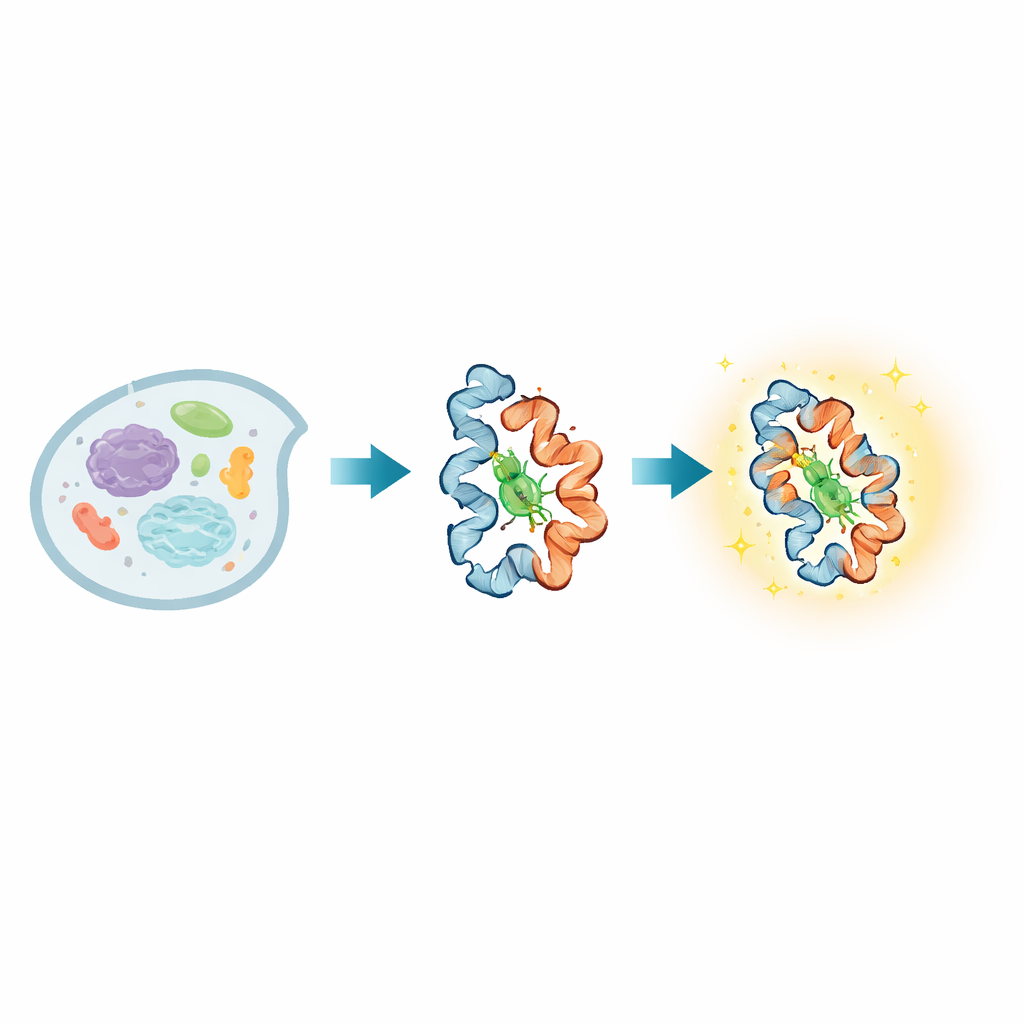
En ny ljusbrytare för rörliga proteiner
I kärnan av BIOSCE finns en liten färgmolekyl, MTPABP-Cl, som blir ljusstarkare när den pressas ihop. Forskarna fäster denna färg vid en ofta använd proteintagg kallad HaloTag, som kan fuseras genetiskt med nästan vilket protein som helst. När det taggade proteinet ändrar form eller packas tätare med grannar ändras hur mycket “utrymme” färgen har att röra sig på. I en lös miljö kan färgens interna delar rotera fritt och en större del av den absorberade ljusenergin går förlorad som rörelse; i ett trängre fickformat blockeras dessa rörelser och färgen avger i stället mer av energin som ljus. Denna “steriskt konformationsinducerade emission” omvandlar subtila förändringar i lokal trängsel kring ett enda protein till en jämn ändring i ljusstyrka, snarare än en enkel på/av-signal, vilket gör proben mycket känslig för små konformationsförändringar.
Att bygga och testa den tryckkänsliga färgen
Teamet designade och syntetiserade först MTPABP-Cl så att den skulle vara svag i lösning men ljusna när den hålls på plats av HaloTag eller av ett mer kompakt fusionsprotein. Noga mätningar visade att färgen absorberar blått ljus och emitterar i långt rött spektrum, vilket är fördelaktigt för avbildning djupt inne i celler och för långtidsobservationer. När den var bunden endast till HaloTag ökade ljusutbytet; när HaloTag fuserades till en partnerprotein som veckade sig runt färgen ökade ljusstyrkan ännu mer. Datorsimuleringar bekräftade att i mer kompakta proteinarrangemang upplever färgen starkare trängsel, en mindre exponerad yta och fler stabiliserande kontakter — allt som begränsar rörelse och förstärker emissionen. Färgen binder också snabbt och specifikt till HaloTag, visar mycket låg bakgrund i celler utan taggen och förblir icke-toxisk vid arbetssammanhang, vilket stödjer dess användning i experiment med levande celler. 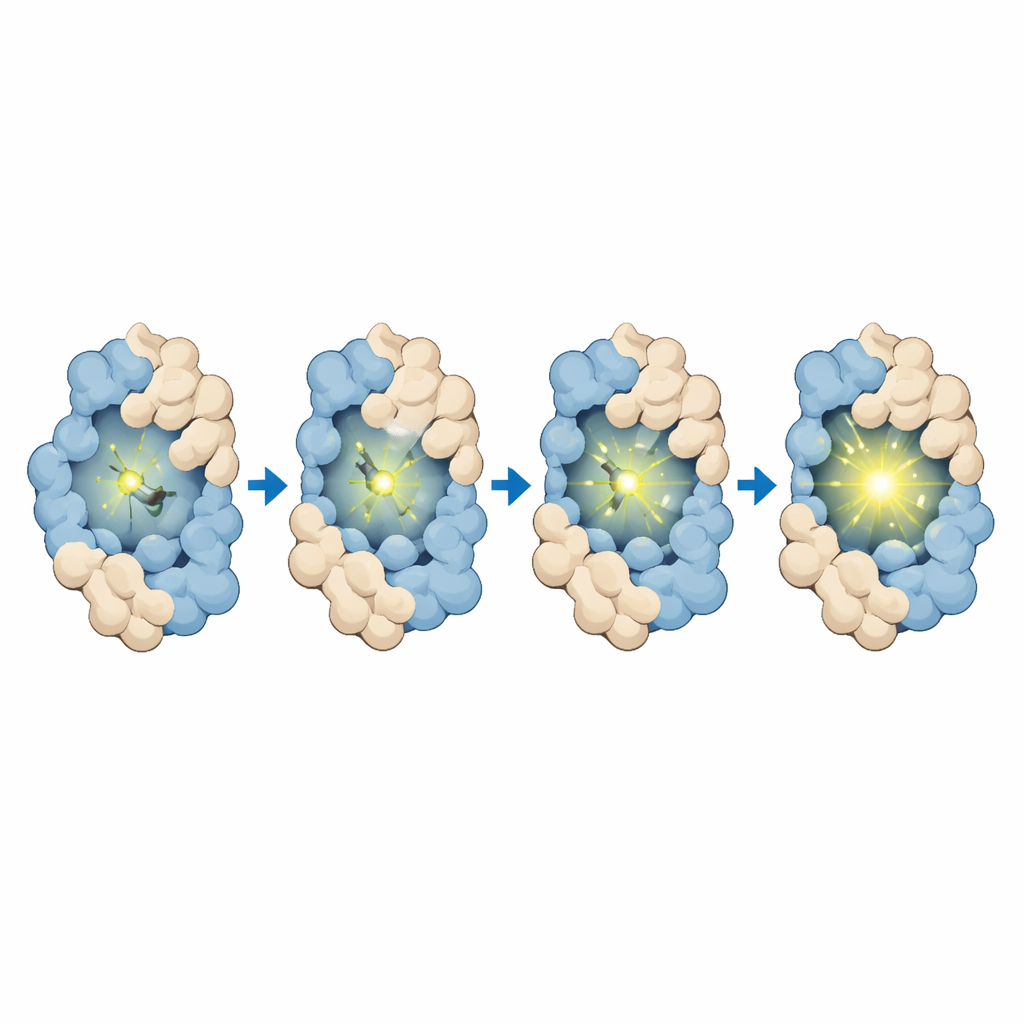
Följa snabba signaler och proteinmöten
För att visa vad BIOSCE kan göra applicerade författarna den på flera välkända cellulära processer. Först anpassade de en kalciumsensor baserad på kalmodulin, ett protein som ändrar form när det binder kalciumjoner — centrala budbärare vid nervutskott och många andra cellulära händelser. Genom att fusera kalmodulin till HaloTag och märka det med MTPABP-Cl skapade de en kemigenetisk indikator kallad SCECaMP. I humana celler och neuronliknande celler ljusnade och mörknade denna indikator i takt med kalciumspikar framkallade av kaliumstimulering, med responstider jämförbara med de välanvända fluorescerande proteinerna GCaMP. Eftersom BIOSCE-signalen beror direkt på lokal trängsel kring färgen kan den troget spegla kalmodulins strukturella förändringar samtidigt som den ger stabil fluorescence lämplig för utsträckt avbildning.
Se drogframkallade interaktioner och toxinskador
Forskarna frågade sedan om BIOSCE kunde spåra när två proteiner förs samman av en läkemedelssignal. De använde ett klassiskt system där rapamycin drar ihop två partners, FKBP och FRB, i en viktig tillväxtreglerande väg. Genom att fästa HaloTag på antingen FKBP eller FRB och märka med MTPABP-Cl observerade de snabba, millisekundsskala ökningar i fluorescens när rapamycin inducerade dessa proteiner att närma sig och omstrukturera sig. Ökningen i ljusstyrka speglade en tätare mikroomgivning runt färgen när partnerna kom i nära kontakt. I ett mer komplext test studerade de SNAP25, ett nervterminalprotein avgörande för frisättning av neurotransmittorer och huvudmålet för botulinumneurotoxin A. Genom att placera HaloTag på vardera sidan om toxinets klyvningsställe och märka med färgen kunde de separat följa rörelserna hos de N-terminala och C-terminala fragmenten efter klyvningen. Enkelpartikelspårning visade att ett fragment förblev förankrat nära cellmembranet, medan det andra diffunderade friare genom cytoplasman, och att det exakta mönstret berodde på om märkning skedde före eller efter toxinexponering. Proben rapporterade till och med snabba, zinkinducerade konformationella finjusteringar i SNAP25 under processen.
Vad detta betyder för biologi och medicin
Tillsammans visar dessa resultat att BIOSCE är ett mångsidigt nytt sätt att visualisera hur enskilda proteiner rör sig, veckas och interagerar inne i levande celler över ett brett spektrum av tidskalor. Eftersom metoden bygger på en generell HaloTag-fusion och en enda liten molekylfärg kan den i princip tillämpas på många olika proteiner utan att sensorn behöver omdesignas för varje fall. Den kontinuerliga, konfinansberoende ljushetsförändringen gör det möjligt för forskare att upptäcka subtila strukturella skiftningar istället för endast stora, binära händelser. Framöver planerar författarna att förbättra probleverans och avbildningsdjup så att BIOSCE kan användas i vävnader och hela organismer. Om detta lyckas kan tillvägagångssättet bli ett kraftfullt verktyg för att koppla var proteiner befinner sig, hur de rör sig och vad de gör i hälsa och sjukdom, och kan i slutändan mata in i detaljerade datormodeller av cellulärt beteende.
Citering: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Nyckelord: proteiners konformationsdynamik, avbildning i levande celler, fluorescerande biosensorer, HaloTag-prober, botulinumneurotoxin