Clear Sky Science · sv
Direkt diazotisering av indoler med 2-metoxiethyl nitrit
Att omvandla en problematisk gas till användbar kemi
Kväveoxid ses ofta som en besvärlig industrigas: den är giftig, svår att hantera och betraktas vanligtvis som avfall. Samtidigt är den rik på kväve, ett nyckelgrundämne i många läkemedel. Denna studie visar hur kemister kan tygla kväveoxid genom att omvandla den till ett stabilt flytande reagens som i sin tur hjälper till att bygga komplexa molekyler med koppling till läkemedelskandidater. Arbetet erbjuder ett sätt att förvandla en farlig biprodukt till ett verktyg för att framställa värdefulla föreningar på ett säkrare och renare sätt.
En ny hjälpmolekyl för knepiga reaktioner
Kemister förlitar sig ofta på ”diazo”-föreningar — molekyler som bär ett mycket reaktivt par kväveatomer — för att bygga intrikata kolramverk. Dessa ramverk återfinns i många läkemedel, särskilt de baserade på indoler, ett ringsystem som är vanligt i naturprodukter och läkemedel. Traditionella sätt att framställa diazoföreningar använder ofta explosiva azider eller stora mängder starka syror och baser, vilket skapar säkerhets- och miljöproblem. Författarna fokuserar på ett säkrare alternativ: en vätska kallad 2-metoxiethyl nitrit, eller MOE-ONO, som kan framställas direkt från kväveoxidgas, syre och en enkel alkohol, och som endast ger vatten som biprodukt.
Direkt omarbetning av en viktig läkemedelslik ring
Gruppen satte som mål att fästa diazogrupper direkt på indoler och modifiera dem vid en bestämd position på ringen utan hårda förhållanden. De upptäckte att en kombination av MOE-ONO med en vanlig organisk radikal, TEMPO, och en liten mängd av en metalsaltkatalysator baserad på scandium utlöser denna omvandling effektivt. Jämfört med klassiska blandningar av natriumnitrit och syra, eller med andra flytande kväveoxiddonatorer som tert-butylnitrit, ger den nya kombinationen högre utbyten, betydligt färre oönskade biprodukter och fungerar på mycket kortare tid. Även indoler som tidigare motstått äldre metoder — såsom de med stora fenylgrupper — kunde omvandlas rent med detta tillvägagångssätt.
En metod, många byggstenar
Efter att ha optimerat reaktionen testade forskarna hur brett den kunde tillämpas. De fann att ett stort antal indolderivat tolererade förhållandena, inklusive de med estrar, ketoner, amider och olika substituenter runt ringen, från elektronrika alkyl- och metoxigrupper till halogener och cyano-grupper. Metoden sträckte sig också bortom indoler till närbesläktade naftolföreningar och bildade diazoderivat som tidigare krävde längre, flerstegsprocedurer. Noterbart är att reaktionen fortfarande fungerade när den kördes i vatten, trots att startämnena inte löser sig väl i det. Detta så kallade ”on-water”-beteende antyder att enkel omrörning i vatten ger ett grönare medium som hjälper reaktionen att gå framåt samtidigt som beroendet av organiska lösningsmedel minskas.
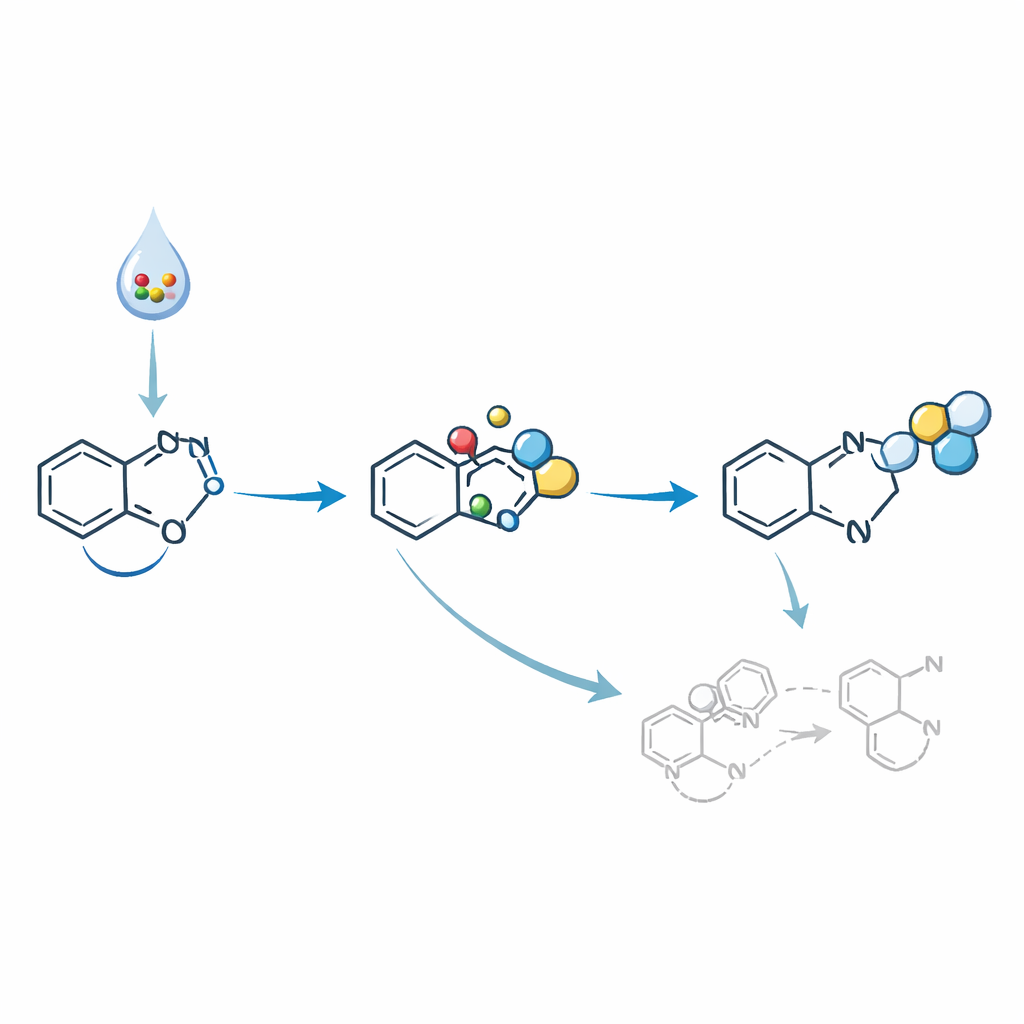
Från reaktiva mellanprodukter till läkemedelskandidater
För att visa varför dessa diazoindoler är värdefulla omvandlade författarna dem vidare till mer förfinade molekyler. Med en rodiumkatalysator omvandlade de diazogruppen till en mycket reaktiv mellanprodukt kallad en karben, som sedan bildade nya bindningar för att skapa cyklopropanringar vid specifika positioner på indolen. I en annan sekvens sammanställde de en kandidat som modulerar en receptor involverad i blodsockerreglering, vilket visar metodens relevans för medicinsk kemi. De visade också att Grignard-reagenser — klassiska koltillsatsverktyg — selektivt kunde fästa vid en position på diazoindolen samtidigt som diazogruppen förblev intakt, vilket öppnar för stegvis konstruktion av tätt substituerade indol- och indolinstrukturer.
Hur reaktionen håller sig på rätt spår
I bakgrunden finns flera konkurrerande vägar som kan leda till oönskade nitro- eller oximprodukter i stället för de önskade diazoföreningarna. Mekanistiska experiment tyder på att TEMPO hjälper till att styra kemin genom att fånga skadliga radikaler och fånga en flyktig nitroso-mellanprodukt innan den kan omarrangera. Ytterligare kväveoxidmolekyler adderas sedan i följd och bildar slutligen diazogruppen samtidigt som ofarlig nitrat frigörs. Scandiumsaltet verkar främja sönderfallet av MOE-ONO till reaktiva arter och aktivera indolskärnan, vilket ytterligare förbättrar effektiviteten. Upptäckten av nitrat i slutblandningen stöder denna föreslagna väg från kväveoxiddonator till diazoprodukt.
Säker och hållbar väg till komplexa molekyler
Sammantaget presenterar detta arbete ett praktiskt sätt att installera mycket användbara diazogrupper på indolringar utan att förlita sig på explosiva reagenser eller hårda förhållanden. Genom att använda en stabil vätska härledd från kväveoxidgas både ”uppcyklar” metoden en problematisk industriell emission och effektiviserar tillgången till komplexa, läkemedelslika molekyler. För icke-specialister är huvudbudskapet att skicklig kemi kan omvandla en giftig avfallsgas till en mångsidig byggsten för framtida läkemedel samtidigt som miljöpåverkan minskas på vägen.
Citering: Hashidoko, A., Kitanosono, T., Nakao, Y. et al. Direct diazotization of indoles with 2-Methoxyethyl nitrite. Commun Chem 9, 104 (2026). https://doi.org/10.1038/s42004-026-01910-1
Nyckelord: återanvändning av kväveoxid, diazoindoler, grön organisk syntes, indolbaserade läkemedel, NO-donatorreagenser