Clear Sky Science · sv
Minimerad provförbrukning för tidsupplöst seriekristallografi tillämpad på redoxcykeln hos mänskligt NQO1
Att se enzymer i arbete med färre värdefulla prover
Modern biologi förlitar sig ofta på kraftfulla röntgenlaser för att se hur livets molekyler rör sig och ändrar form, men dessa experiment förbrukar vanligtvis stora mängder noggrant berett protein. Denna studie introducerar ett nytt sätt att "mata" små proteinkristaller in i en röntgen free-electron-laser mycket mer effektivt, vilket minskar materialbehovet med upp till 97 %. Den visar också att denna sparsamare metod ändå kan fånga de tidiga stegen i aktiviteten hos ett medicinskt relevant mänskligt enzym, vilket öppnar dörren för mer rutinmässiga filmer av proteiner i arbete. 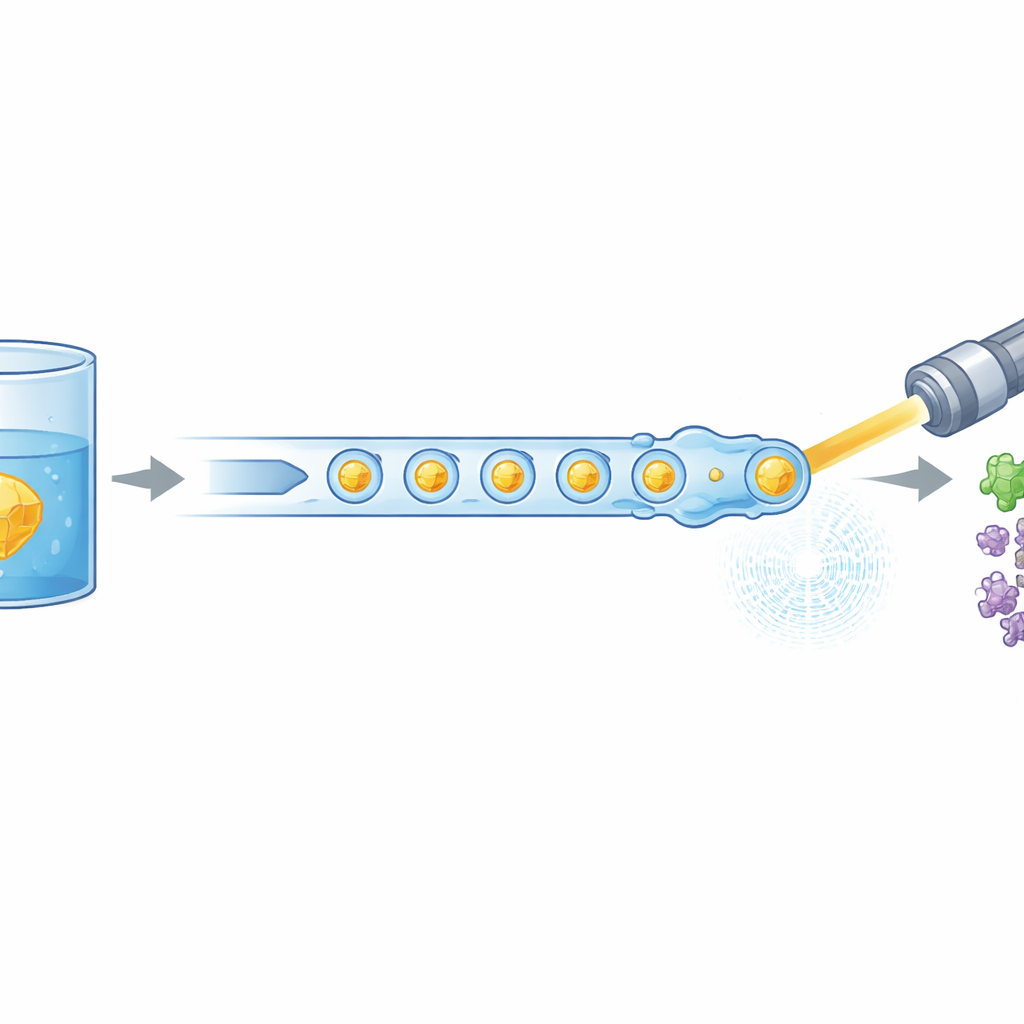
Varför molekylfilmer är så kostsamma
För att förstå hur proteiner faktiskt utför sina uppgifter vänder sig forskare i allt större utsträckning från statiska ögonblicksbilder till tidsförlopp—"filmer" som följer reaktioner i realtid. Ett ledande tillvägagångssätt, tidsupplöst seriekristallografi, sprutar miljontals mikroskopiska proteinkristaller genom en extremt ljusstark röntgenstråle. Varje kristall träffas bara en gång, vilket ger en skadefri inblick i strukturen, och tusentals sådana bilder kombineras till en hel bild. Problemet är att varje tidpunkt i en reaktion—tioendels sekund, en hel sekund och så vidare—kräver en ny sats kristaller. Eftersom proteinberedning kan vara både långsam och dyr har provförbrukningen blivit en viktig flaskhals, särskilt vid toppmoderna anläggningar som European XFEL, där röntgenpulserna kommer i snabba tåg med megahertz-frekvenser.
Ett nytt sätt att leverera små droppar på kommando
Forskarna löste detta problem genom att omarbeta hur kristaller levereras till röntgenstrålen. I stället för en kontinuerlig vätskeström genererar de ett noggrant avståndsat tågmönster av mikroskopiska droppar, där varje droppe innehåller proteinkristaller och är separerad av en oljefas. En miniatyr 3D-utskriven enhet kombinerar två strömmar—proteinkristaller och en upplöst reaktionspartner—till små blandade volymer som sedan kläms av till droppar. Dessa droppar leds genom en gasfokuserad munstycke som bildar en smal jet anpassad för vakuumet och hastigheten hos XFEL. Avgörande är att droppproduktionen är elektriskt synkroniserad med tidpunkten för röntgenpuls-tågen så att nästan varje användbar puls träffar en droppe i stället för tom vätska. 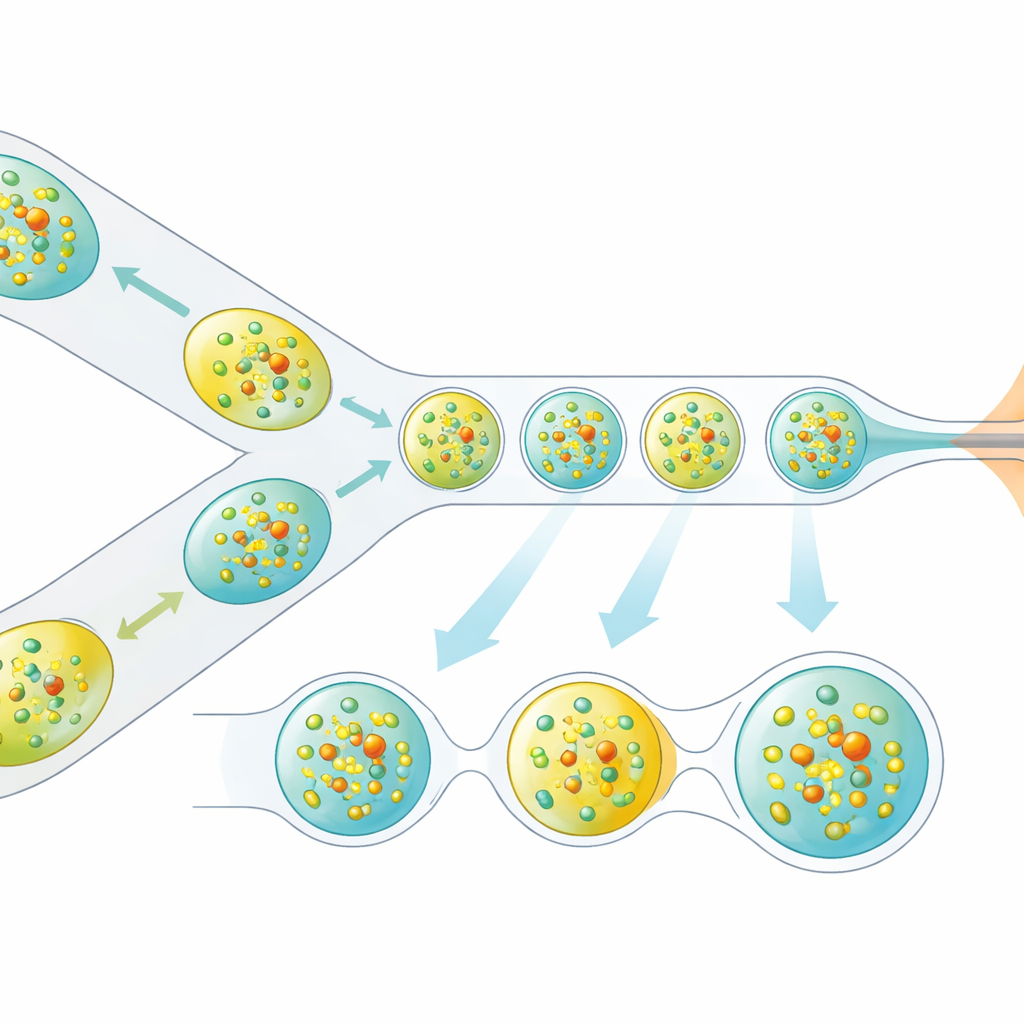
Metoden prövas på ett mänskligt enzym
För att visa att denna droppbaserade metod fungerar för verkliga biologiska frågor studerade teamet NAD(P)H:kinonreduktas 1 (NQO1), ett mänskligt enzym som deltar i cellens redoxbalans och kopplats till sjukdom. De blandade mikrokristaller av NQO1 med dess naturliga kofaktor NADH och undersökte systemet vid två tidiga tidpunkter: 0,3 sekunder och 1,2 sekunder efter blandning. Genom att analysera de resulterande röntgendiffraktionsmönstren rekonstruerade de tredimensionella strukturer för enzymet vid varje fördröjning. Trots att de använde dramatiskt mindre protein än vid konventionella kontinuerliga flödesexperiment var datakvaliteten tillräcklig för att avslöja subtila elektronäggetäthetsdrag i enzymets aktiva säten, förenliga med att NADH-molekyler börjar binda med låg ockupans.
Vad de tidiga strukturella ögonblicksbilderna visar
Strukturerna visar att inte alla aktiva säten i kristallen beter sig likadant kort efter blandningen. Vid 0,3 sekunder framträder tecken på NADH tydligt i tre av fyra aktiva säten i enhetscellen, och ofta i mer än en form, vilket tyder på att kofaktorn utforskar flera positioner innan den stabiliserar sig. Vid 1,2 sekunder har några av dessa drag skärpts till en dominerande bindningsläge, men den övergripande bilden är fortfarande en flexibel och endast delvis ockuperad interaktion. Detta ojämna, skiftande beteende stämmer överens med tidigare biokemiska bevis för att NQO1:s två partnerenheter i en dimer inte agerar helt synkront, utan uppvisar en "halv-av-sidorna"-aktivitet där den ena sidan engagerar sig först medan den andra dröjer efter. De tidsupplösta uppgifterna erbjuder därmed en tidig strukturell inblick i hur denna asymmetri ter sig i verkligt rum.
Spara prov utan att förlora vetenskapen
På ett praktiskt plan minskade den segmenterade droppmetoden proteinanvändningen med ungefär sex gånger för 0,3-sekundersmätningarna och med upp till 97 % för 1,2-sekundersexperimenten, jämfört med traditionella kontinuerliga jetstrålar under liknande förhållanden. Ändå levererade den pålitlig strukturell information vid rumstemperatur, kompatibel med European XFEL:s krävande pulsstruktur. För icke-specialister är slutsatsen att forskare nu kan se enzymer som NQO1 påbörja sitt arbete i nära realtid, samtidigt som de använder endast milligram av det värdefulla provet per tidpunkt. Det gör det mycket mer realistiskt att undersöka många reaktionstider och många olika proteiner, och bidrar i slutändan till att avslöja hur medicinskt viktiga enzymer rör sig, böjer sig och samarbetar när de utför livets kemi.
Citering: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Nyckelord: seriekristallografi, X-ray free-electron laser, droppmikrofluidik, enzymdynamik, NQO1