Clear Sky Science · sv
Onkogena PI3Kα-varianter avslöjar graderat konformationsspektra med mutationsspecifika kryptiska fickor
När en DNA-förändring inte räcker
Cancer beskrivs ofta som en sjukdom av mutationer, men den här studien visar att inte alla mutationer verkar ensamma. Forskarna undersökte ett nyckelenzym för tillväxtkontroll, PI3Kα, och fann att när två specifika DNA-förändringar förekommer tillsammans i samma genkopiera kan de pressa proteinet in i mer aktiva former än någon av förändringarna gör för sig. Det spelar roll eftersom överaktiv PI3Kα inte bara driver cancer, utan också är inblandat i godartade överväxtsyndrom och utvecklingsstörningar i hjärnan—och det hjälper till att förklara varför vissa tumörer svarar dåligt på nuvarande läkemedel.
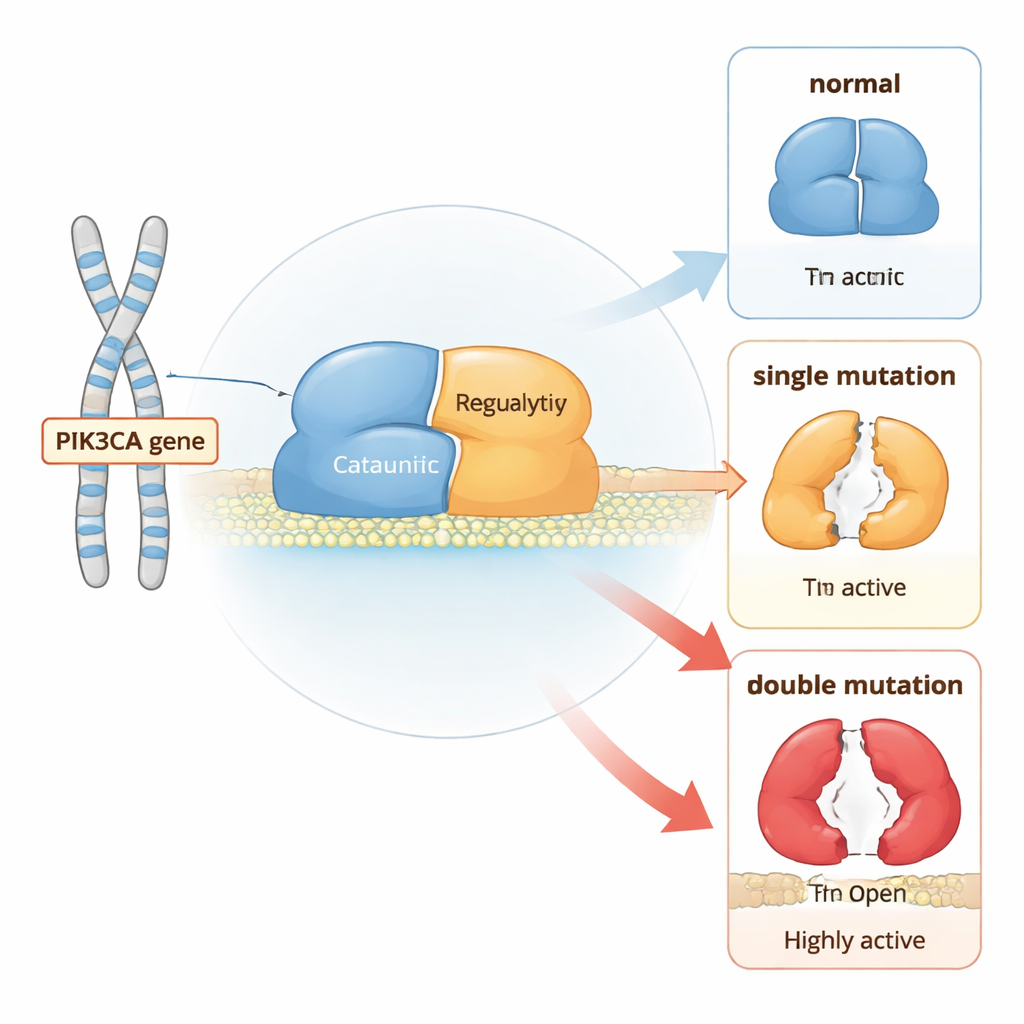
En molekylär strömbrytare för celltillväxt
PI3Kα är ett tvådelat protein som sitter vid cellmembranet och förmedlar tillväxtsignaler. Under normala förhållanden ligger det mestadels i ett ”av”-läge tills receptorer på cellytan aktiveras. Då flyttar PI3Kα till membranet och omvandlar ett lipid kallat PIP2 till PIP3, vilket signalerar åt cellen att växa och dela sig. För att förhindra okontrollerad tillväxt fungerar flera delar av proteinet som inbyggda bromsar: ett område håller fast den katalytiska kärnan, en annan håller en flexibel aktiveringsslinga nära, och en partnerunderenhet hjälper till att hålla hela komplexet i schack.
Hur enkla och dubbla mutationer tippar balansen
Med långa, atomnivåbaserade datorsimuleringar jämförde författarna normal PI3Kα med varianter som bar antingen enstaka ”hotspot”-cancermutationer eller kombinationer av en hotspot med en svagare mutation i samma molekyl. De fann att varje mutation ändrar hur ofta proteinet antar mer öppna, aktiva former, men dubbelmutanter förskjuter balansen mycket mer än enkla. Särskilt samarbetar vissa mutationspar för att luckra upp kontakterna som håller en reglerande del (kallad nSH2) på plats och för att förflytta ett annat segment (iSH2) bort från dess dockningsställe. Denna samordnade rörelse låser upp den katalytiska kärnan, vilket gör det lättare för proteinet att röra sig till membranet och börja signalera.
Hjälper substratet nå reaktionsstället
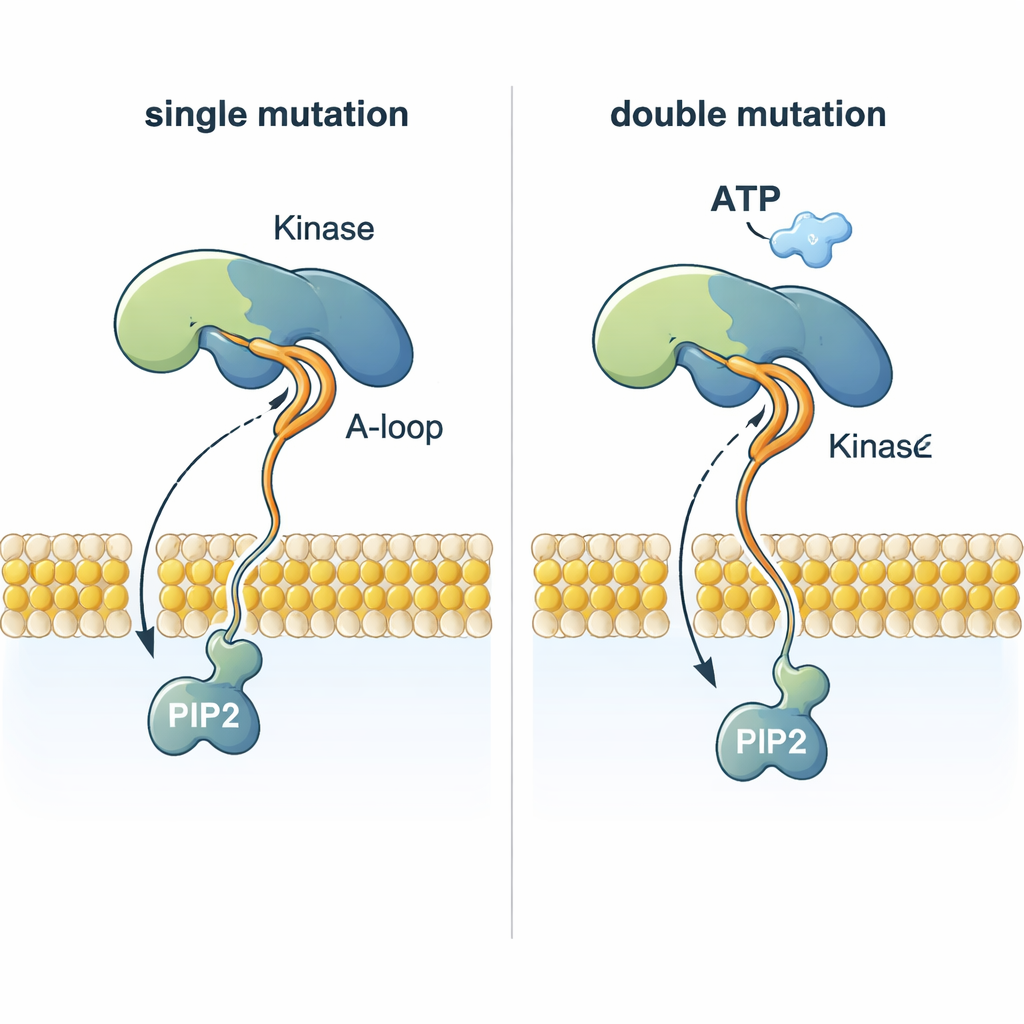
Ett slående pussel är hur PI3Kα kan överföra en fosfatgrupp från ATP—som ligger nästan 2 nanometer ovanför membranet—till PIP2, som är inbäddad i membranet. Simuleringarna visar att vissa mutationer formar om en flexibel aktiveringsslinga så att ett mycket positivt laddat streck sträcker sig mot membranet. Denna slinga kan greppa den negativt laddade huvudet på PIP2, dra ut det ur lipidlagret och styra det upp mot ATP. Dubbelmutanter som kombinerar en membranankrande mutation med en som ändrar denna slinga koordinerar PIP2 mycket effektivare än normal PI3Kα eller enkla mutanter, vilket ger en strukturell förklaring till varför tumörer med två PI3Kα-mutationer kan vara särskilt aggressiva.
Dolda läkemedelsställen avslöjade av rörelse
Eftersom PI3Kα är stort och flexibelt har ett enskilt läkemedel riktat mot dess aktiva site ofta svårt att fungera över alla mutantformer och kan orsaka biverkningar såsom allvarliga förändringar i blodsockret. Genom att följa hur proteinet andas och böjer sig över tid upptäckte forskarna ”kryptiska” fickor—tillfälliga spår som öppnas bara i vissa mutanta former och som är osynliga i statiska kristallstrukturer. Dessa fickor dyker upp på mutationsspecifika platser, till exempel i närheten av regioner som rör sig kraftigast i särskilda dubbelmutanter. Det antyder att noggrant utformade allosteriska läkemedel, som binder bortom den aktiva ytan, kan skräddarsys för att låsa individuella mutantvarianter tillbaka i säkrare, mindre aktiva konformationer.
Mot smartare kombinationsbehandlingar
Sammanfattningsvis stöder arbetet en ”en-två-slag”-syn på cancergenetik: en stark hotspot-mutation plus en svagare partner i samma PI3Kα-molekyl kan skapa ett graderat spektrum av mer aktiva former, ofta kopplade till allvarligare kliniska utfall. För terapi menar författarna att istället för att förlita sig på en enskild hämmare kan det vara mer effektivt att kombinera läkemedel som riktar olika fickor—en vid den aktiva ytan och en eller flera allosteriska platser som endast finns i specifika mutanter. Sådana kombinationer skulle i princip kunna dämpa PI3Kα-aktiviteten mer precist, minska toxiska biverkningar och bättre anpassa behandlingen till det exakta mutationsmönster som finns i en patients tumör.
Citering: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Nyckelord: PI3K alfa, onkogena mutationer, allosteriska hämmare, molekyldynamik, signaltransduktion