Clear Sky Science · sv
Sekvens- och längdskaleberoende dynamik i biokondensat av starkt laddade oordnade proteiner
Varför små proteindroppar spelar roll
Inuti våra celler sker många viktiga reaktioner i mjuka, droppliknande strukturer utan omgivande membran. Dessa ”biomolekylära kondensat” beter sig som små flytande compartment och byggs ofta upp av flexibla, starkt laddade proteiner. Experiment har visat att molekyler inne i vissa av dessa droppar kan röra sig förvånansvärt snabbt, trots att dropparna som helhet kan vara ganska trögflytande och klibbiga. Denna artikel ställer en enkel men viktig fråga: hur styr den exakta ordningen av positiva och negativa laddningar längs dessa proteiner hur snabbt saker rör sig inne i sådana droppar?
Bygga droppar av flexibla laddade kedjor
Författarna fokuserar på intrinsiskt oordnade proteiner—långa, flexibla kedjor som inte viker sig till styva former. Många av dessa kedjor bär både positiva och negativa laddningar, ordnade i olika mönster längs kedjan. Med storskaliga datorsimuleringar skapade teamet modell-droppar bestående av många kopior av sådana proteiner, tillsammans med vatten och små joner, för att efterlikna den trånga inre miljön i verkliga kondensat. De ändrade systematiskt hur ”blockigt” laddningsmönstret var, från sekvenser där positiva och negativa laddningar alternerar till sekvenser där alla positiva laddningar grupperas ihop och alla negativa bildar ett separat block.
Vatteninnehåll och fluidflöde formar rörelse
Simuleringarna visade att dessa droppar fortfarande kan bete sig som riktiga vätskor med ett mycket högt vatteninnehåll—mellan ungefär 55 % och 84 %, beroende på laddningsmönstret. Denna mängd vatten innebär att fluidflöde, eller hydrodynamik, inte är helt undertryckt såsom många teorier för täta polymerlösningar skulle föreslå. Genom att följa hur proteindelar vandrar över tiden fann författarna rörelsemönster typiska för kedjor vars rörelse understöds av omgivande vätska, snarare än enbart fördröjs av friktion. Detta hydrodynamiska inflytande kvarstår upp till och till och med bortom storleken av en hel proteinkedja, särskilt i droppar bildade av sekvenser med mer blandade laddningar och därmed mer vatten.
Lokala laddningsmönster styr mikroskopisk flexibilitet
Närmare granskning visade att författarna undersökte hur korta sektioner av varje kedja slappnar av och omarrangerar sig inne i droppen. Olika delar av samma protein, innehållande samma antal byggstenar, kunde röra sig i mycket olika takt beroende på deras lokala blandning av positiva och negativa laddningar. Sektioner som var mer balanserade i laddning slappnade av snabbare, medan partier dominerade av en laddningstyp rörde sig trögare. Överraskande nog kvarstod dessa skillnader starkt trots att enkla screeningsargument skulle förutsäga att elektrostatisk påverkan borde vara korträckviddig i så salta, trånga förhållanden. Arbetet visar att det faktum att laddningarna är bundna längs en kedja bevarar långräckviddiga elektriska korrelationer som starkt påverkar lokal rörelse.
Viskositet beror på storleken av det du undersöker
Teamet frågade sedan hur ”tjock” dessa droppar känns vid olika längdskalor. Med en metod som kopplar små vågor i vätskans rörelsemängd till dess motstånd mot flöde beräknade de en viskositet som beror på undersökningslängden. För alla sekvenser verkar vätskan tunnare när den undersöks i mycket små skalor och tjockare när den undersöks över hela droppen. Detta storleksberoende är särskilt dramatiskt för de blockiga laddningssekvenserna: för det mest segregerade mönstret är bulkviskositeten mer än tjugo gånger högre än den lokala, monomer-nivå viskositeten. I kontrast visar droppar från välblandade sekvenser ett mycket mindre gap. Sammantaget ökar bulkviskositeten brant med proteinkoncentrationen, i linje med hur täta neutrala polymerlösningar beter sig, trots att proteinerna själva är starkt laddade.
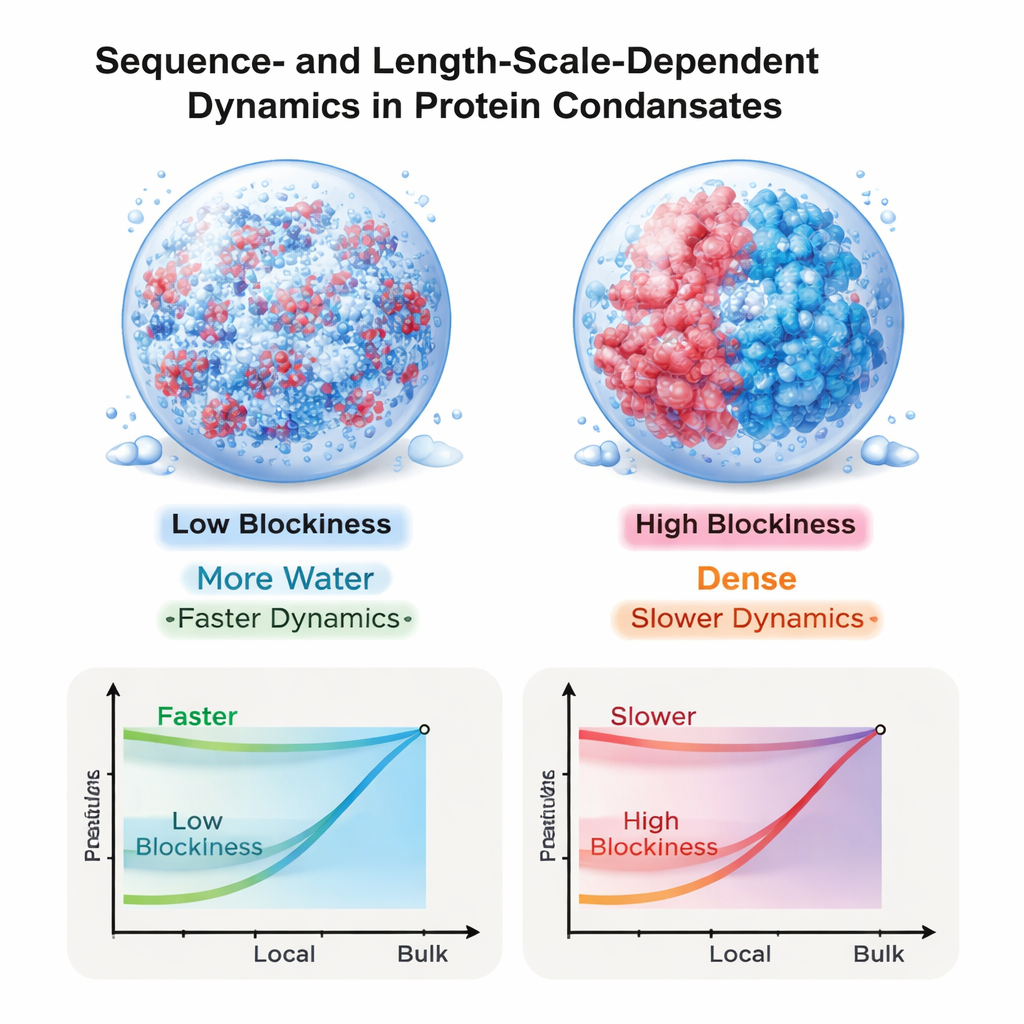
Koppla simuleringar till förbryllande experiment
Dessa resultat hjälper till att lösa ett uppenbart paradoxalt fynd från nyligen genomförda experiment: hur kan små molekyler och proteindelar diffundera så snabbt inne i kondensat som, mätt som helhet, verkar extremt viskösa? Svaret som framträder från detta arbete är att både vattnets flöde och långräckviddiga elektriska interaktioner förblir viktiga i dessa droppar, och deras påverkan styrs noggrant av hur laddningarna är ordnade längs varje kedja. Sekvenser med blockiga laddningsmönster ger täta, mycket viskösa droppar som ändå förblir relativt flytande på mikroskopiska skalor, medan mer blandade sekvenser ger genomgående mer rörliga miljöer. Genom att visa att laddningssekvensen kan finjustera rörelse olika vid olika längdskalor erbjuder studien en designprincip för att konstruera syntetiska proteinbaserade material och belyser hur celler kan programmera kondensatbeteende genom den detaljerade sekvensen hos sina oordnade proteiner.
Citering: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Nyckelord: biomolekylära kondensat, intrinsiskt oordnade proteiner, ladningsmönster, proteindynamik, viskositet