Clear Sky Science · sv
Utveckling av en fyrfaldigt konjugerad kol-dot-nanomodell för riktad gliombehandling
Nytt hopp för svårbehandlade hjärntumörer
Höggradiga hjärntumörer som glioblastom är bland de svåraste cancerformerna att behandla. Många läkemedel som fungerar i andra delar av kroppen kan antingen inte passera hjärnans skyddande blod-hjärnbarriär eller skadar frisk vävnad på vägen. I denna studie beskrivs en laboratoriumkonstruerad ”smart” nanopartikel som syftar till att smyga in i hjärntumörer mer precist, bära en kraftfull läkemedelskombination och frigöra den direkt inne i tumörcellernas cellkärnor, där den kan orsaka mest skada på cancern samtidigt som normala celler skonas.
En liten leveransbil byggd av kol
I centrum för den nya ansatsen står koldots—nanometerstora partiklar gjorda av kol som är billiga att framställa, blandas väl med vatten och lyser under vissa typer av ljus. Eftersom deras ytor är rika på kemiska fästen kan de dekoreras med flera biologiska komponenter samtidigt. I detta arbete skapade forskarna en ”fyrfaldigt konjugerad” nanomodell: varje koldot kopplades kemiskt, i en enda satuppställning, till två olika riktande peptider och två anticancermolekyler. Denna modulära design förvandlar varje dot till en liten leveransbil som kan känna igen tumörceller, passera cellulära barriärer och föra läkemedel till rätt intracellulära adress.
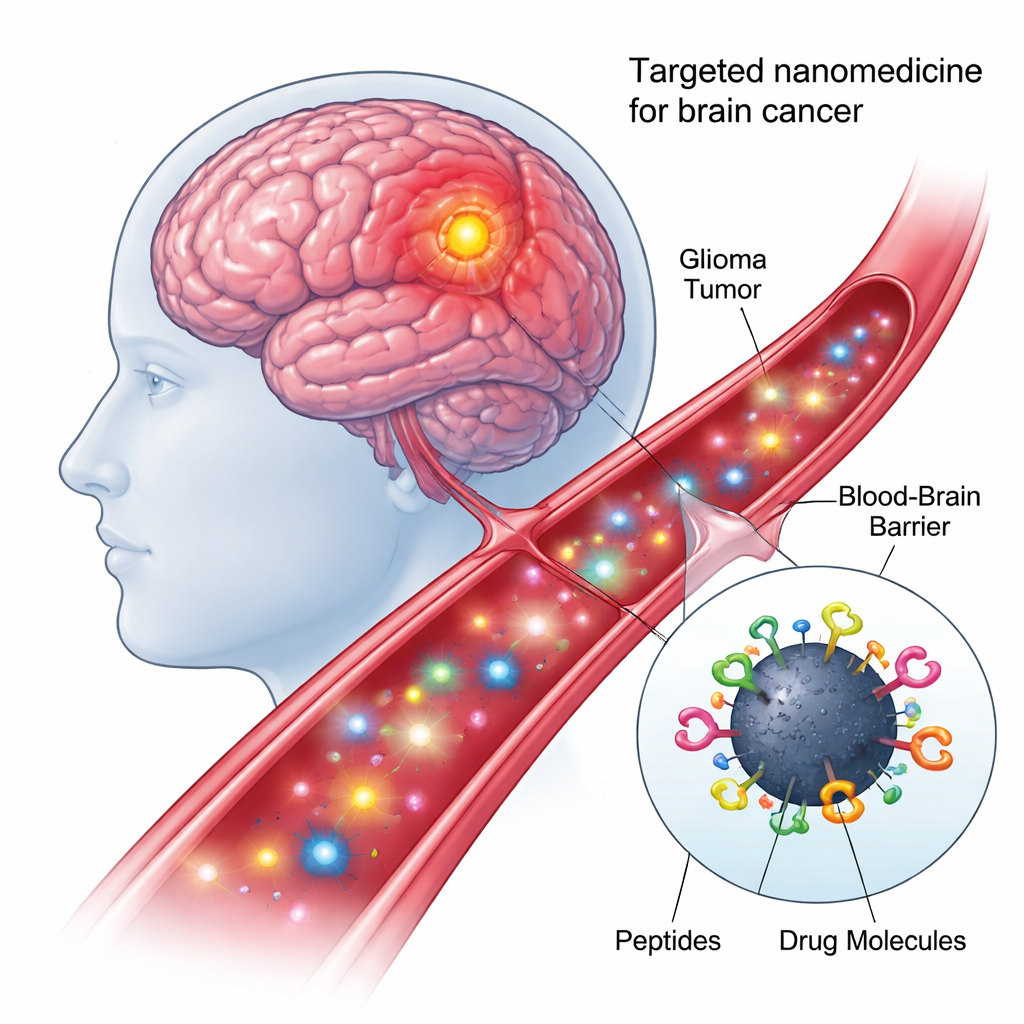
Hitta och gå in i rätt hjärnceller
Den första peptiden på nanopartikeln, kallad shPep-1, är utformad för att känna igen en receptor som heter IL13Rα2. Denna receptor finns i höga nivåer på många aggressiva hjärntumörer—inklusive vuxen- och pediatriskt glioblastom samt diffus intrinsisk pontin gliom—men verkar bara svagt uttryckt på normala hjärnceller. Genom att binda IL13Rα2 hjälper shPep-1 koldotsen att rikta in sig på tumörceller och tas upp via receptor-medierad endocytos. Den andra, längre peptiden, lnPep-1, innehåller en signal för nukleär lokalisering: en kort sekvens som hjälper lasten att passera kärnmembranet och nå cellens kontrollcenter, där DNA lagras. Tillsammans ger dessa två peptider nanopartikeln både tumörpreferens och förmågan att nå kärnan när den väl är inne.
Leverera en koordinerad läkemedelsattack
Den terapeutiska lasten består av två små molekyler. Den första är epirubicin, ett välkänt cytostatikum som dödar cancerceller genom att lägga sig in i DNA och blockera enzymer som behövs för att reparera dubbelsträngsbrott. Den andra är en metabolit kallad 5-aminoimidazol-4-karboxamid (AIC), som bildas från hjärntumörläkemedlet temozolomid vid fysiologiskt pH. I tidigare arbete visade samma grupp att kombinationen av epirubicin och AIC på en koldot ökade cancercelldöd jämfört med vardera läkemedlet för sig. I den nya designen levereras båda samtidigt på den dual-peptidnanopartikeln, med målet att uppnå en synergistisk effekt direkt i tumörcellens kärna.
Potent i tumörceller, mildare mot normala celler
För att testa hur väl nanomodellen fungerade exponerade teamet flera cellinjer från höggradig gliom—vuxet glioblastom, pediatriskt glioblastom och en modell för diffus intrinsisk pontin gliom—för de fyrfaldigt konjugerade koldotsen. Även vid mycket låga koncentrationer (ända ner till 50 nanomolar) sjönk tumörcellernas livsduglighet till ungefär hälften jämfört med obehandlade kontroller, och vid högre doser dödade alla testade konjugat de flesta tumörcellerna. Viktigt är att den fyrfaldiga nanomodellen överträffade enklare ”envpeptid”-versioner, trots att den totalt bar mindre epirubicin. När den testades på icke-cancerösa vaskulära glattmuskelceller var den betydligt mindre toxisk: dessa celler krävde ungefär 25–40 gånger mer nanopartikel för att se en liknande minskning i livsduglighet, vilket tyder på ett användbart säkerhetsfönster drivet av tumörtargeting snarare än hög dosering.
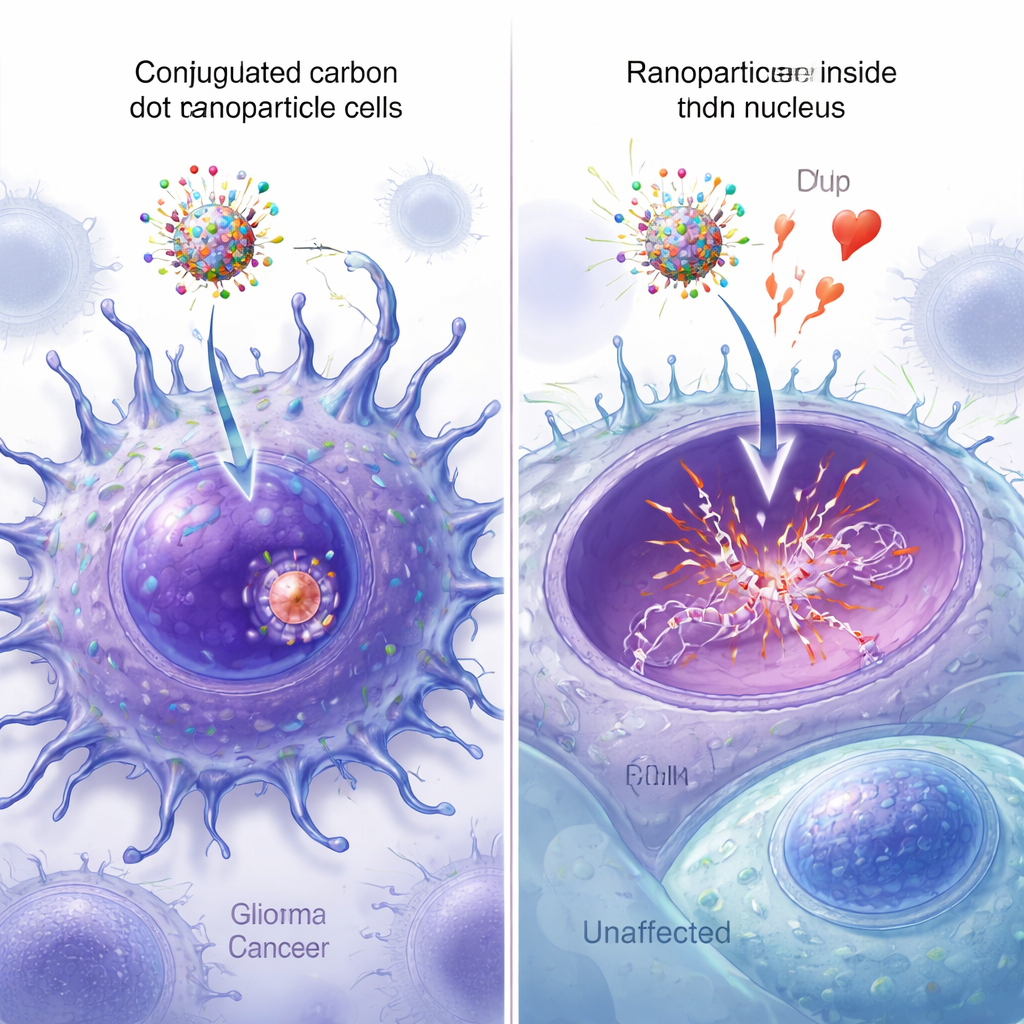
Se nanopartiklarna nå kärnan
Fluorescerande versioner av nanopartiklarna gjorde det möjligt för forskarna att följa hur väl varje design trängde in i celler och nådde kärnan. Under mikroskop visade koldots utrustade med båda peptiderna den starkaste signalen spridd genom cancercellerna, med tydlig överlappning mellan den gröna nanopartikel-fluorescensen och blå nukleär färgning. Kvantitativ bildanalys bekräftade att dual-peptidpartiklarna hade högst nukleär kolokalisering, betydligt mer än partiklar som bar endast en peptid eller ingen. Vidare verifierade spektroskopi, masspektrometri och atomkraftmikroskopi att alla fyra komponenter framgångsrikt sattes fast på koldotsen och måttligt ökade deras storlek, utan att störa epirubicins viktiga DNA-bindande funktion.
Vad detta kan betyda för framtida vård av hjärncancer
För patienter är dessa fynd fortfarande en tidig, cellkulturbaserad demonstration snarare än en färdig behandling. Ändå visar de på ett lovande koncept: en liten, stabil och relativt lättproducerad kolbaserad nanopartikel som snabbt kan skräddarsys med riktande peptider och läkemedelskombinationer. Genom att styra läkemedel specifikt till tumörceller som överproducerar IL13Rα2 och koncentrera dem i kärnan, skulle sådana nanomediciner en dag kunna möjliggöra lägre doser, färre biverkningar och mer personligt anpassade behandlingsstrategier för mycket dödliga hjärntumörer som glioblastom och diffus intrinsisk pontin gliom.
Citering: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Nyckelord: glioblastom, nanomedicin, koldots, riktad läkemedelsleverans, hjärntumörer