Clear Sky Science · sv
En generaliserbar analys för intracellulär ackumulering för att profilera cytosolisk läkemedelsleverans i däggdjursceller
Varför det spelar roll att få läkemedel in i celler
Många av dagens mest lovande läkemedel — små molekyler, korta proteinfragment kallade peptider och fullstora proteiner — är utformade för att verka på mål inuti våra celler. Men cellmembranet är en hård säkerhetsgrind. Ett läkemedel kan fastna på cellens utsida eller hamna instängt i inre blåsor kallade endosomer och ändå aldrig nå den vattniga insidan, cytosolen, där många mål finns. Denna artikel beskriver ett nytt laboratorietest, kallat CHAMP-analysen, som berättar för forskare inte bara om en molekyl tar sig in i en cell, utan om den verkligen når cytosolen, där den kan göra sitt jobb.
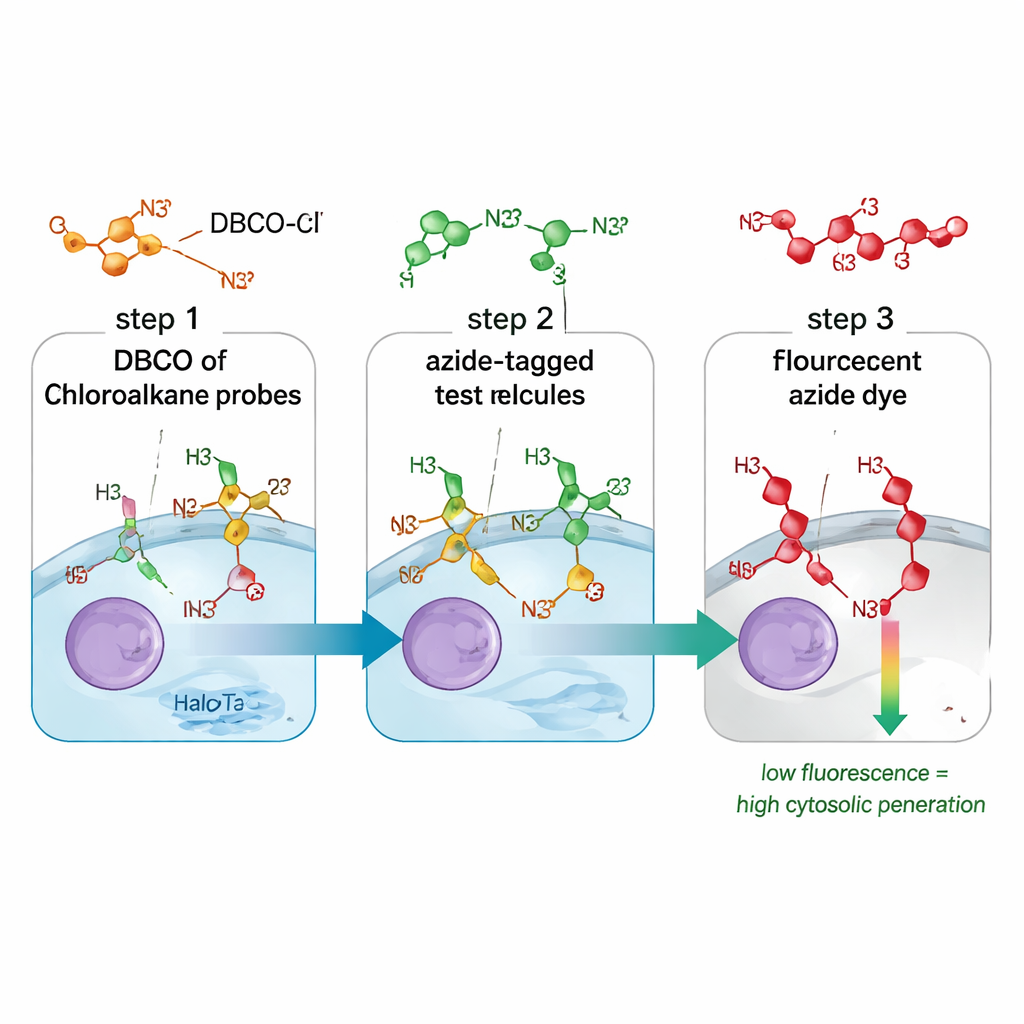
Ett nytt sätt att följa läkemedelsintrång
Traditionella metoder för att mäta upptag av läkemedel suddar ofta ihop molekyler som bara rör vid cellytan, sitter i endosomer eller faktiskt når cytosolen. De kan också förlita sig på skrymmande fluorescerande etiketter som förändrar hur en molekyl beter sig. CHAMP-analysen löser båda problemen genom att kombinera ett litet kemiskt ”handtag” kallat en azid med en proteinmarkör vid namn HaloTag, som är konstruerad för att flyta fritt i cytosolen i odlade humana celler. Först behandlas cellerna med en länkarmolekyl som fäster DBCO, en spänd form av alkyn, på HaloTag. Därefter tillsätter forskarna den testade föreningen, som bär den lilla azid-taggen. Endast om den föreningen korsar cellmembranet in i cytosolen kan aziden och DBCO klicka ihop i en mycket selektiv kemisk reaktion. En slutlig fluorescerande azidfärg avslöjar hur många DBCO‑platser som är kvar: svaga celler betyder att testföreningen tog sig in och ockuperade de flesta platser; starkt lysande celler betyder dålig cytosolisk åtkomst.
Från koncept till fungerande analys
Författarna bekräftade först att HaloTag producerades korrekt och var lokaliserad i cytosolen i humana HeLa‑celler genom att använda en standard chloroalkanefärg och bildframställning. De optimerade sedan varje steg i CHAMP: hur mycket DBCO‑länkare som skulle tillsättas, hur länge man skulle inkubera, och vilken fluorescerande azidfärg som gav en stark, specifik signal utan att skada cellerna. Flödescytometri — ett instrument som mäter fluorescens i tusentals individuella celler — visade att analysen var snabb, robust och justerbar. Avgörande visade teamet att fluorescensen verkligen härrörde från specifika reaktioner vid HaloTag‑platser snarare än från färger som ospecifikt fastnade på cellkomponenter, och att den lilla azid‑taggen inte märkbart störde hur molekyler tog sig in i cellerna.
Vad analysen avslöjar om små läkemedel och peptider
Med CHAMP i handen utsatte forskarna den för hundratals azidmärkta små molekyler och varierade systematiskt egenskaper som laddning, storlek och flexibilitet. De observerade till exempel att omvandlingen av en negativt laddad karboxylsyra till en neutral amid ökade cytosolisk ackumulering, och att graden och positionen för kvävemetylering förändrade hur väl föreningar tog sig in. Genom att jämföra reaktioner på fria pärlor mot levande celler kunde de skilja på inneboende kemisk reaktivitet och barriären som själva membranet utgör. Teamet tillämpade också CHAMP på en panel vanliga antibiotika och visade att vissa nådde cytosolen mycket bättre än andra — viktig information vid behandling av bakterier som gömmer sig inne i värdceller.
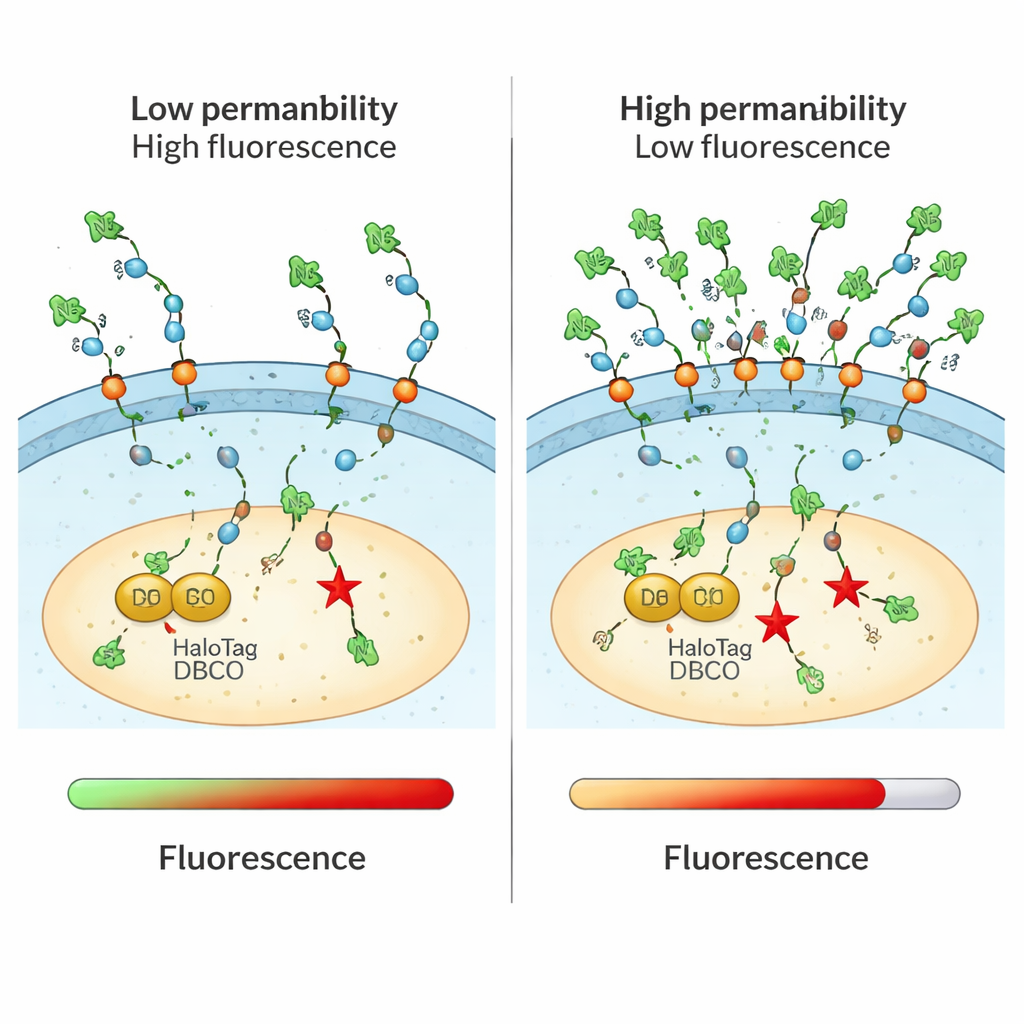
Superladdade peptider och proteiner som korsar barriären
Analysen var särskilt kraftfull för att studera större, starkt laddade molekyler som är svåra att följa med andra metoder. Författarna undersökte cellpenetrerande peptider uppbyggda av flera argininrester och bekräftade en tydlig trend: längre, mer positivt laddade kedjor levererade mer material till cytosolen, upp till en viss gräns. De undersökte hur omvänd handighet (stereokemi) hos vissa aminosyror påverkade inträde och fann att spegelbildsvarianter ibland ackumulerade bättre, vilket antyder subtila kirala interaktioner med membranet. CHAMP visade också att ”superladdade” proteiner — konstruerade för att bära många positiva laddningar — kunde nå cytosolen mer effektivt än sina normala motsvarigheter, vilket stöder deras potential som bärare för stora terapeutiska laster.
Designregler för framtida intracellulära läkemedel
Genom att systematiskt testa små molekyler, peptider, makrocykliska peptider och modifierade ryggrader avslöjade studien generella designprinciper. Makrocykliska peptider, där ryggraden är sluten i en ring, tenderade att nå cytosolen lättare än flexibla linjära varianter. Omsorgsfullt placerade N‑metylgrupper på peptidryggraden ökade inträdet måttligt, men för många kunde vara kontraproduktiva. Dessa struktur–permeations‑relationer, avslöjade med en enda standardiserad analys, ger praktisk vägledning för kemister som vill utforma molekyler som inte bara binder sina mål utan faktiskt kan nå dem inne i cellerna.
Hur detta hjälper läkemedelsutveckling
Enkelt uttryckt är CHAMP‑analysen en finjusterad trafikräknare vid cellens ytterdörr och inre korridor. Den berättar för forskare vilka experimentella läkemedel som verkligen tar sig förbi membranet och in i cytosolen, utan att bedragas av molekyler som sitter fast på ytan eller i inre kompartment. Eftersom den fungerar med ett brett spektrum av molekylära former och storlekar och använder endast en liten azid‑tag, kan CHAMP integreras i höggenomströmningens upptäcktsprocesser. Med tiden bör detta påskynda designen av mer effektiva behandlingar för sjukdomar där de viktigaste målen är inlåsta inne i våra celler.
Citering: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Nyckelord: intracellulär läkemedelsleverans, cellmembranpermeabilitet, cytosolisk ackumulering, cellgenomträngande peptider, bioortogonal click-kemi