Clear Sky Science · sv
Första kristallstrukturen av ett adukt bildat vid reaktion mellan en vanadiumnförening och mänskligt serumtransferrin
Varför ett blodprotein och ett metall läkemedel spelar roll
Många experimentella läkemedel innehåller metallatomer som kan hjälpa till att behandla sjukdomar från diabetes till cancer. Men när dessa metallbaserade läkemedel väl kommer in i blodomloppet måste de fästa sig vid kroppens naturliga transportproteiner. Denna studie undersöker hur ett sådant protein, mänskligt serumtransferrin—huvudbäraren av järn i vårt blod—interagerar med en lovande vanadiumnförening och belyser hur metallläkemedel transporteras i kroppen och hur de kan finjusteras för säkrare och mer effektiva behandlingar.
Kroppens järnbudbärare och dess sidojobb
Transferrin är ett 80 kilodalton stort protein vars huvudsakliga uppgift är att fånga upp järn och leverera det till celler som behöver det. Det har två ”flikar”, vardera kapabel att binda en järnjon, och ändrar form beroende på om järn är närvarande. När järn binder stänger en flik; utan järn förblir den öppen. Specialiserade receptorer på cellytor känner igen dessa järnlastade former och internaliserar dem, vilket gör transferrin centralt för järnbalans och cellhälsa. Transferrin kan dock också binda andra metaller, inklusive sådana från medicinska behandlingar, vilket innebär att det kan påverka var metallbaserade läkemedel färdas och hur de verkar.
En formsnapshot av vanadium på transferrin
Forskarlaget fokuserade på en välstuderad vanadiumkandidat, bis(acetylacetonato)oxovanadium(IV), ofta skriven som [VIVO(acac)₂]. Tidigare arbete visade att denna förening, eller arter härledda från den i vatten, kan fästa vid transferrin, men ingen hade sett exakt hur. Genom röntgenkristallografi erhöll teamet högupplösta strukturer av transferrin som bär järn endast i dess C-terminala flik (”FeC”-formen), både före och efter exponering för vanadiumläkemedlet. I de vanadiumbehandlade kristallerna observerade de inte det ursprungliga läkemedlet, utan en omvandlad vanadium‑oxigen‑kluster bunden i den järnfria N-terminala fliken. Detta gav dem den första direkta strukturella bilden av en vanadiumfragment fäst vid mänskligt transferrin.
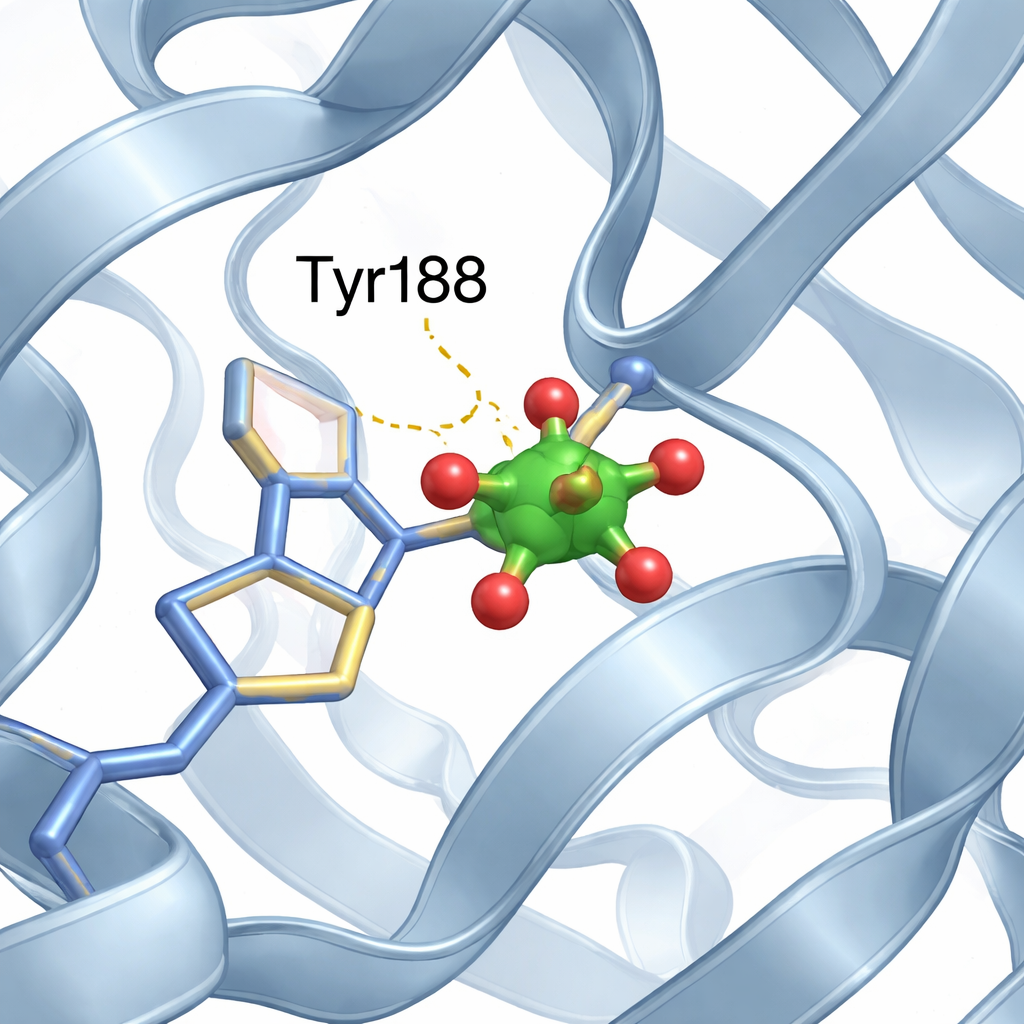
En liten vanadiumkluster hittar en nisch
I N‑flikens järnsite identifierade teamet en liten kluster bestående av två vanadiumatomer och syreatomer, bäst beskriven som en modifierad ”divanadat”-enhet. En av klustrets syrepositioner övertas av syret från en specifik aminosyra, tyrosin 188 (Tyr188), vilket bildar en direkt bindning mellan protein och metallklustret. Ytterligare milda interaktioner, såsom vätebindningar från närliggande proteindelar, stabiliserar klustret ytterligare på plats. Viktigt är att trots denna nya metallgäst som upptar ett järnbindningsfack, behåller proteinet sin vanliga öppna N‑flik och stängda C‑flikarrangemang, nästan identiskt med strukturen utan vanadium.
Hur transferrin omformar vanadiumkemin
I lösning vid det pH och den koncentration som användes för kristallisering är den specifika två‑vanadiumarten som ses i kristallen normalt bara en minoritetsform; större vanadium‑oxigen‑kluster tenderar att dominera. Spektroskopiska mätningar och teoretiska specieringsberäkningar tyder på att det ursprungliga vanadiumläkemedlet långsamt oxiderar och sönderfaller i vatten, vilket producerar enkla vanadatjoner som sedan monteras till en mängd olika kluster. Kristallstrukturen indikerar att transferrin selektivt stabiliserar detta lilla divanadatliknande fragment framför de större klustren—i praktiken ”väljer” en kemisk form ur en tät lösningsblandning genom att erbjuda en välpassande bindningsplats vid Tyr188 och ett stödjande nätverk av vätebindningar.
Behåller handslaget med cellreceptorn
Eftersom transferrin måste binda en receptor på cellytor för att leverera järn frågade forskarna om fästningen av denna vanadiumkluster skulle störa detta avgörande handslag. Med hjälp av icke-denaturerande gelelektrofores och en känslig teknik kallad biolagerinterferometri mätte de hur väl vanadiumbehandlat transferrin band till transferrinreceptorn jämfört med den obehandlade järn‑endast formen. Båda uppträdde nästan identiskt, med mycket stark bindning i låga nanomolära området. Detta bekräftar att vanadiumklustret, medan det ligger inbäddat i N‑fliken, inte ändrar transferrins form där receptorn interagerar i någon nämnvärd grad och därför inte bör hindra proteinet från att kännas igen av celler.
Vad detta betyder för metallbaserade läkemedel
För icke‑specialister är slutsatsen att denna studie ger ett molekylärt ögonblicksbild av hur en vanadiumläkemedelsderivat fäster vid kroppens huvudjärnbudbärare utan att störa dess normala funktion. Transferrin kan fånga ett specifikt litet vanadium‑oxigenkluster i ett järnsite, samtidigt som proteinets övergripande form och dess förmåga att binda sin receptor förblir i stort sett oförändrade. Detta hjälper till att förklara hur vanadiumläkemedel kan cirkulera fästa vid transferrin och framhäver att olika proteiner kan föredra olika storlekar av vanadiumkluster. Sådana insikter är avgörande för att utforma smartare metallbaserade terapier vars beteende i blodomloppet—vilka former de antar, vart de går och hur länge de kvarstår—kan förutses och kontrolleras.
Citering: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Nyckelord: vanadiumläkemedel, mänskligt serumtransferrin, metallbaserade terapier, protein–metallbindning, strukturell biologi