Clear Sky Science · sv
Laktam möjliggör fjärrförflyttningar av boronat till C═N-bindningar
En ny genväg för att bygga läkemedelslika molekyler
Kemister söker ständigt snabbare och renare sätt att bygga de komplexa molekyler som finns i läkemedel och avancerade material. Denna studie presenterar en smart genväg som låter en vanlig ringsluten struktur, kallad laktam, temporärt styra en reaktion för att sedan tyst dra sig undan—vilket gör det möjligt att omvandla enkla, lättillgängliga utgångsmaterial till värdefulla byggstenar för läkemedel utan att använda dyra metaller eller invecklade förberedelsesteg.
Att förvandla en tyst hjälpare till en tillfällig vägvisare
Många moderna läkemedel och funktionella material förlitar sig på reaktioner med boronsyror, en grupp borinnehållande föreningar uppskattade för sin tillförlitlighet och milda beteende. Traditionellt, för att få boronsyror att bilda nya bindningar till kol–kväve-dubbelbindningar (C=N), måste kemister förinstallera speciella ”styrgrupper” på utgångsmaterialet. Dessa grupper fungerar som handtag som styr reaktionen men kostar extra tid, pengar och steg—och fungerar ofta bara med mycket reaktiva partners. Författarna insåg att laktamer, ringslutna släktingar till den välkända amidbindningen i proteiner, skulle kunna fungera som inbyggda, temporära vägvisare. Genom att koordinera till boratomen hjälper laktamets syre till att bilda ett välordnat, fyrkoordinerat borcentrum som kan omfördela en fäst fragment till en avlägsen position längs molekylen, vilket ställer upp nya kol–kväve-bindningar utan någon permanent styrgrupp.
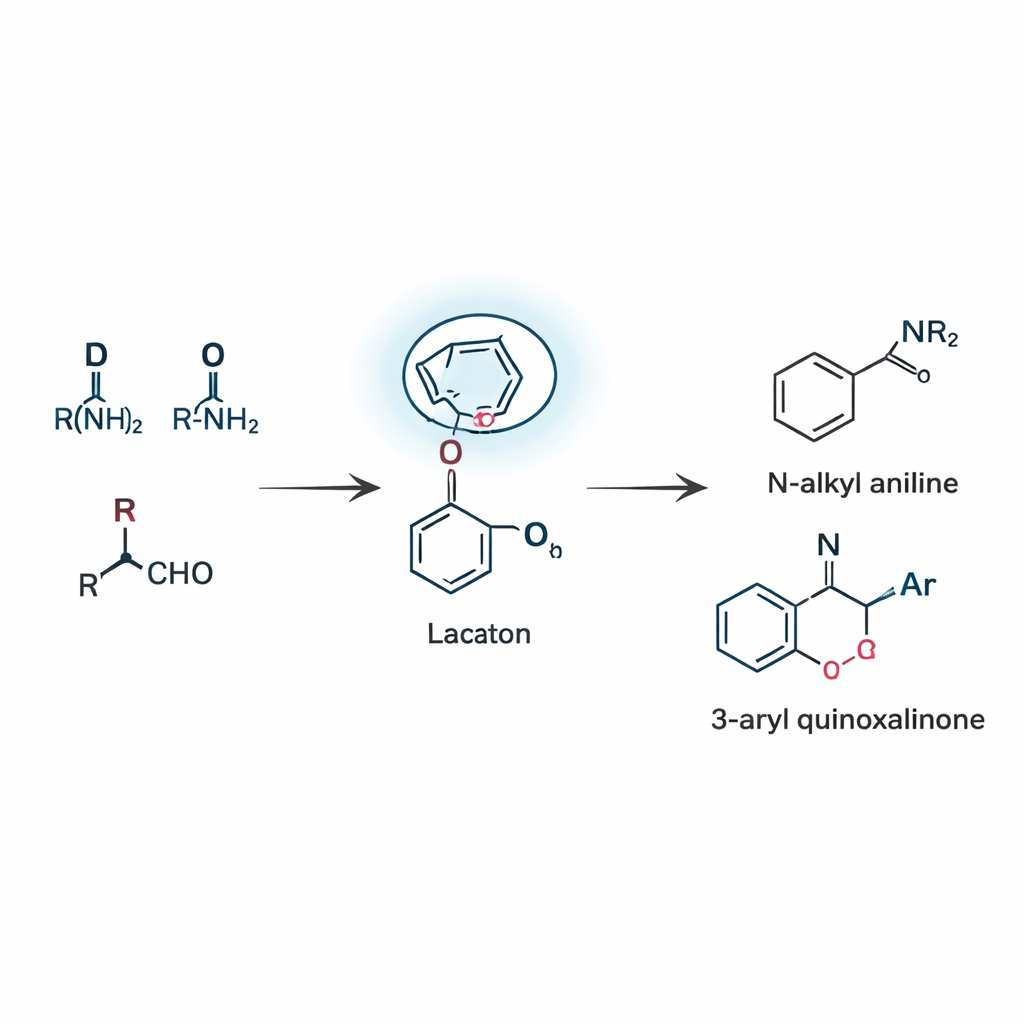
Att bygga två familjer av användbara produkter i en strategi
Med detta koncept utvecklade teamet två närbesläktade reaktioner som båda förlitar sig på denna laktamstyrda omflyttning, känd som en fjärr boronat-omläggning. I den första förenas tre enkla delar—en aldehyd, en amin och en boronsyra—för att bilda N‑alkyl aniliner, ett kärnmotiv som återfinns i otaliga läkemedelskandidater och färgämnen. Reaktionen går via en sällsynt 1,5‑förskjutning, där en arylgrupp på boron hoppar över fem atomer för att nå C=N‑bindningen. Genom att noggrant stämma av katalysator, lösningsmedel och temperatur uppnådde forskarna respektabla utbyten och visade att många olika substituenter, inklusive halogener, alkylgrupper och heterocykliska enheter, tolereras. I den andra reaktionsläget tillämpas samma vägledande idé på kinoxalinoner, en klass kväverika ringar vanliga inom läkemedelskemi. Här används ingen tillsatt metalkatalysator alls och ändå levererar metoden effektivt 3‑aryl kinoxalinoner, tack vare laktamets förmåga att engagera boron och stabilisera den viktiga mellanprodukten.
Miljövänliga villkor och sent stadie-redigering av läkemedel
Förutom att visa på ett brett tillämpningsområde visar författarna att strategin är praktisk för verkliga molekyler. Eftersom 1,4‑omläggningen på kinoxalinonerna sker under metallfria förhållanden i ett specialiserat alkoholiskt lösningsmedel undviks behovet av dyra eller giftiga övergångsmetaller. Teamet tillämpade metoden på komplexa fragment härledda från marknadsförda läkemedel som ibuprofen och andra terapier som innehåller kinoxalinone-ramverket. I varje fall installerade reaktionen nya arylgrupper på en specifik position utan att störa andra känsliga funktioner. Denna typ av ”late‑stage‑funktionalisering” låter kemister snabbt dekorera befintliga läkemedelskärnor med nya sidokedjor, vilket påskyndar sökandet efter förbättrad potens, säkerhet eller fysikaliska egenskaper.
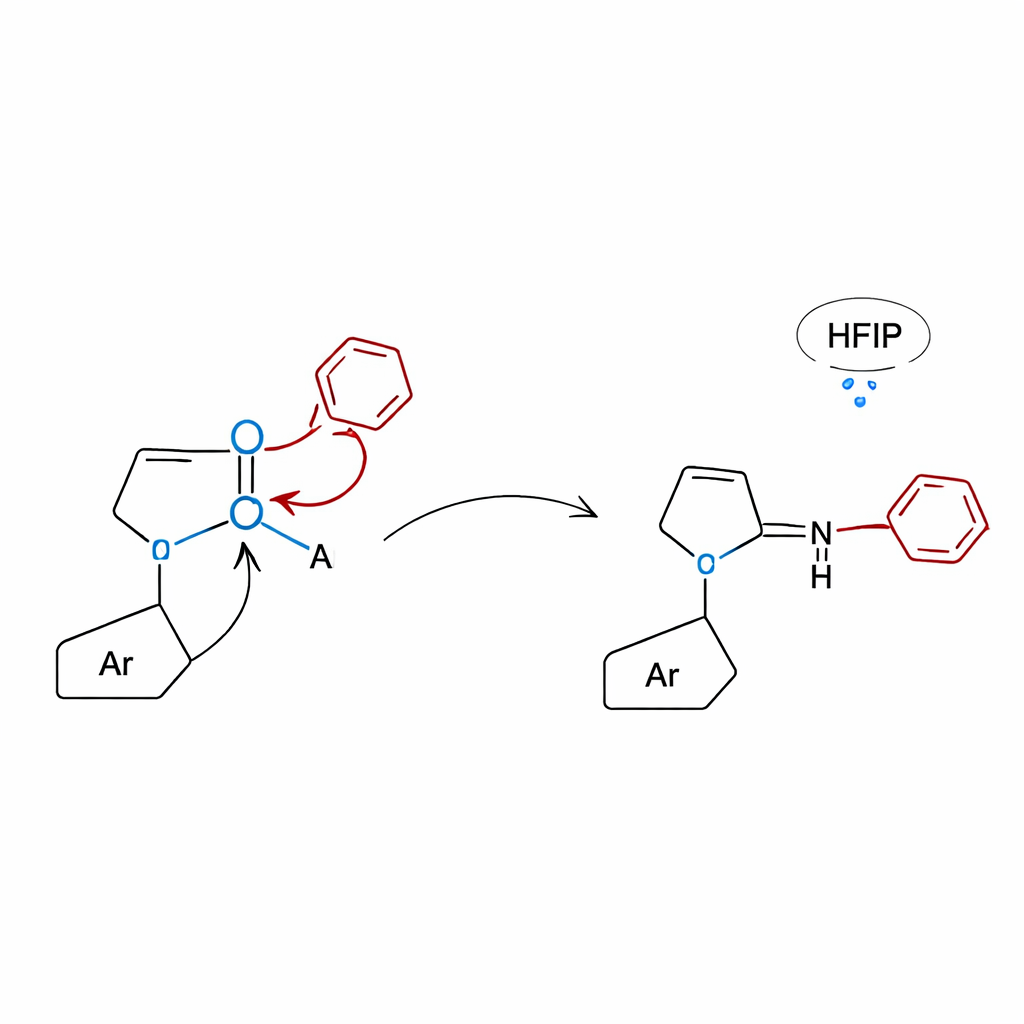
En titt under huven med teori och kontrolltester
För att förstå varför laktam‑ansatsen fungerar så bra kombinerade forskarna genomtänkta kontrollexperiment med beräkningssimulationer. När molekyler utan laktammojlighet testades stannade reaktionerna i stort sett av, vilket bekräftade att laktamringen är avgörande för att aktivera boronsyran och styra omläggningen. Kvantkemiska beräkningar visade att laktamets syre binder till boron för att bilda en kompakt, fyrkoordinerad struktur från vilken arylgruppen kan migrera antingen över fem atomer (1,5‑förskjutning) för att ge N‑alkyl aniliner eller över fyra atomer (1,4‑förskjutning) för att ge 3‑aryl kinoxalinoner. I kinoxalinonfallet sänker vätebindningsnätverket som tillhandahålls av HFIP‑lösningsmedlet ytterligare energibarriären, vilket hjälper reaktionen att gå under relativt milda termiska förhållanden utan någon tillsatt katalysator.
Varför detta är viktigt för framtida läkemedel
Sammanfattningsvis visar arbetet att en enkel laktamring kan fungera som en dynamisk, återanvändbar vägvisare som låser upp tidigare otillgängliga bindningsbildningsmönster i boronsyrekemin. För icke‑specialister är huvudbudskapet att kemister nu har ett mer direkt, effektivt sätt att förvandla grundläggande byggstenar till två viktiga klasser kväveinnehållande molekyler som ligger till grund för många läkemedel. Eftersom metoden undviker ädla metaller, tolererar ett brett spektrum av funktionella grupper och fungerar på avancerade läkemedelslika strukturer, har den god potential att effektivisera designen och optimeringen av framtida läkemedel och eventuellt nya bekämpningsmedel också.
Citering: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Nyckelord: boronsyror, laktamkemi, C–N-bindningsbildning, kinoxalinoner, läkemedelskemi