Clear Sky Science · sv
Enzymmining baserad på ortologinferens för diversifiering av det anti-cancerösa evodiaminskellettet
Att göra växtkemikalier till bättre läkemedel
Många av dagens läkemedel började som försvarskemikalier i växter. Dessa naturliga molekyler uppvisar ofta starka effekter mot cancer, infektioner eller smärta, men de är sällan ”perfekta” läkemedel. Kemister vill gärna finjustera deras strukturer på precisa sätt för att göra dem säkrare och mer effektiva, men dessa molekyler är ofta så komplexa att även små förändringar är svåra. Denna studie visar hur forskare kan utnyttja växtenzymer som små molekylära verktyg för att göra målinriktade förändringar i en anticancerförening kallad evodiamin, vilket potentiellt öppnar nya vägar till förbättrade terapier.
Varför denna växtmolekyl är viktig
Evodiamin är en naturlig förening som hittas i frukterna från ett träd som används i traditionell kinesisk medicin. Den tillhör en familj av ringslutna molekyler som redan ligger till grund för viktiga läkemedel mot cancer, högt blodtryck och infektioner. Själva evodiamin har visat anticancer-, antiinflammatoriska, smärtlindrande och antimikrobiella egenskaper, och vissa av dess modifierade varianter ser särskilt lovande ut som mångmålsinriktade cancerledarämnen. Utmaningen är hur man fäster nya kemiska ”handtag”, såsom syre innehållande grupper, på mycket specifika platser på detta trånga skellett utan att använda hårda kemikalier eller flerstegs-synteser.
Låta enzymerna göra den svåra kemin
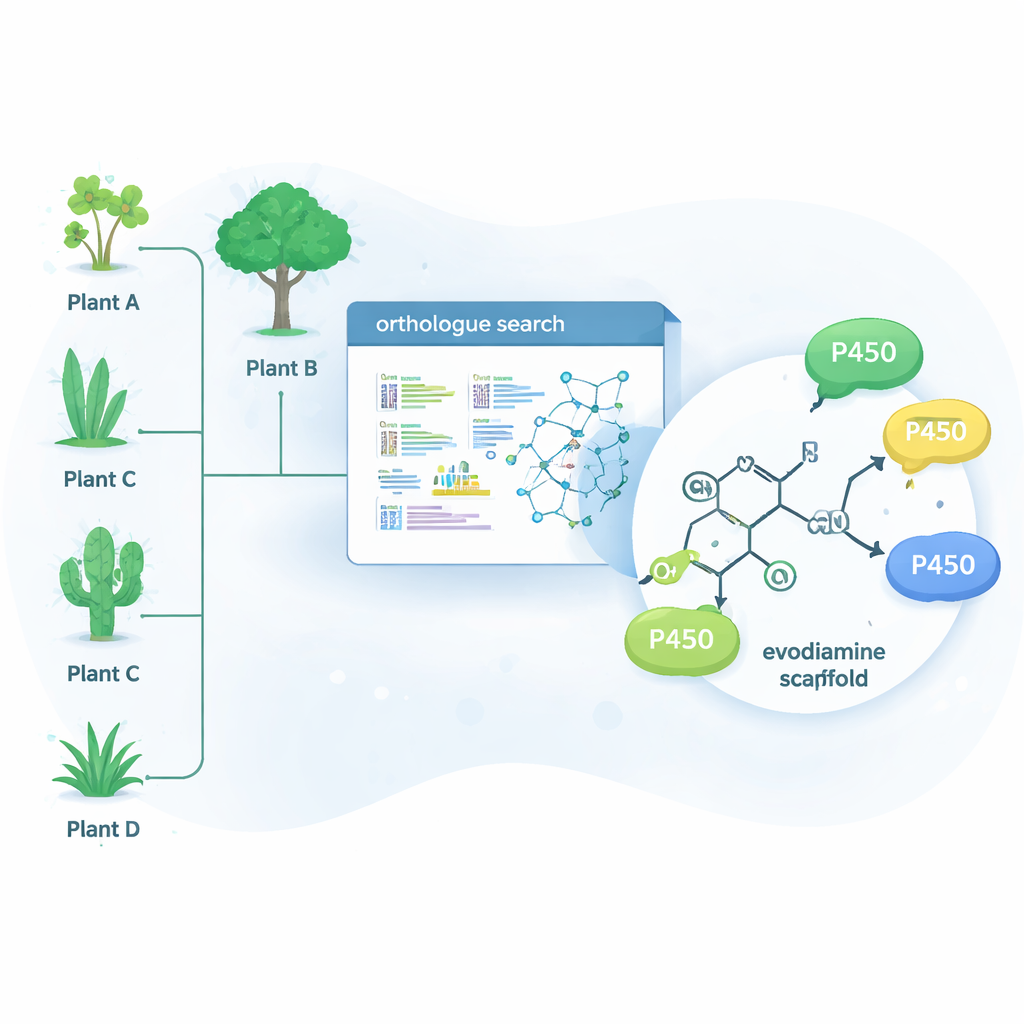
Naturen har redan löst många av dessa svåra kemiska problem med hjälp av enzymer — proteiner som katalyserar specifika reaktioner. En stor enzymfamilj, kallad cytochrome P450, utmärker sig i att tillsätta syre till annars oreaktiva kol–vätebindningar. Det enkla steget kan dramatiskt ändra hur en molekyl beter sig i kroppen och kan också skapa en startpunkt för vidare kemisk modifiering. Istället för att bara söka i växter som naturligt producerar evodiamin använde forskarna ett bioinformatiskt verktyg kallat OrthoFinder för att skanna genetiska data från 15 olika alkaloidproducerande växter. De letade efter P450-enzymer som är nära ”ortologer” till kända alkaloidmodifierande enzymer, med resonemanget att släktingar till dessa enzymer också kan kunna finjustera närbesläktade läkemedelslika molekyler.
Hitta nya enzymer i oväntade växter
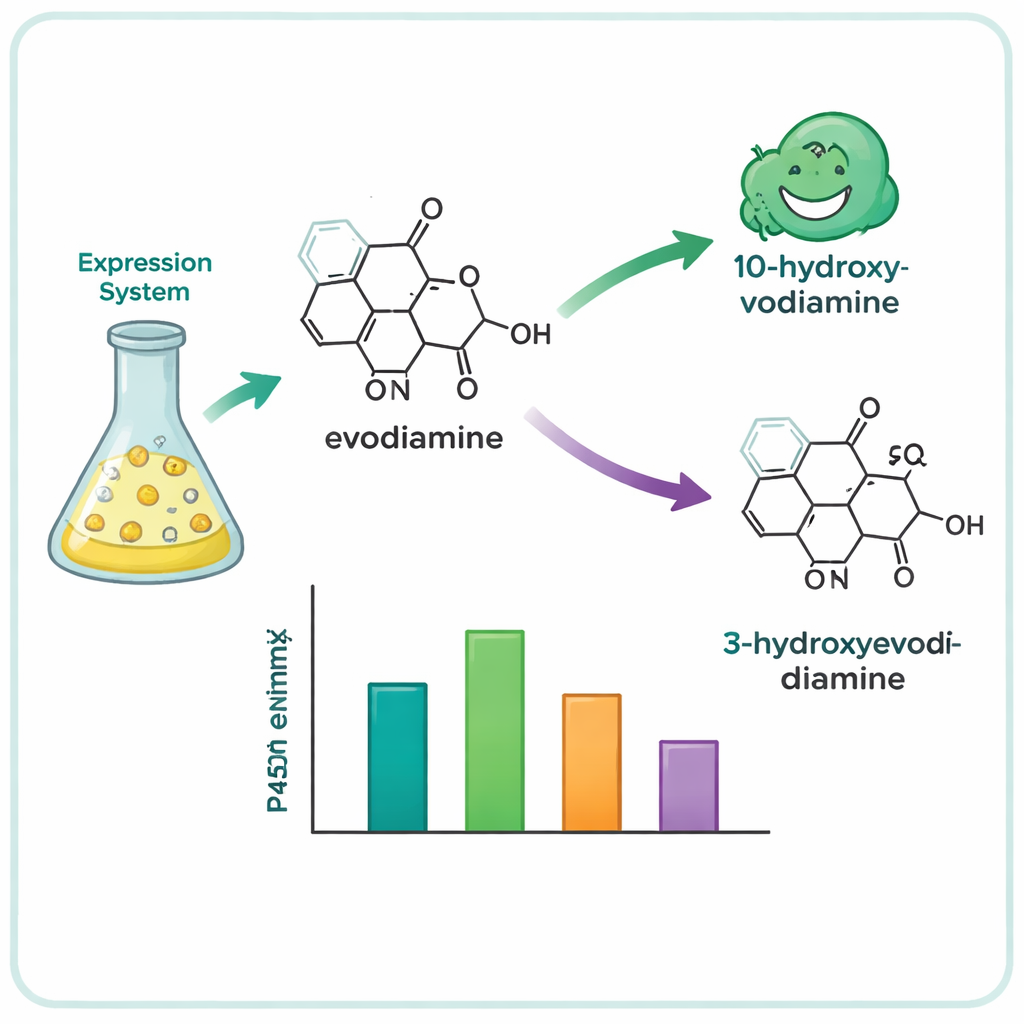
Från hundratals kandidatgener snävlade teamet ner listan till 15 lovande P450:or och uttryckte dem i jästceller, som tjänade som miniatyrenzymfabriker. De matade sedan dessa jästarter med en samling komplexa växtmolekyler och analyserade vilka som kemiskt förändrades. Fyra enzymer — tre från trädet Camptotheca acuminata och ett från busken Tabernaemontana elegans — visade sig agera på evodiamin, trots att ingen av dessa växter är kända för att producera den. Dessa enzymer infogade selektivt en syreatom vid en av två positioner i evodiaminets ringsystem och genererade två huvudprodukter: 10‑hydroxyevodiamin och 3‑hydroxyevodiamin. Sådana oxygenerade varianter är lättare att vidareomvandla till vattentabbara eller mer potenta läkemedelskandidater, med mildare kemi än traditionella syntesvägar.
Ett blick in i det molekylära verktygslådan
För att förstå varför dessa nära släktingar till enzymerna betedde sig olika byggde forskarna tredimensionella modeller av det mest aktiva enzymet och dess släktingar med moderna verktyg för proteinstrukturprediktion. De använde sedan datorbaserad dockning för att se hur evodiamin kan placera sig i enzymernas aktiva fickor, nära P450:ans järninnehållande centrum där reaktionen sker. Modellerna framhöll flera skrymmande, vattenavvisande aminosyror — särskilt fenylalaninrester — positionerade nära evodiaminets aromatiska ringar. Genom att omsorgsfullt mutera dessa positioner visade teamet att förändring av fickans storlek och form kan försvaga aktiviteten, ändra hur väl substratet passar, eller till och med byta det favoriserade syreinfogningsstället från en ring i molekylen till en annan. I ett fall vände en enda mutation enzymets preferens från att bilda 10‑hydroxyprodukten till att bilda 3‑hydroxyprodukten.
Vad detta betyder för framtida läkemedel
För icke-specialister är huvudpoängen att författarna har demonstrerat en praktisk färdplan för att upptäcka och finjustera växtenzymer som kan utföra precisa, ”kirurgiska” ändringar på komplexa läkemedelslika molekyler. Genom att kombinera storskalig genetisk prospektering med enzymtestning och strukturell modellering upptäckte de en uppsättning biokatalysatorer som selektivt kan omforma evodiaminskellettet på positioner som är svåra att nå med standardkemi. Detta erbjuder inte bara ett renare, mer hållbart sätt att göra avancerade versioner av evodiamin — såsom vattenlösliga anticancerledare — utan visar också att användbara enzymer kan hittas i växter som aldrig gör målmolekylen själva. Samma strategi kan nu tillämpas på många andra naturprodukter och påskynda designen av nästa generationens växtbaserade läkemedel.
Citering: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Nyckelord: evodiamin, växtenzymer, cytochrome P450, biokatalys, läkemedelsupptäckt