Clear Sky Science · sv
PACS1‑syndromets mutation stör dyneinmedierad godstransport via HDAC6 och BICD2
Varför detta är viktigt för hjärnans utveckling
PACS1‑syndromet är ett sällsynt genetiskt tillstånd som orsakar utvecklingsstörning, anfall och karakteristiska ansiktsdrag. Familjer och kliniker känner till symtomen, men ända tills nyligen var det oklart vad som faktiskt går fel inne i patienternas celler. Denna studie lyfter på slöjan och visar hur en enkel bokstavsförändring i PACS1‑genen saboterar cellens interna transportsystem, särskilt i neuroner, och hur det kopplar PACS1‑syndromet till en bredare familj av nervsystemsjukdomar som beror på störd ”trafik”. 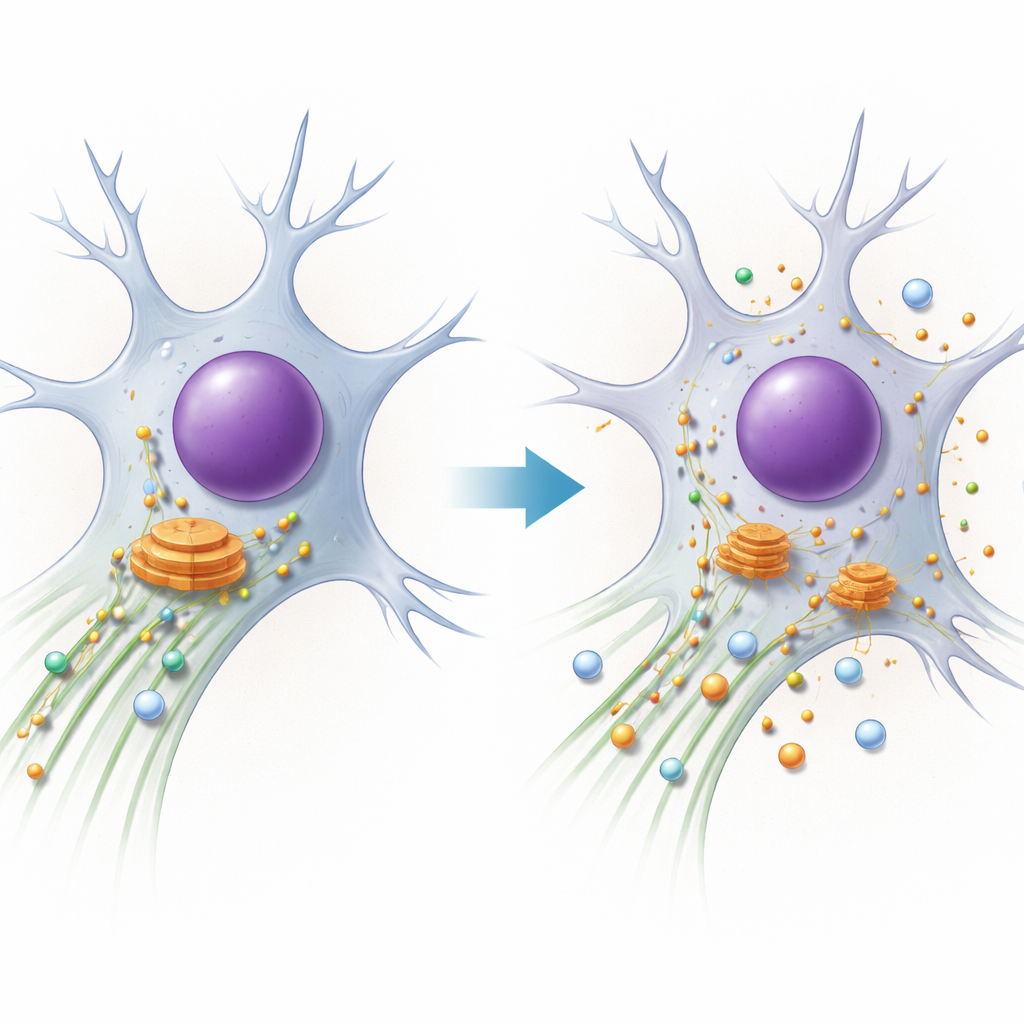
Cellens leveransmotorvägar
Varje cell förlitar sig på mikroskopiska motorvägar byggda av proteintubuli som kallas mikrotubuli. Molekylära motorer rör sig längs dessa spår och fraktar last, som enzymer och membrankomponenter, dit de behövs. En av motorerna, dynein, ansvarar för långdistans "återresor" och drar gods från cellens perifieri tillbaka mot centrum, där en stor sorteringsstation, Golgiapparaten, ligger. Författarna fokuserar på PACS1, ett protein som hjälper till att välja vilken last som kopplas till dynein och dessutom finjusterar spårens tillstånd via ett annat protein, HDAC6, som kontrollerar en kemisk märkning (acetylation) på mikrotubuli. Neuroner, med sina mycket långa utskott, är särskilt känsliga för även små fel i detta system.
En mutant koordinator som griper för hårt
PACS1‑syndromet orsakas av den återkommande R203W‑mutationen i PACS1. Forskarna fann att både normalt och muterat PACS1 fysiskt binder dyneins tunga kedja, men den muterade formen fastnar starkare. Med hjälp av patienthudceller och konstruerade cellinjer visade de att denna överengagemang ger samma utfall som en partiell förlust av dyneinfunktion: Golgi splittras i spridda mini‑stackar, och ett viktigt enzym kallat furin, som normalt finns vid Golgis trans‑sida, hamnar felaktigt i andra kompartment. Genom att dissekera PACS1:s struktur identifierade de en kort beta‑strängs"lapp" som specifikt kontaktar dynein. När de ändrade denna lapp utan att störa andra PACS1‑funktioner förlorade furin åter sin korrekta adress, vilket bekräftar att dynein–PACS1‑handskakningen är avgörande för korrekt lastplacering. 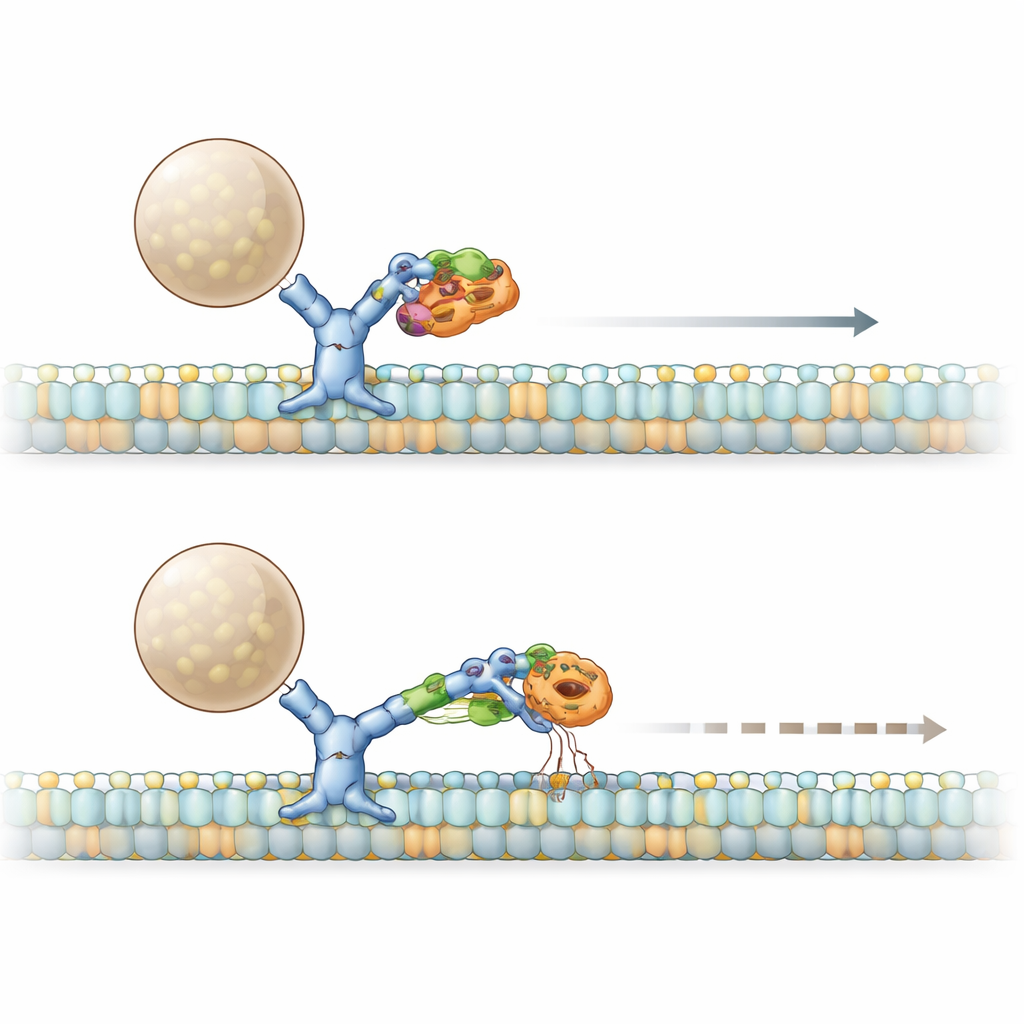
Hur en treproteinsallians sätter motorn i baklås
Berättelsen fördjupas med två ytterligare aktörer: HDAC6 och en adaptrarprotein kallat BICD2, som hjälper till att bygga aktiva dyneinkomplex. Den muterade PACS1 ökar inte bara HDAC6‑aktiviteten, vilket minskar acetylationen på mikrotubuli, utan bildar också ett förstorad komplex med HDAC6 och BICD2. Biokemiska tester visade att mutant PACS1 och HDAC6 tillsammans drar bort BICD2 från dynein samtidigt som BICD2:s partnerskap med en framåtriktad motor (kinesin) lämnas intakt. I levande celler saktade en artificiell last som normalt rör sig snabb längs dynein ner, och färre laster rörde sig alls när muterat PACS1 fanns närvarande. Blockering av HDAC6:s aktivitet återställde både hastigheten och antalet rörliga partiklar, vilket visar att det muterade PACS1–HDAC6–BICD2‑komplexet fungerar som en broms på dyneins förmåga att initiera och upprätthålla transport.
Rädda trafiken med en naturlig dyneinhjälpare
Forskarna testade därefter om dynein kunde "åter‑aktiveras" trots det muterade komplexet. De vände sig till Lis1, en känd dyneinhjälpare som stabiliserar aktiva motorkomplex. I patientceller var Lis1‑nivåerna något minskade. När forskarna tillsatte extra Lis1 förbättrades två saker: Golgi återklustrades nära cellcentrum, och lysosomer, en annan organellklass som hade förskjutits utåt, återgick till sin plats. I samma motilitetsanalys ökade Lis1 både frekvensen och hastigheten för dyneindriven lasttransport i närvaro av muterat PACS1. Dessa resultat visar att problemet inte är att dynein saknas, utan att den sitter fången i ett svagt aktivt tillstånd — ett tillstånd som delvis kan korrigeras antingen genom att dämpa HDAC6 eller genom att förstärka dyneinaktivering.
Knyta ett sällsynt syndrom till en bredare uppsättning störningar
Genom att kombinera strukturanalys, cellbiologi och liveavbildning föreslår författarna en tydlig modell: PACS1 länkar normalt utvalda laster till dynein och finjusterar motorns prestanda via HDAC6 och mikrotubuliacetylation. R203W‑mutationen öppnar upp PACS1:s interaktionsyta, vilket överrekryterar HDAC6 och BICD2 till ett komplex som undergräver dyneins förmåga att greppa mikrotubuli och röra sig effektivt. Resultatet blir utbredd felplacering av Golgi, lysosomer och andra laster, särskilt i neuroner där långdistans‑transport är avgörande. Denna mekanism hjälper till att förklara varför sänkning av PACS1 eller HDAC6 med antisense‑behandlingar korrigerar hjärndefekter i musmodeller och nu undersöks hos patienter. Mer generellt placerar den PACS1‑syndromet inom det växande spektret av mikrotubulära trafikstörningar, tillsammans med tillstånd orsakade av mutationer i dynein, BICD2 och relaterade transportfaktorer.
Citering: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Nyckelord: PACS1‑syndromet, dyneintransport, mikrotubulär trafik, Golgi‑organisation, neuronal utveckling