Clear Sky Science · sv
Det sekretoriska proteinet CLCF1 förbättrar kolestatisk leversjukdom genom att hämma leverns gallsyrasyntes och främja gallsyrautsöndring
Varför denna forskning är viktig för leverhälsa
Kolestatiska leversjukdomar är tillstånd där galla, en matsmältningsvätska som produceras i levern, inte flödar som den ska utan istället ansamlas och gradvis förgiftar levern inifrån. Nuvarande läkemedel hjälper endast en del av patienterna, och många blir till slut beroende av levertransplantation. Denna studie avslöjar ett naturligt producerat protein, kallat CLCF1, som kroppen tycks aktivera som ett försvarssystem vid kolestatiska leversjukdomar. Att förstå hur detta protein verkar kan peka mot nya behandlingar som skyddar levern genom att både minska produktionen av skadliga gallkomponenter och hjälpa kroppen att göra sig av med dem mer effektivt.
En dold hjälpare i sjuka lever
Forskarna började med att undersöka levervävnad från patienter med primär biliär kolangit och primär skleroserande kolangit, två stora former av kronisk kolestatisk leversjukdom. De jämförde personer med tidig sjukdom med dem som hade mer avancerad kolestas och analyserade också befintliga offentliga gen-dataset. I dessa oberoende humana datakällor utmärkte sig ett sekretoriskt protein: CLCF1 var konsekvent bland de mest kraftigt uppreglerade generna i kolestatiska lever. Högre nivåer av CLCF1 korrelerade med sämre blodmarkörer för sjukdomens svårighetsgrad, vilket tyder på att levern ökar produktionen av detta protein i takt med ökad stress och gallans ansamling. Hos patienter i tidigt skede som behandlades med standardläkemedlet ursodeoxikolsyra hade de som svarade väl ofta mer CLCF1 i levern, vilket antyder att detta protein kan vara ett tecken på en mer anpassningsbar och behandlingskänslig lever.
Test av CLCF1 i djurmodeller
För att gå bortom humana korrelationer vände teamet sig till möss och använde både genetiska och dietära metoder för att efterlikna kolestatisk leversjukdom. I två olika musemodeller ökade kolestas starkt leverns produktion av Clcf1, vilket speglade fynden från människan. När forskarna särskilt avlägsnade receptorn för CLCF1 från leverceller förvärrades den kolestatiska skadan markant: gallgångarna överväxte, leverceller dog, inflammation ökade, ärrvävnad bildades och toxiska gallsyror ansamlades. Den omvända experimentuppställningen gav en mer hoppfull bild. När teamet använde ett ofarligt virus för att öka Clcf1-nivåerna endast i levern skyddades mössen. Deras leverstatus förbättrades visuellt, blodproverna förbättrades, fibros minskade och mängden gallsyror som fastnade i levern sjönk kraftigt.
Stänga av kranen och öppna avloppet
Hur minskar CLCF1 gallsyrabelastningen så effektivt? Forskarna identifierade två kompletterande åtgärder. För det första dämpade CLCF1 direkt leverns egen gallbildande maskineri. I flera musemodeller och i odlade leverceller slog extra CLCF1 konsekvent av nyckelenzymer som omvandlar kolesterol till gallsyror, vilket i praktiken minskade tillflödet av ny galla. Detta skedde utan att aktivera den vanliga leverbrytaren för gallkontroll, en nukleär receptor kallad FXR, vilket tyder på att CLCF1 använder en alternativ väg inne i levercellerna för att bromsa gallsyrasyntesen. För det andra påverkade CLCF1 hur galla hanterades längre ned i kroppen. Det omformade tarmens mikrobiella samhälle mot bakterier som är särskilt skickliga på att bearbeta gallsyror och ökade mängden gallsyror som lämnar kroppen i avföringen, vilket fungerar som ett effektivare avlopp.
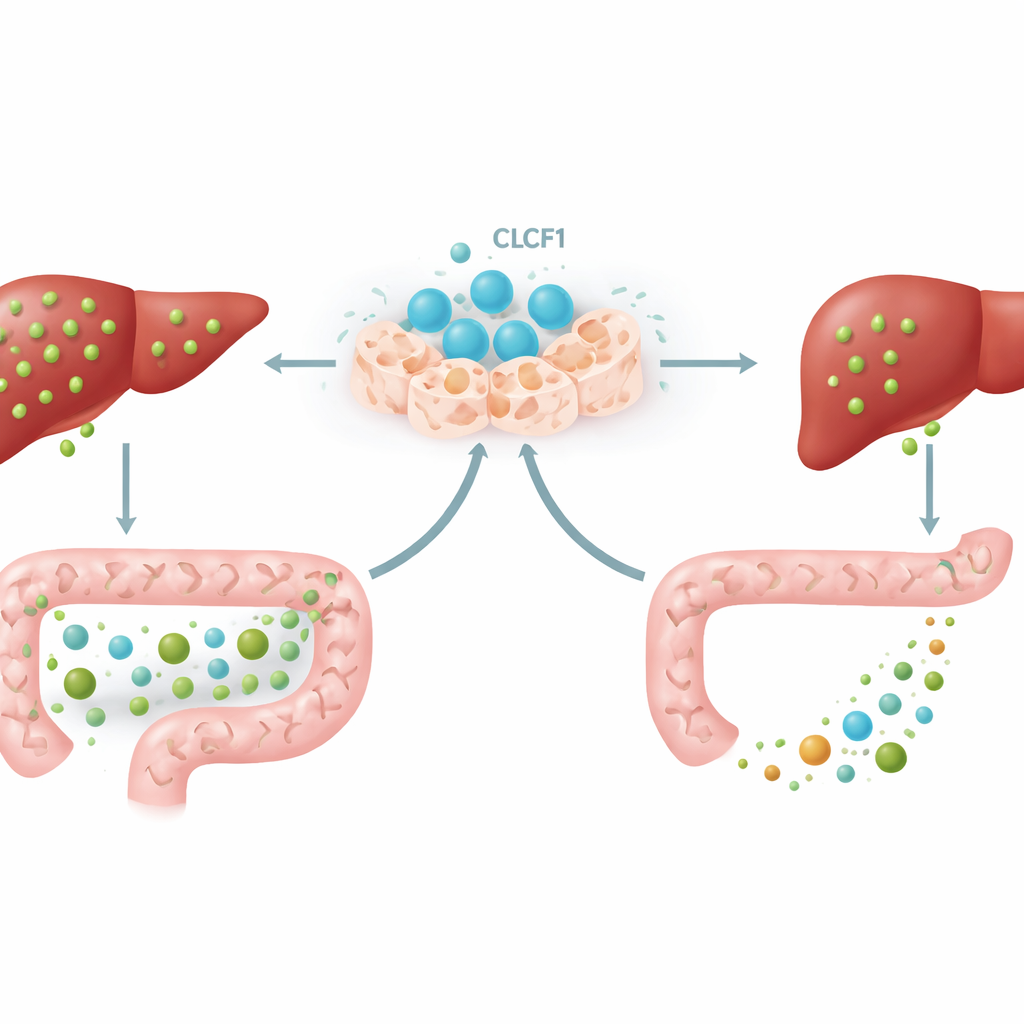
Samtalet mellan tarm och lever
En central del av pusslet involverade en signalslinga mellan tarm och lever. Vissa gallsyror i tarmen aktiverar en sensor kallad FXR i tarmceller, som då frigör ett budskapshormon känt som FGF15 i möss. Detta hormon färdas via blodet till levern och säger åt den att sakta ner gallsyrasyntesen. Med extra CLCF1 ackumulerade mössen specifika typer av gallsyror i tarmarna—särskilt former som är kända för att starkt aktivera FXR. Som ett resultat aktiverades tarmens FXR, FGF15-nivåerna steg i både tarm och lever, och levern dämpade ytterligare sin produktion av gallsyror. När forskarna blockerade intestinal FXR med ett tarmbegränsat läkemedel försvagades mycket av CLCF1:s skyddande effekt, vilket visar att detta tarm–lever-samtal är en väsentlig del av proteinets verkningsmekanism.
Vad detta kan innebära för framtida behandlingar
Tillsammans målar dessa fynd upp CLCF1 som en inbyggd säkerhetsventil vid kolestatisk leversjukdom. Proteinet minskar gallsyranivåerna från båda ändar: det bromsar deras bildning i levern och främjar deras avlägsnande via tarmen, hjälpt av fördelaktiga tarmbakterier och en hormonell återkopplingssignal. Till skillnad från befintliga läkemedel som aktiverar FXR i hela kroppen och kan ge biverkningar som klåda och förändrade blodfetter, verkar CLCF1 styra gallkontrollen mer milt och selektivt, särskilt via tarmen. Även om arbetet fortfarande är begränsat till möss och laboratorieprov tyder resultaten på att förstärkning av CLCF1 eller imitation av dess vägar skulle kunna bilda grunden för nya terapier—och att mätning av detta protein, eller de gallsyror det ökar i tarmen, kan hjälpa till att identifiera patienter som skulle ha störst nytta.
Citering: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Nyckelord: kolestatisk leversjukdom, gallsyror, tarm–lever-axeln, CLCF1, tarmmikrobiota