Clear Sky Science · sv
Typ VI-sekretionssystemet hos Acinetobacter: mekanismer, biologi och terapeutisk potential
Dolda vapen i sjukhusbakterier
Många vet att vissa sjukhusbakterier kan motstå antibiotika, men färre inser att dessa mikrober också för hårda strider sinsemellan. Denna översikt granskar ett mikroskopiskt "fjäderladdat spjut" inne i Acinetobacter, en grupp bakterier som inkluderar den ökända sjukhusbakterien Acinetobacter baumannii. Att förstå hur detta inbyggda vapen fungerar, när det aktiveras och hur det hjälper infektioner att etablera sig kan öppna nya vägar för diagnos och desarmering av livshotande, läkemedelsresistenta infektioner.
En överlevnadsmaskin, inte bara ett giftspjut
Acinetobacter-arter lever i jord, vatten och på vår hud, men några har blivit mycket framgångsrika sjukhuspatogener. Ett nyckelverktyg i deras arsenal är typ VI-sekretionssystemet, eller T6SS, en liten kontraktil maskin förankrad i cellmembranet. När det triggas avfyrar det en nålliknande spets laddad med giftiga proteiner in i intilliggande celler, ofta och omedelbart dödande konkurrerande bakterier vid kontakt. Till skillnad från vissa andra bakterier som bär flera varianter av detta system har patogena Acinetobacter vanligtvis bara ett T6SS, men de har anpassat denna enda plattform för många syften — från att hålla konkurrenter på avstånd till att forma infektioner.
Omsmidad hårdvara: en ovanlig uppskjutningsplattform
De flesta bakterier bygger sitt T6SS kring en standarduppsättning delar, men Acinetobacter har omarbetat flera nyckelkomponenter. Den saknar en vanlig yttre membranankare kallad TssJ och förlitar sig istället på en trio specialiserade hjälpämnen: TsmK bildar en grund i innermembranet, TslA stabiliserar ett långt "tunnel"-protein (TssM) när det korsar cellväggen, och TagX skär lokalt i väggen för att skapa plats åt vapnet. Utöver detta måste ett särskilt spikprotein, VgrG1, ha nästan perfekt form för att systemet överhuvudtaget ska kunna avfyras — enstaka aminosyreförändringar kan göra det obrukbart. Tillsammans visar dessa förändringar hur evolutionen kan ersätta saknade delar med nya lösningar samtidigt som den grundläggande avfyrningsprincipen bevaras.
Smarta styrningar: när attackläge är meningsfullt
Att bygga och avfyra denna nanomaskin är kostsamt, så Acinetobacter håller den under strikt kontroll. Ett globalt DNA-bindande protein (H-NS) och speciella repressorer som finns på plasmider med multiresistens kan låsa systemet i "av"-läge, särskilt när resistensgener delas mellan celler. Vid hög celltäthet kan kemiska "kvorum"-signaler slå på det, vilket förbereder bakterierna för täta konkurrenssituationer. Metalljoner spelar också en roll: vid oxidativ stress aktiverar importerad mangan en liten RNA-molekyl som orsakar att viktiga T6SS-meddelanden förstörs, vilket nedjusterar vapnet för att gynna överlevnad i värden. Även kapseln — en sockrig yttre hinna — fungerar både som sköld och broms, genom att blockera inkommande attacker men också mekaniskt dämpa Acinetobacters egen avfyrning.
En mångsidig verktygslåda av mikroskopiska stötar
När Acinetobacter väl drar i avtryckaren kan den leverera ett brett spektrum av toxiner. Vissa enzymer bryter ner den sega cellväggen hos konkurrenter; andra fräter tyst sönder cellmembran, och åter andra skär upp DNA inuti målceller. Varje toxin paras ihop med ett motsvarande "immunitets"-protein som skyddar angriparen från vänskott. Ett DNA-skärande toxin, som nu kallas TafE, kan till och med döda svampar, vilket antyder tvärkungliga drabbningar på platser som tarm eller lungor. Genomikstudier tyder på att Acinetobacter kodar för många fler, ännu okarakteriserade toxiner, ofta packade i stora Rhs-proteiner som fungerar som modulära bärare. Istället för att förlita sig på ett enda slag verkar dessa bakterier använda lager av attacker som skadar flera viktiga strukturer samtidigt.
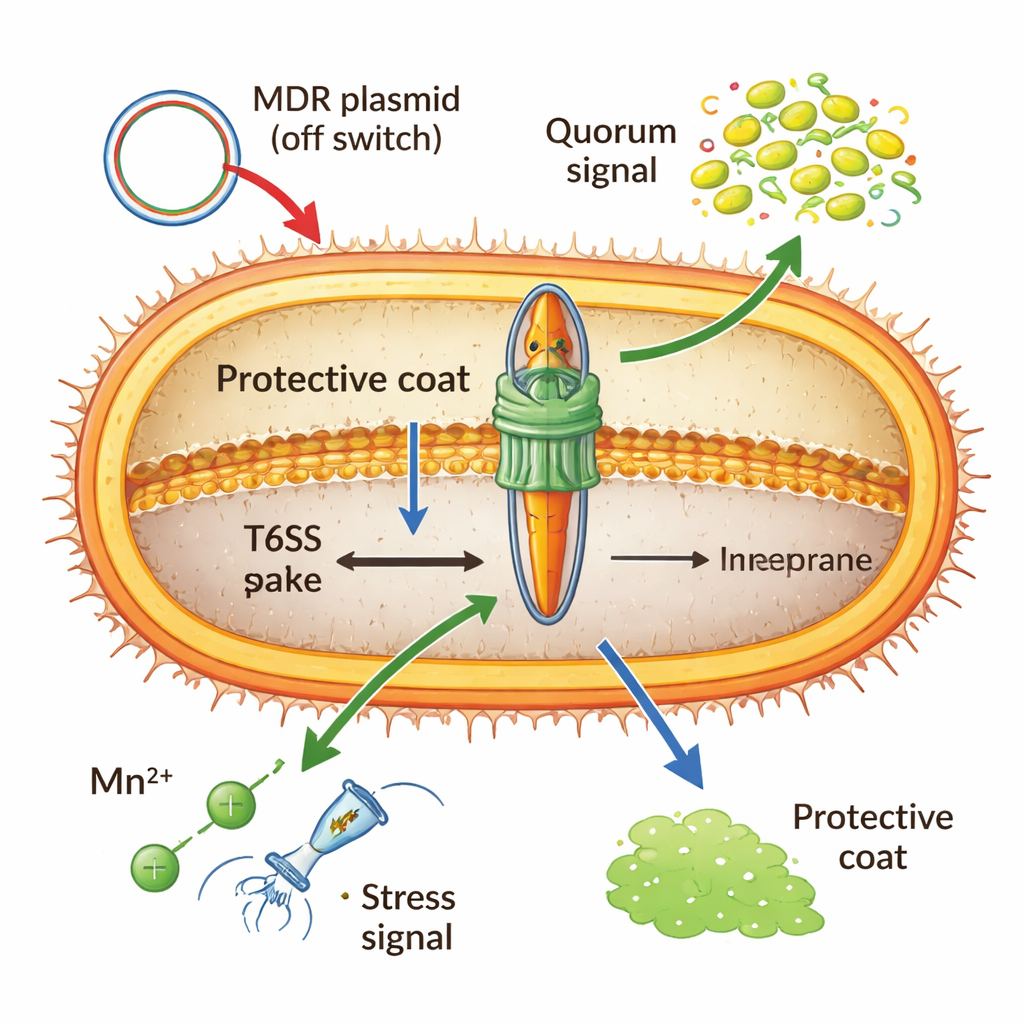
Formar infektioner, gener och framtida behandlingar
Bevis från patientisolat och djurmodeller tyder på att ett aktivt T6SS ofta går hand i hand med svårare sjukdom, starkare inflammation och bättre överlevnad för bakterierna inne i värdar. Genom att döda intilliggande mikrober frigör systemet också DNA som naturligt kompetenta Acinetobacter-celler kan ta upp, vilket påskyndar spridningen av egenskaper som antibiotikaresistens. Samtidigt är det kostsamt att hålla vapnet konstant aktivt, så många framgångsrika sjukhusstammar bär plasmider eller mutationer som tystar det när resistensen är säkrad. Sammantaget argumenterar författarna för att detta sekretionssystem inte bör ses som en enkel virulensfaktor utan som en flexibel "fitnessmodul" som Acinetobacter finslipar upp eller ner för att balansera aggression, persistens och energianvändning. Denna nya syn pekar mot praktiska tillämpningar, från vaccin som riktar in sig på bevarade T6SS-delar till läkemedel som selektivt låser upp avfyrningsmekanismen, och hjälper läkare att överlista en farlig och anpassningsbar sjukhusmotståndare.
Citering: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Nyckelord: Acinetobacter, typ VI-sekretionssystem, antibiotikaresistens, bakteriell konkurrens, sjukhusinfektioner