Clear Sky Science · sv
Tillväxthastighetsdriven modellering tyder på att fenotypisk anpassning driver läkemedelsresistens i BRAFV600E-mutant melanom
Cancerceller som lär sig leva med läkemedel
Målstyrda läkemedel har förändrat behandlingen för många med melanom, en allvarlig hudcancer. Ändå slutar dessa läkemedel nästan alltid att fungera: tumörer som tidigare krympt börjar växa igen. Denna studie ställer en enkel men kraftfull fråga: i stället för att enbart förlita sig på genetiska mutationer, kan melanomceller "lära sig" att överleva behandling genom att förändra sitt beteende — och kan denna inlärning förklara varför vissa sätt att ge läkemedel fungerar bättre än andra?
Från känsliga celler till överlevare
Forskarlaget fokuserade på melanomceller med en vanlig förändring i genen BRAF, vilket gör dem särskilt känsliga för en typ av läkemedel kallad BRAF-hämmare. I tidigare laboratorieexperiment exponerades dessa celler för läkemedlet encorafenib i olika doser och under olika tidsperioder. Genom att noggrant mäta hur snabbt cellerna växte eller dog under varje förhållande delade författarna in cellerna i två breda kategorier: läkemedelsnaiva celler som aldrig tidigare sett läkemedlet, och läkemedelsanpassade celler som levt i läkemedlet i minst en vecka. De läkemedelsnaiva cellerna växte bra utan behandling men bromsades kraftigt eller dödades av läkemedlet. De läkemedelsanpassade cellerna, däremot, växte bättre i närvaro av läkemedlet men förlorade den fördelen när läkemedlet togs bort — vilket antyder att deras överlevnad hänger ihop med ett flexibelt, reversibelt tillståndsskifte snarare än permanent genetisk skada.
Karta över dolda cellbeteenden
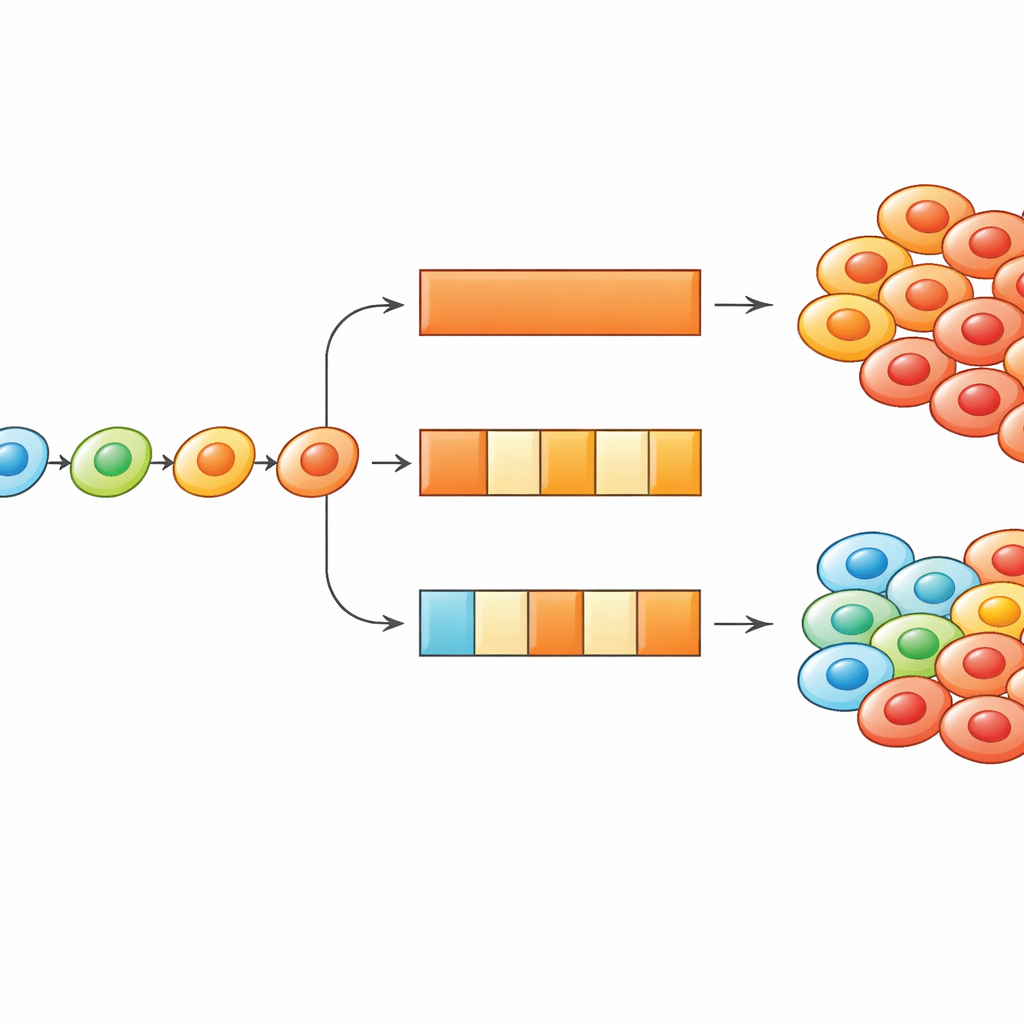
För att förstå dessa förändringar byggde teamet en matematisk modell där varje cancercell tilldelas ett "fenotyptillstånd" — en abstrakt position på en skala från mycket läkemedelskänslig till mycket läkemedelsresistent. Istället för att anta endast två celltyper tillät de många mellanliggande tillstånd, vilket speglar gradvisa beteendeskift som observerats i biologiska markörer för resistens. För varje kombination av tillstånd och läkemedelsdos uppskattade de en nettotillväxthastighet, som kan vara positiv (fler celldelningar än dödsfall) eller negativ (fler dödsfall än delningar). Alla dessa hastigheter arrangerades i ett rutnät, en "fitness-matris", som fungerar som ett landskap: vissa tillstånd vid vissa doser är gynnsamma platser för cellerna att frodas, andra är dödliga. Celler i modellen kan förflytta sig steg för steg över detta landskap när behandlingen sätts på eller stängs av.
Driver cellerna bort eller mot fördel?
Den avgörande okända faktorn var hur cellerna rör sig över detta landskap. Författarna testade fyra möjliga strategier. I en förändrar sig cellerna aldrig, så eventuella resistenta celler måste finnas från början. I en annan vandrar cellerna slumpmässigt mellan närliggande tillstånd, som en berusads vandring, oavsett om deras situation förbättras. I de två återstående strategierna tenderar cellerna att röra sig mot tillstånd där deras tillväxthastighet är högre — antingen med brus, med vissa misstag, eller starkt, alltid klättrande mot bättre överlevnad. När teamet körde datorsimuleringar och jämförde dem med verkliga laboratoriedata, särskilt experiment där läkemedlet gavs antingen kontinuerligt eller i ett av–på-mönster (en vecka på, en vecka av), kunde endast de strategier där cellerna klättrar mot högre fitness återge vad som observerats: intermittent behandling vid hög dos undertryckte cellantal bättre än kontinuerlig behandling med samma totala tid och en högre total mängd läkemedel.
Använda av–pådoser för att vända anpassning mot cancern
Genom att gå djupare använde forskarna både simuleringar och enklare ekvationer för att utforska hur ofta celler tillåts byta tillstånd och hur långa perioder med läkemedel på respektive av är. De fann att när celler anpassar sig i en riktad riktning kan behandlingsscheman ställas in för att antingen bromsa eller utnyttja denna anpassning. Att förkorta hur ofta celler kan uppdatera sitt tillstånd — konceptuellt att sakta ner de biologiska mekanismer som möjliggör fenotypiska förändringar — tenderar att göra intermittenta behandlingar mer effektiva, eftersom cellerna inte så snabbt kan klättra till starkt resistenta tillstånd. Omvänt, om cellerna börjar i ett starkt resistent tillstånd kan läkemedelsuppehåll ge dem tid att glida tillbaka mot mer känsliga tillstånd, så att återinträde av läkemedlet utlöser en våg av celldöd. Studien visar hur doseringstidpunkt och snabbheten i cellulär anpassning tillsammans formar vilket schema som fungerar bäst.
Vad detta betyder för framtidens cancervård
För en lekman är huvudbudskapet att cancerceller inte bara är statiska fiender; de är formväxlare. I detta melanomsystem verkar cellerna aktivt röra sig mot beteenden som hjälper dem att växa under de förhållanden de möter. Författarnas modell antyder att denna riktade anpassning ensam — utan att åberopa olika permanenta kloner — kan förklara varför av–påläkemedelsscheman ibland slår konstant dosering, även när de använder mindre läkemedel totalt. Medan dessa resultat kommer från celler odlade i labb och kräver mer arbete innan de kan styra patientbehandling, erbjuder tillvägagångssättet en praktisk ram: genom att mäta hur snabbt och i vilken riktning cancerceller anpassar sig kan läkare så småningom utforma behandlingsscheman som inte bara attackerar tumörer utan också styr deras fenotypiska "inlärning" mot återvändsgränder i stället för flyktvägar.
Citering: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Nyckelord: melanom, läkemedelsresistens, cellplastisitet, intermittent terapi, matematisk modellering