Clear Sky Science · sv
Strukturell bas för aktivering av Neisseria meningitidis quinolberoende kvävemonoxidreduktas genom dimerisering
Hur bakterier överlistar vårt immunsvar
När skadliga bakterier invaderar kroppen släpper våra immunceller lös giftiga molekyler som kvävemonoxid för att döda dem. Vissa patogener har dock utvecklat molekylära knep för att neutralisera denna attack och överleva. Denna studie visar, i atomär detalj, hur ett centralt bakteriellt enzym omkonfigurerar sig till par för att bli betydligt bättre på att avgifta kvävemonoxid, och varför förståelsen av detta formskiftande beteende kan öppna nya vägar för antibiotikautveckling.
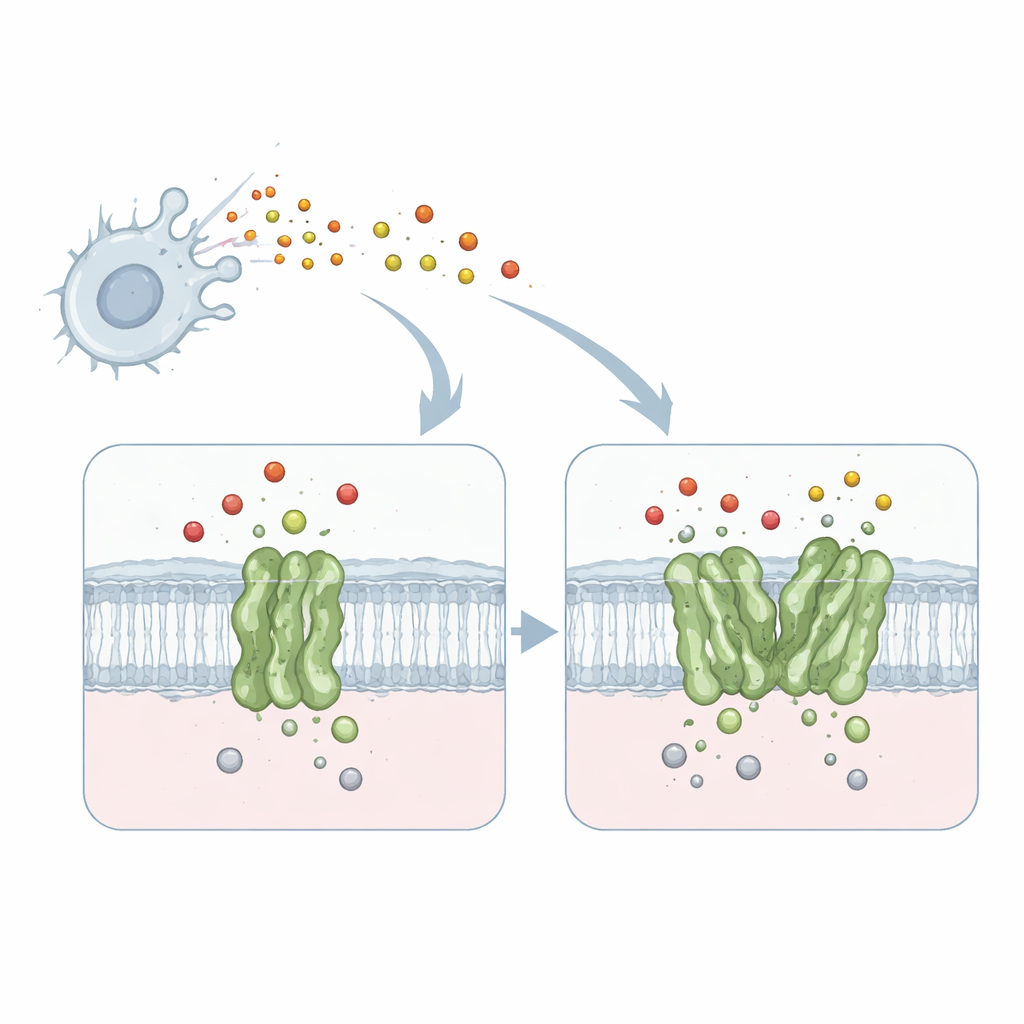
En liten maskin som avväpnar en giftig gas
Arbetet fokuserar på ett membranprotein kallat quinolberoende kvävemonoxidreduktas, eller qNOR, från hjärnhinneinflammationsframkallande bakterien Neisseria meningitidis. qNOR sitter i bakteriens cellmembran och omvandlar kvävemonoxid—en giftig gas som produceras av vårt immunsystem—till mindre skadliga produkter. Denna avgiftning gör att mikroben kan fortsätta andas och växa även i fientliga miljöer såsom mänskliga makrofager. Eftersom respiration och borttagning av kvävemonoxid är avgörande för patogenens överlevnad är qNOR ett attraktivt mål för nya antimikrobiella läkemedel.
När en är bra men två är bättre
Tidigare biokemiska studier visade att qNOR kan förekomma antingen som en enhet (en monomer) eller som ett par (en dimer), och att dimeren arbetar två till fyra gånger snabbare med att neutralisera kvävemonoxid. Fram till nu har det varit oklart varför det att bara para ihop två kopior av samma enzym hade en så dramatisk effekt på prestandan. För att besvara detta använde forskarna högupplöst enkelpartikel-kryoelektronmikroskopi för att fånga detaljerade tredimensionella strukturer av både monomera och dimeriska qNOR från samma bakteriestam. De erhöll närapå atomupplösta vyer—1,89 ångström för dimeren och 2,25 ångström för monomeren—tillräckligt skarpa för att lokalisera individuella aminosidokedjor, metalljoner och många vattenmolekyler.
En flexibel helix blir ett stabiliserande stag
Överraskande nog såg enzymets katalytiska kärna—metallcentret där kvävemonoxid omvandlas—nästan identisk ut i båda formerna. I stället framträdde nyckelskillnader en bit bort, i en transmembranhelix kallad TM10 och i hur den kontaktar en annan helix (TM2) när två qNOR-molekyler parar sig. I monomeren är TM10 löst förankrad och kan svaja och böjas avsevärt, vilket framkom ur beräkningsmässiga analyser av kryo-EM-data. I dimeren låser TM10 från varje partner mot sin granne och bildar ett fyrhelixpaket som kraftigt begränsar dess rörelse. Denna stabilisering omplacerar subtilt en avgörande aminosyra, en glutamat benämnd Glu563, och för den närmare en annan glutamat (Glu494) nära den aktiva ytan och formar en mer fokuserad väg för inkommande protoner som behövs för reaktionen.
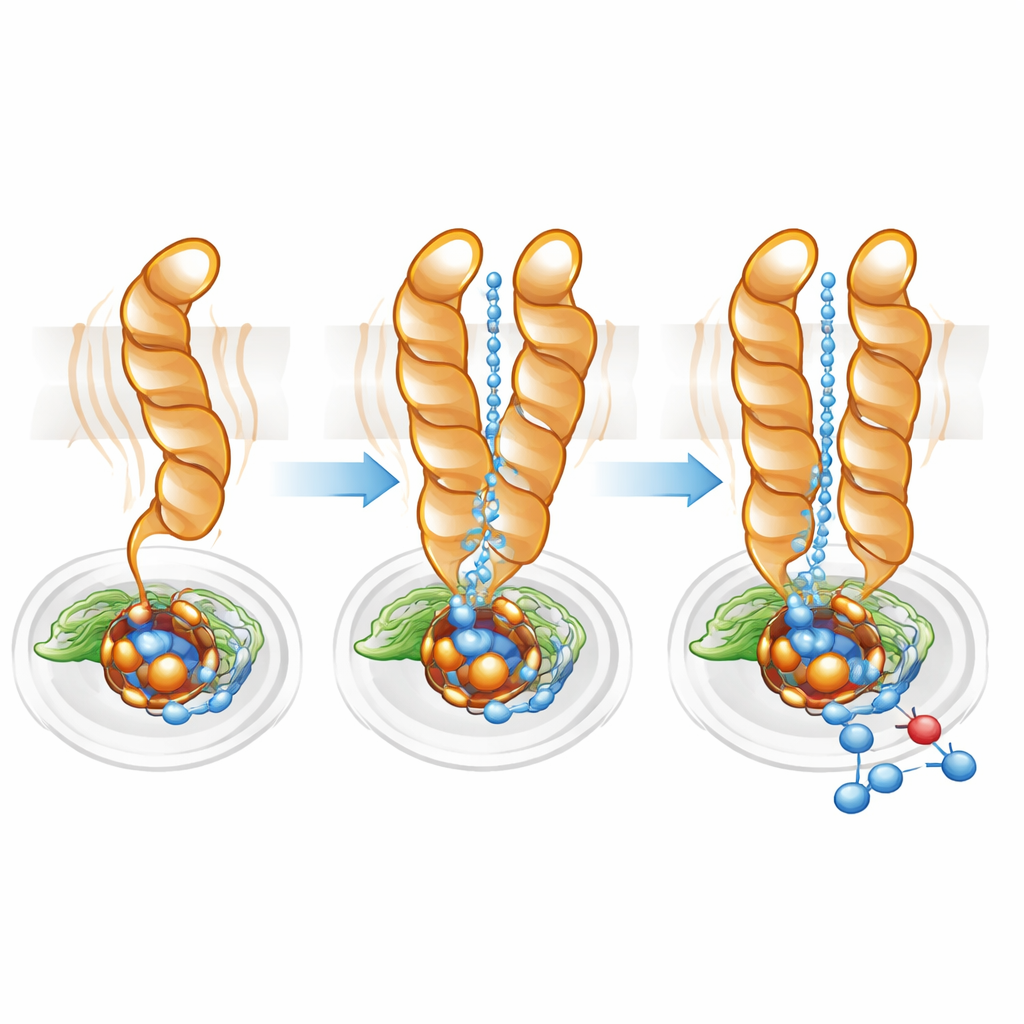
Finjustering av protonmotorvägen
Protoner—positivt laddade vätejoner—måste levereras effektivt från cellens insida till den begravda aktiva ytan för att reduktion av kvävemonoxid ska kunna fortskrida. Med vägkartläggningsprogram fann teamet en hydrofil kavitet som förbinder cytoplasman med den aktiva ytan i både monomer och dimer. I monomeren var dock denna kanal bredare och mer diffus, i linje med TM10:s större rörlighet. I dimeren hjälpte TM10:s låsta position och den gynnsamma orienteringen av Glu563 att definiera en mer direkt, bättre organiserad väg. Att mutera Glu563 till aminosyror som inte kan bilda samma interaktioner sänkte enzymets aktivitet till under 10 % av det normala och destablerade också dimeren, medan mutationer på närliggande positioner minskade mängden av det viktiga icke-hemsiska järnet vid den aktiva ytan. Tillsammans visar dessa resultat att dimerbildning och den precisa positioneringen av Glu563 och Glu494 är tätt kopplade till både strukturell integritet och katalytisk effektivitet.
Från strukturella insikter till nya behandlingar
Resultaten avslöjar en tydlig kedja från proteinparning vid membranytan till fina justeringar djupt inne i den aktiva ytan som styr hur effektivt qNOR avlägsnar kvävemonoxid. Enkelt uttryckt: när två kopior av enzymet griper i varandra rätas en flexibel segment ut och stelnar, vilket hjälper till att styra protoner in i reaktionscentret och öka enzymets aktivitet. För läkemedelsutveckling antyder detta en okonventionell strategi: i stället för att blockera den aktiva ytan direkt skulle man kunna designa molekyler som kilar isär dimern eller stör interaktionen mellan Glu563 och Glu494, vilket tvingar enzymet in i dess långsamma monomeriska tillstånd. Eftersom qNOR och närbesläktade enzymer är avgörande för överlevnaden hos flera farliga, läkemedelsresistenta patogener, kan sådana strukturstyrda angreppssätt bidra till nästa generation av riktade antimikrobiella medel.
Citering: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Nyckelord: avgiftning av kvävemonoxid, bakteriell respiration, membranproteiner, kryoelektronmikroskopi, mål för antimikrobiella läkemedel