Clear Sky Science · sv
Rumslig multiomik avslöjar irreversibel elektroporations inducerade immunometaboliska egenskaper hos den inflammatoriska marginalen vid levercancer
Varför en ny behandling för levercancer kräver närmare granskning
Irreversibel elektroportation (IRE) är ett nyare sätt att förstöra levertumörer med korta, högspänningspulser istället för värme. Eftersom metoden kan skona närliggande blodkärl och gallgångar är den särskilt användbar för tumörer i känsliga lägen. Ändå återkommer tumören intill det behandlade området hos upp till en tredjedel av patienterna. Den här studien undersöker vad som händer i det smala gränsområdet efter IRE — och om dolda förändringar i immunceller och cellernas metabolism där tyst kan bana väg för att cancer ska växa tillbaka.
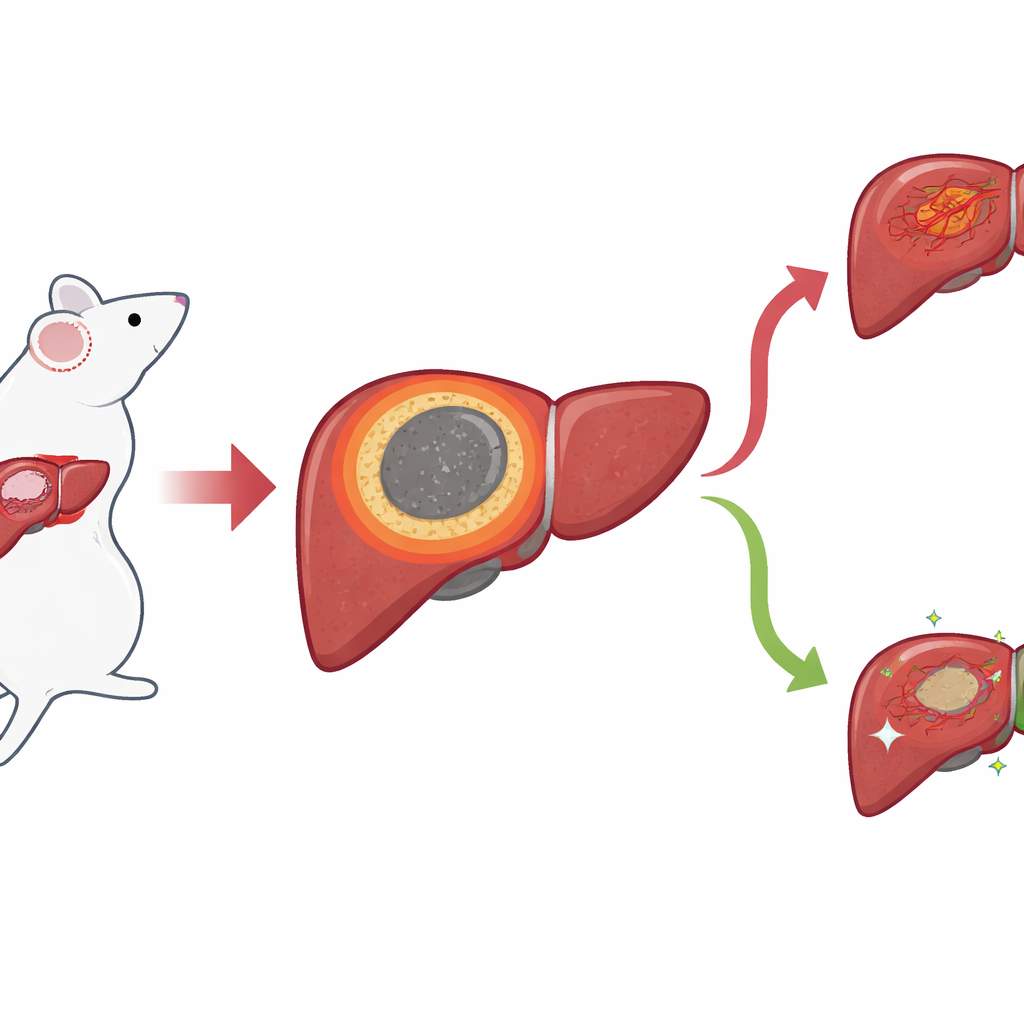
En smal gräns med stora följder
Med en musmodell för levercancer fokuserade forskarna på den tunna ring av vävnad som uppstår mellan den döda, ablaterade kärnan och den omgivande friska levern efter IRE. De kallar detta den inflammatoriska marginalen, eller IM. Standardmikroskopiska bilder visade att denna zon ligger exakt där lokala återfall vanligtvis uppträder, men dess gränser var svåra att avgränsa med blotta ögat. För att få en skarpare bild använde teamet rumsliga metoder som läser av vilka gener och små molekyler som finns närvarande samtidigt som deras läge i vävnaden bevaras. Med rumslig transkriptomik kartlade de genaktivitet punkt för punkt och upptäckte en distinkt kluster av punkter som överensstämde exakt med IM och skiljde den nekrotiska kärnan från normal lever- och tumörområden.
Immunceller samlas — men många bromsar angreppet
Forskarna använde sedan single‑cell och single‑nucleus RNA‑sekvensering tillsammans med en kraftfull profileringsmetod kallad CyTOF för att katalogisera individuella celltyper i levern. De fann att IM domineras av en typ av immuncell kallad makrofager. Särskilt en undergrupp som liknar "lipidassocierade makrofager" (LAMs) strömmade in i IM inom dagar efter IRE. Dessa celler bär ytantigener och genuttryckssignaturer kopplade till immunundertryckande funktioner, inklusive höga nivåer av PD‑L1, en molekyl känd för att dämpa T‑cellsresponser. Genuttrycksanalyser antydde att dessa makrofager är skickliga på att uppta material, svara på kemiska attraktanter och skicka ut signaler som kan hämma de T‑celler som behövs för att döda cancerceller. Avbildning bekräftade att PD‑L1‑positiva makrofager var betydligt vanligare i IM än i närliggande normal vävnad.
En hotspot av förändrad fettkemi
Nästa steg var att lägga detta immunlandskap över rumslig metabolomik, en masspektrometribaserad avbildningsmetod som kartlägger fördelningen av hundratals små molekyler. De visade att IM har ett metabolt fingeravtryck som skiljer sig från både den döda kärnan och den omgivande levern. I denna smala zon var många lipidrelaterade vägar starkt uppreglerade, inklusive produktion av omättade fettsyror, arakidonsyraderivat och sfingolipider. Viktiga signalerande fetter såsom prostaglandiner och leukotriener, härledda från arakidonsyra, var berikade i IM, medan andra enzymvägar för bearbetning av samma molekyl var relativt dämpade. En annan lipidfamilj, sfingolipider — inklusive ceramider och sfingomyeliner — ackumulerades också, understödda av ökat uttryck av de enzymer som syntetiserar och omvandlar dem.
En stegvis förskjutning från skada till bränslerik nisch
Genom att dela upp den inflammatoriska marginalen i tre tunna lager från den nekrotiska kärnan och utåt såg forskarna en gradvis förändring i kemin. Närmast den döda zonen var komplexa lipider och kolesterolrelaterade molekyler som högst, medan längre ut ökade små energirelaterade molekyler såsom glukos och vissa aminosyror. Detta mönster tyder på att vävnaden över ett kort avstånd övergår från ett lipidfyllt, signalrikt miljö till en som är inriktad på att tillhandahålla bränsle för överlevnad och tillväxt. Författarna föreslår att denna stegvisa omprogrammering hjälper till att upprätthålla de lipidkrävande, immunosuppressiva makrofager som dominerar IM och möjligen tyst förbereder marken för att tumörceller ska åter etablera sig.
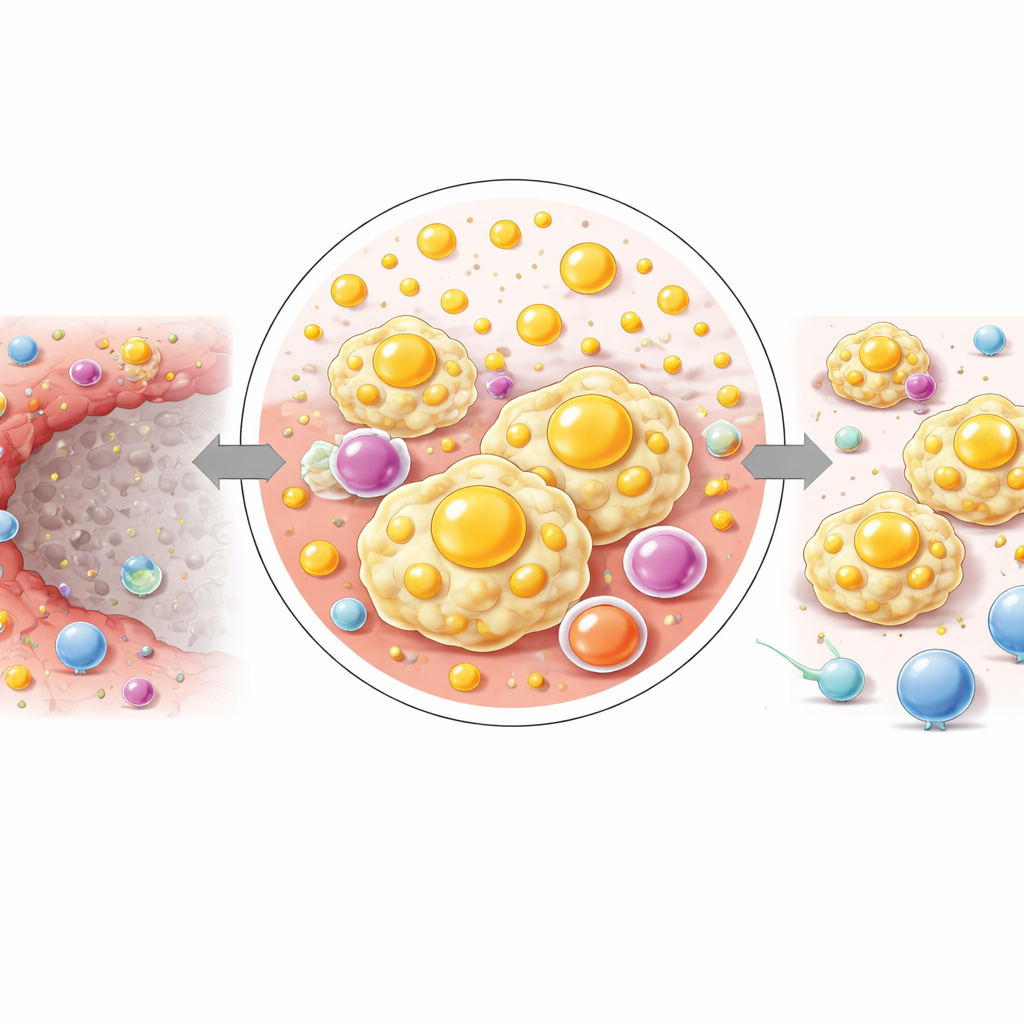
Vad detta innebär för framtida vård vid levercancer
Enkelt uttryckt visar detta arbete att IRE gör mer än att bara döda tumörceller: det skapar också en smal ring av vävnad där immunceller och fettkemi tillsammans bygger ett skärmat, tumörvänligt kvarter. Makrofager i denna zon är rikliga, fyllda med lipider och inriktade på att stänga av T‑celler snarare än att stödja dem. Eftersom dessa förändringar är tätt kopplade till specifika metaboliska vägar antyder de nya behandlingsmöjligheter. Att kombinera IRE med läkemedel som riktar in sig på lipidmetabolism eller blockerar PD‑L1 i denna marginal skulle i princip kunna förvandla en återfallsbenägen gräns till en zon som verkligen avslutar jobbet mot levercancer.
Citering: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Nyckelord: levercancer, tumörablation, immunt mikroklimat, makrofager, lipidmetabolism