Clear Sky Science · sv
Ytdekoration av bakterier skapar robusta levande terapeutika för förbättrad behandling av ulcerös kolit
Förvandla vänliga bakterier till små kroppsvakter
Ulcerös kolit är en smärtsam tarmsjukdom där kroppens egen tarm blir kroniskt inflammerad, vilket leder till trängande diarré, blödningar och kraftigt försämrad livskvalitet. Läkare och patienter är entusiastiska över ”goda bakterier”-kapslar som skulle kunna dämpa denna inflammation inifrån, men de flesta av dessa mikrober dör på den hårda färden genom magsäcken och tunntarmen innan de når tjocktarmen, där de behövs. Denna studie beskriver ett nytt sätt att klä probiotiska bakterier i ett skyddande pansar så att de säkert kan passera matsmältningskanalen, slå sig ned i tjocktarmen och hjälpa till att reparera den skadade tarmen.
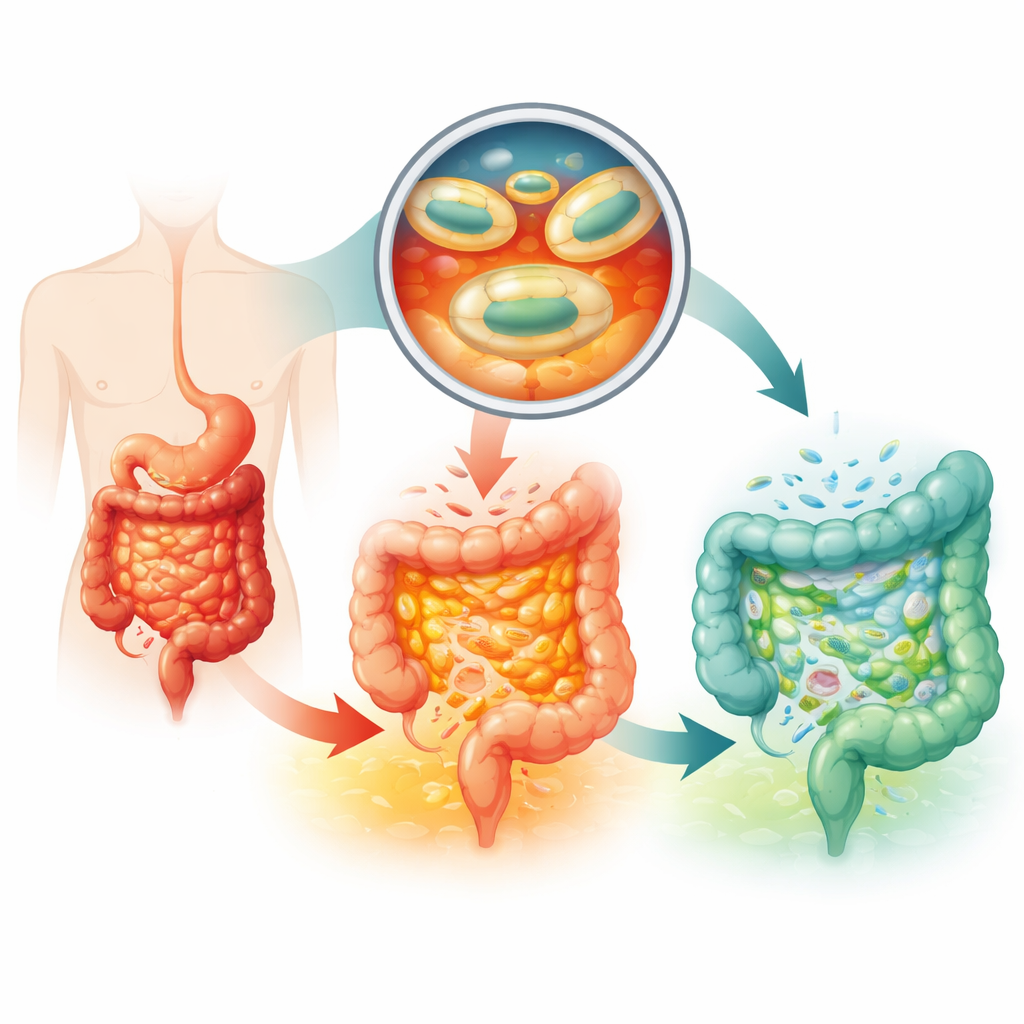
Varför nuvarande probiotika ofta brister
Standardbehandlingar för ulcerös kolit förlitar sig på antiinflammatoriska och immunhämmande läkemedel som kan ha allvarliga biverkningar och inte fungerar för alla. Probiotika erbjuder en mildare strategi genom att hjälpa till att återbalansera tarmens mikrobiella samhälle. En särskild stam av Escherichia coli kallad Nissle 1917 är redan godkänd som medicin för denna sjukdom, men patienter måste svälja mycket stora doser varje dag, och även då är fördelarna blygsamma. Nyckelproblemet är överlevnad och leverans: magsyra, matsmältningsenzymer och snabb transit genom övre tarmar dödar eller sköljer bort de flesta bakterier innan de kan fästa och växa i tjocktarmen, där mer än 99 % av tarmmikroberna normalt finns.
Bygga ett skyddande skal runt hjälpsamma bakterier
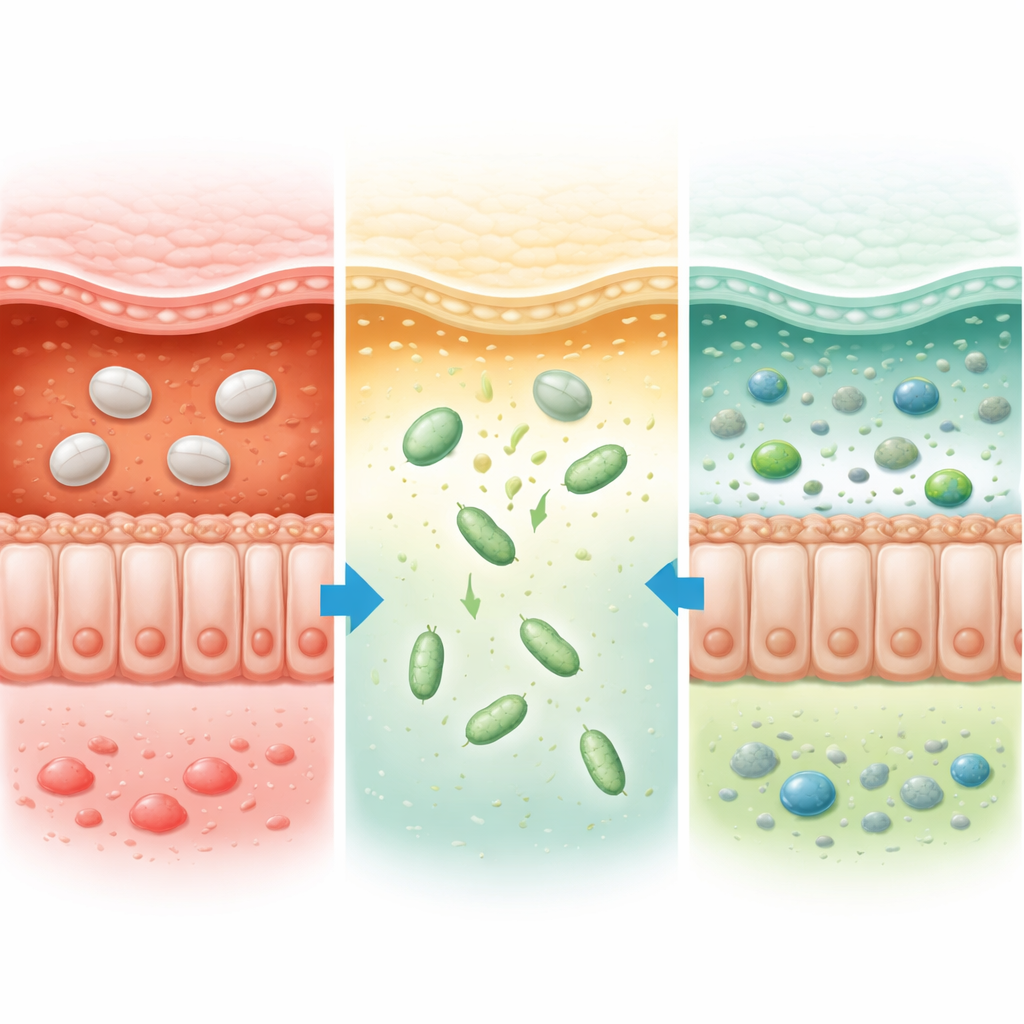
För att lösa detta skapade forskarna en tunn, smart beläggning runt varje probiotisk cell med ett växtbaserat material kallat lignin. De kemiskt modifierade ligninet för att göra det mer lösligt och känsligt för förändringar i surhetsgrad, vilket gav ett ämne som är stabilt i stark syra men faller isär i den mer neutrala miljön i tjocktarmen. Med en skonsam lager-för-lager-process tillsatte de först kalciumjoner till probiotikans yta och svepte sedan in den med det modifierade ligninet, vilket bildade ett slätt ”pansar” ungefär en tiotusendels millimeter tjockt. Mikroskopi och partikelstorleksmätningar visade att detta skyddade bakterierna utan att döda dem, och metoden fungerade på flera mycket olika bakteriearter, vilket tyder på att den kan fungera som en generell plattform för många probiotiska terapier.
Rikta in sig på tjocktarmen och främja läkning
När de testades i simulerade matsmältningsvätskor förstördes obskyddade bakterier snabbt av magsyran, medan bepansrade bakterier överlevde i timmar och bara släppte ut sitt innehåll effektivt vid pH-nivåer som liknar tjocktarmens. Hos möss med kemiskt inducerad ulcerös kolit ackumulerades de belagda bakterierna starkt i tjocktarmen, medan obelagda bakterier eller enkla blandningar med beläggningsmaterialet till stor del misslyckades med detta. Teamet använde fluorescensavbildning, gentester och matematisk modellering för att visa att de skyddade bakterierna inte bara anlände till tjocktarmen intakta utan också förökade sig där och nådde ungefär en av tusen av alla tarmmikrober. Behandlade möss tappade mindre vikt, behöll längre tjocktarmar och hade mycket friskare tarmslemhinna under mikroskopet, med tätare cellförbindelser och ett återställt slem lager som tillsammans bildar en avgörande barriär mellan kroppen och tarminnehållet.
Lugna immunförsvaret och återbalansera mikrobiomet
Bortom fysisk reparation omformade de bepansrade probiotika det immunologiska och mikrobiella landskapet i den sjuka tarmen. I blodet och tjocktarmen hos sjuka möss var nivåerna av inflammatoriska molekyler höga och nivåerna av en nyckel antiinflammatorisk signal låga; den nya behandlingen vände dessa trender och skiftade immunförsvaret mot ett lugnare tillstånd. Detaljerade cellanalyser visade förändringar i mixen av immunceller i både tjocktarm och mjälte. Samtidigt visade DNA-sekvensering av tarmmikrober att terapin ökade den totala mikrobiella mångfalden och förstärkte förekomsten av flera bakteriegrupper kopplade till tarmhälsa, inklusive Akkermansia och Muribaculum. Metabolitprofilering visade vidare breda förändringar i små molekyler kopplade till vitamin-, fettsyre- och aminosyremetabolism, vilket tyder på att det återbalanserade mikrobiomet producerade en kemisk miljö mer kompatibel med läkning.
Från muskstudie till framtida levande läkemedel
Sammanlagt visar arbetet att ge probiotika ett pH-känsligt pansar kan pålitligt föra dem genom matsmältningssystemets prövningar och leverera dem dit ulcerös kolit gör mest skada. Hos möss möjliggjorde denna strategi att mycket lägre doser av bakterier kunde kolonisera tjocktarmen, reparera tarmbarriären, minska skadlig inflammation och återställa ett hälsosammare mikrobielt samhälle och metabolisk profil. Eftersom den växtbaserade beläggningen i stort sett passerar genom kroppen oförändrad och metoden kan tillämpas på många bakterietyper, menar författarna att deras tillvägagångssätt erbjuder en brett användbar modell för att utforma nästa generationens ”levande” läkemedel för ulcerös kolit och andra sjukdomar i tjocktarmen.
Citering: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
Nyckelord: ulcerös kolit, probiotika, tarmmikrobiom, läkemedelsleverans, intestinal barriär