Clear Sky Science · sv
NRF2-aktivatorer och hämmaren av nukleär export, selinexor, begränsar coronavirus genom att rikta in sig på ett nätverk som involverar ACE2, TMPRSS2 och XPO1 via en NRF2-oberoende mekanism
Läkemedel som hjälper celler säga ”nej” till coronavirus
De flesta coronavirusbehandlingar idag riktar sig mot viruset självt. Men virus är mästare på förändring, och nya varianter kan snabbt minska effektiviteten hos sådana läkemedel. Denna studie utforskar en annan strategi: att göra våra egna celler mindre välkomnande för både farliga coronavirus som SARS-CoV-2 och mildare säsongsstammar. Genom att justera hur celler hanterar några få nyckelproteiner som fungerar som grindvakter visar forskarna att redan tillgängliga småmolekyler kraftigt kan minska infektion i laboratoriemodeller — och att de gör detta på ett sätt som inte bygger på den vanliga antivirala vägen de blev kända för.
En ny vinkel på coronavirusförsvar
Teamet fokuserade på föreningar kända för att aktivera ett cellulärt skyddsprogram som styrs av proteinet NRF2. Dessa föreningar — 4-oktyl itaconat (4OI), bardoxolon (BARD) och sulforafan (SFN) — testades tillsammans med selinexor (SEL), ett läkemedel som blockerar ett transportprotein som heter XPO1, vilket hjälper till att föra andra proteiner ut ur cellkärnan. I lung- och njurcellmodeller sänkte alla fyra läkemedlen SARS-CoV-2-nivåerna utan att skada cellerna. De fungerade också mot flera varianter av oro. Överraskande nog, när NRF2 genetiskt avlägsnades, replikerade virusen faktiskt bättre, vilket visar att NRF2 är naturligt skyddande — men läkemedlen fungerade fortfarande bra, vilket visar att deras antivirala effekt kommer via en annan väg. 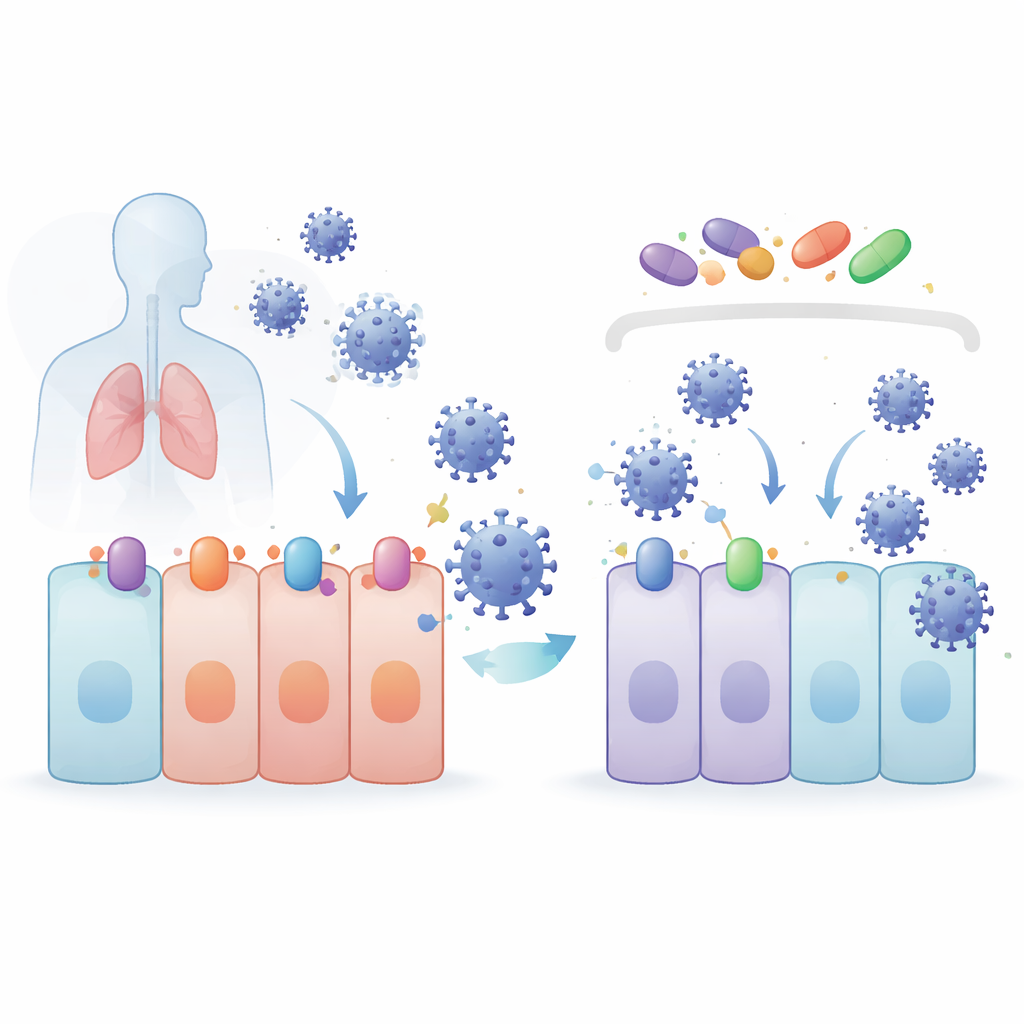
Stänga virusets främre dörr
Coronavirus påbörjar infektion genom att fästa vid receptorproteiner på cellens yta. För SARS-CoV-2 och dess närmaste släktingar är huvuddörren ACE2, med hjälp av ett klyvande enzym som heter TMPRSS2. Exportproteinet XPO1 verkar också underlätta infektion. Forskarna fann att 4OI, BARD, SFN och SEL alla minskade mängderna ACE2, TMPRSS2 och XPO1 i mänskliga lungceller. 4OI och SEL var särskilt effektiva när de var närvarande innan infektion, och de blockerade inträdet av virusliknande partiklar täckta med coronavirusspikeproteiner. Med andra ord: dessa läkemedel bromsar inte bara viruset efter att det tagit sig in — de hjälper till att ta bort låsen och handtagen som viruset behöver för att öppna dörren från början.
Hur celler demonterar viktiga virushjälpare
Genom att gräva djupare visade teamet att 4OI påskyndar nedbrytningen av ACE2-protein. Under normala förhållanden varar ACE2 i många timmar; med 4OI försvann det från cellytan på en bråkdel av den tiden. Denna nedbrytning krävde två cellulära märkare, NEDD4L och MDM2, som fäster molekylära ”släng mig”-flaggor på proteiner. Att blockera dessa märkare försvagade 4OI:s förmåga att eliminera ACE2. Överraskande nog var den vanliga proteinnedbrytande apparaten, proteasomen, inte huvudvägen. Istället styrdes ACE2 in i cellens återvinnings- och avfallssystem, lysosomen. Läkemedlen sänkte också genaktiviteten för ACE2 och XPO1, delvis genom att minska aktiveringen av STAT3, ett protein som normalt ökar läsningen av ACE2-genen. 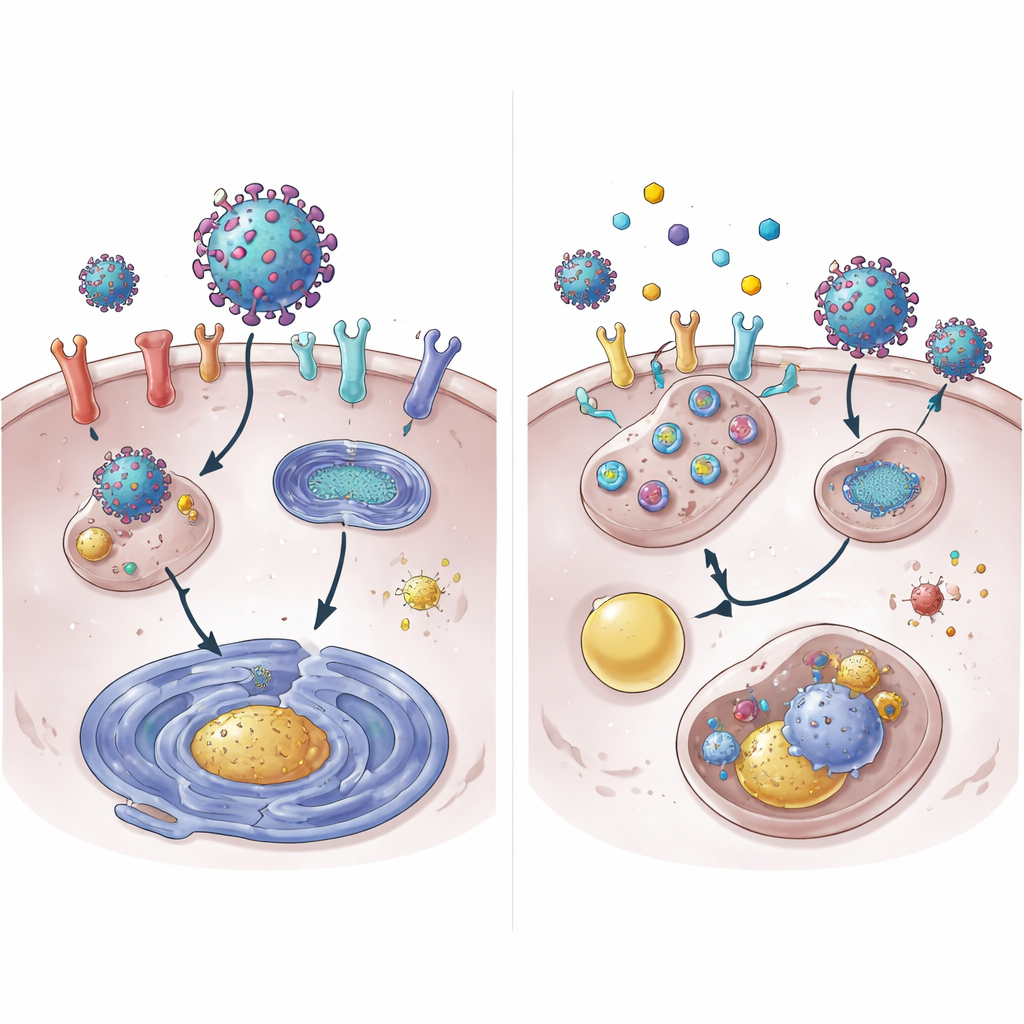
Säsongsbetonade coronavirus och XPO1-anslutningen
Forskarna vände sig sedan till hCoV-229E, ett säsongscoronavirus som vanligtvis orsakar lindriga förkylningar men som kan vara farligt för personer med nedsatt immunförsvar. Genom att använda konstruerade virus som lyser när de replikerar visade de att alla fyra föreningarna starkt undertryckte 229E i lung- och blodkärlsceller, även när NRF2 saknades. Till skillnad från SARS-CoV-2 använder detta virus en annan receptor, ANPEP, som läkemedlen inte påverkade. Istället korrelerade deras effekt tätt med hur starkt de minskade XPO1. Att slå ner XPO1 i sig minskade kraftigt 229E-replikation, och selinexors effekt försvann nästan i dessa XPO1-fattiga celler. Denna rangordning — SEL mest beroende av XPO1, BARD minst — antyder att varje förening har en något olika mix av mål, med XPO1 som en central nav för många av deras antivirala effekter.
Vad detta kan betyda för framtida behandlingar
För icke-specialister är huvudbudskapet att det är möjligt att bekämpa coronavirus inte bara genom att attackera viruset, utan genom att varsamt omprogrammera våra egna celler så att de blir svårare att infekteras. I laboratorieodlade humana celler strippade de studerade föreningarna bort avgörande dockningsställen och hjälpvärdar som SARS-CoV-2 och ett vanligt förkylningsvirus förlitar sig på, och de gjorde detta till stor del utan den NRF2-väg som först gjorde dem intressanta. Även om dessa fynd fortfarande är prekliniska och ännu inte direkt kan omvandlas till läkemedel, lyfter de fram en lovande väg: läkemedel som samtidigt minskar viral entry, dämpar skadlig inflammation och skyddar vävnader genom att rikta in sig på ett delat nätverk av värdproteiner som ACE2, TMPRSS2 och XPO1.
Citering: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Nyckelord: värdriktade antivirala medel, coronavirusinträde, ACE2 och TMPRSS2, NRF2-aktivatorer, hämmning av XPO1