Clear Sky Science · sv
En tvåstegsaktinmedierad strategi gör det möjligt för Campylobacter jejuni att främja mitokondrieaggregation och järnhomeostas för intracellulär överlevnad och persistens
Varför denna lilla kamp inne i celler spelar roll
Matförgiftning från underkokt kyckling tillskrivs ofta en bakterie som heter Campylobacter jejuni. De flesta återhämtar sig, men mikroben är förvånansvärt duktig på att överleva i många miljöer, vilket underlättar spridning från gård till tallrik. Denna studie undersöker vad som händer när bakterien gömmer sig inne i en frittlevande amöba — en vanlig sötvattensmikroorganism — och avslöjar ett förvånansvärt sofistikerat överlevnadstrick som kretsar kring omformning av cellens inre skelett, klustring av energiproducerande "kraftpaket" kallade mitokondrier, och kontroll av järn samt skadlig syrefysik. Att förstå denna dolda fas i dess livscykel kan peka på nya sätt att minska kontaminering innan bakterien når människor.
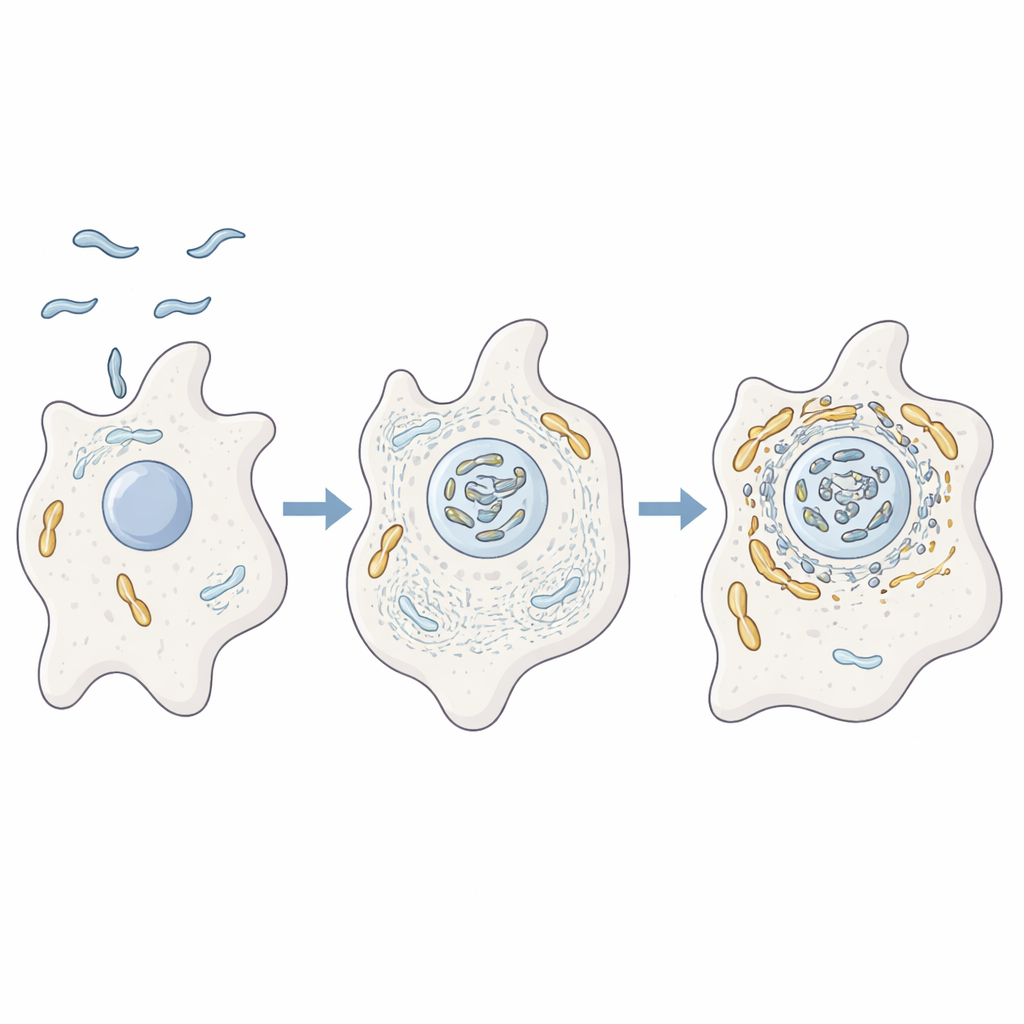
En mikroorganism som tränar inne i amöbor
Författarna studerade hur C. jejuni beter sig inne i amöban Acanthamoeba castellanii, en encellig organism som lever i jord och vatten. Dessa amöbor fungerar som träningsfält för många sjukdomsframkallande bakterier och erbjuder skydd från hårda förhållanden och desinfektionsmedel. Med avancerad proteomanalys, mikroskopi och genetiska mutanter visade forskarna att när C. jejuni infekterar amöbor hamnar den tätt associerad med värdcellens mitokondrier. Samtidigt är amöbans inre skelett av aktin, tillsammans med proteiner som reglerar form och rörelse, starkt förhöjt nära dessa mitokondrier, vilket tyder på att bakterien aktivt omorganiserar värdcellens inre arkitektur.
Böja cellens skelett för att flytta kraftpaket
För att testa om aktin verkligen driver denna interaktion blockerade teamet aktin från att bilda filament eller att förgrenas till nätverk. Under dessa förhållanden samlades inte mitokondrierna nära bakterierna utan förblev istället utspridda punkter, och bakteriens överlevnad minskade. De koncentrerade sig sedan på två bakteriella hjälpproteiner, CiaD och CiaI, som injiceras i värdceller genom bakteriens flagell, en piskliknande svans. CiaD visade sig främja aktintillväxt och skapa taggiga utskott på amöbans yta, vilket hjälpte cellen att fånga upp bakterierna. När de väl var inne observerades att mitokondrier klustrade runt det bakterieinnehållande rummet på ett aktinberoende sätt, vilket placerade bakterien i en privilegierad zon rik på värdens energimaskineri.
En molekylär strömbrytare som omformar mitokondrier
Medan CiaD är avgörande för inträde, styr CiaI vad som händer därefter. När forskarna tog bort genen för CiaI utlöste C. jejuni inte längre stark mitokondrieklustring och överlevde dåligt inne i amöbor. Tillsättning av renat CiaI bundet till små pärlor, utan några levande bakterier, var tillräckligt för att få närliggande mitokondrier att fusionera och klustra samt lokalt ta bort aktin. Biokemiska tester visade att CiaI binder energibärande molekyler på ett kooperativt sätt och beter sig som en molekylär strömbrytare som kan slå på eller av sin aktivitet beroende på förhållanden inne i värden. Författarna föreslår att efter att CiaD‑driven aktintillväxt fört mitokondrier nära, driver CiaI lokal aktinnedbrytning och omformar mitokondrienätverket till täta aggregat som omger det bakterieinnehållande rummet.
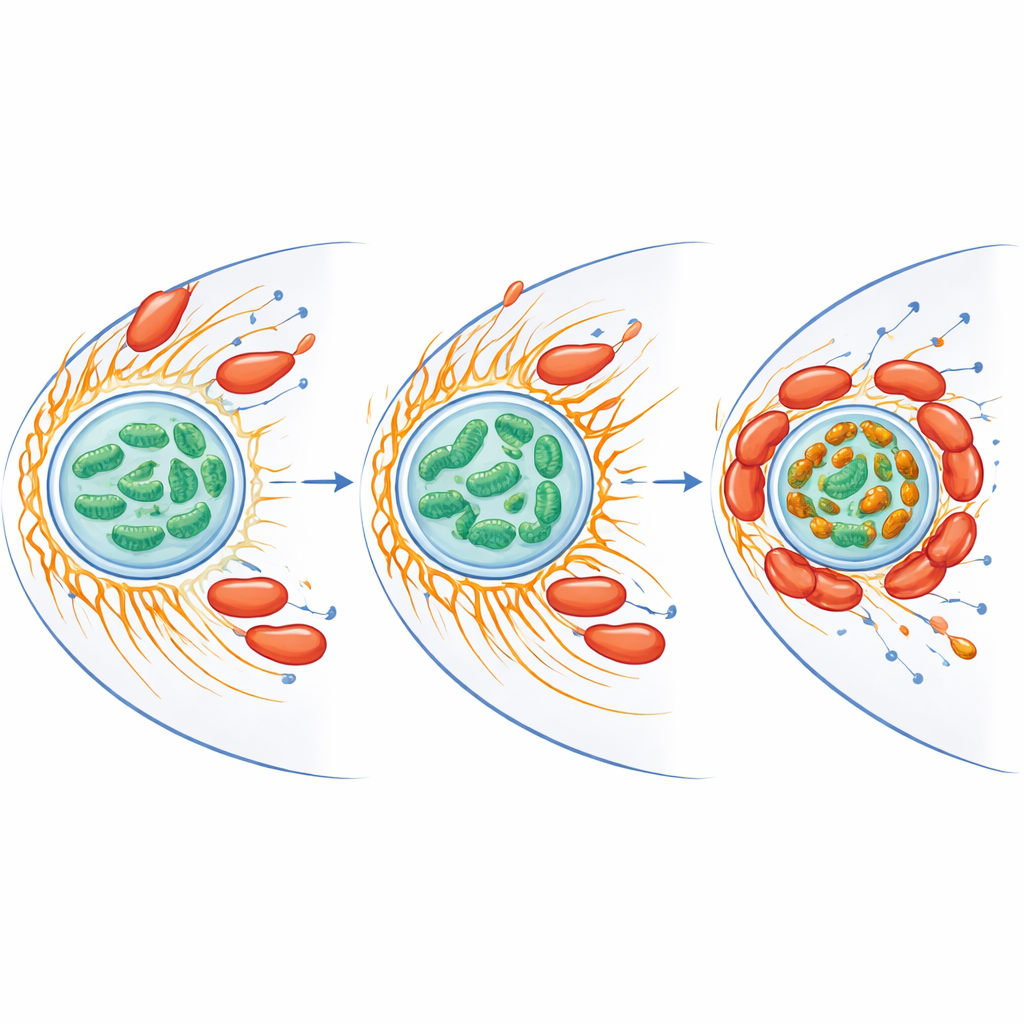
Omlänkning av järn och stress inne i värdcellen
Mitokondrier gör mer än att producera energi — de hanterar också järn och producerar reaktiva syreradikaler, kemiskt aggressiva former av syre som kan döda mikrober. Forskarna fann att infektion minskade mängden fritt järn i mitokondrierna som helhet men samtidigt skapade ljusa järnrika kluster där mitokondrierna klustrade runt bakterierna. Proteiner som är involverade i järnhantering och i försvar mot oxidativ stress ökade både i värden och i bakterien. När teamet avlägsnade fritt järn med en kelaterande förening minskade amöbans utsläpp av reaktiva syreradikaler och C. jejuni överlevnad ökade dramatiskt. Mitokondrier i infekterade celler visade också högre membranpotential, ett tecken på förhöjd aktivitet, vilket tyder på att bakterien skjuter värdens kraftpaket mot ett tillstånd som gynnar dess egen persistens samtidigt som skadlig syrefysik begränsas.
Vad detta betyder för livsmedelssäkerhet och infektion
Tillsammans stöder resultaten en tvåstegsstrategi: först stimulerar CiaD aktintillväxt för att hjälpa bakterien att komma in i amöbor och att dra mitokondrier mot inträdesplatsen; andra steget är att CiaI lokalt demonterar aktin och omformar mitokondrier till järnrika kluster som omsluter det bakterieinnehållande rummet, samtidigt som värdens oxidativa försvar dämpas. Denna finjusterade kontroll av cellform, energianvändning och metallbalans hjälper C. jejuni att överleva inne i amöbor och bidrar sannolikt till dess förmåga att bestå i miljön och senare infektera människor. Genom att avslöja nyckelspelarna i detta mikroskopiska dragkamp pekar studien på nya mål — såsom Cia‑proteinerna, kontaktpunkter mellan aktin och mitokondrier eller järnhanteringsvägar — som skulle kunna störas för att minska kontaminering och sjukdom.
Citering: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Nyckelord: Campylobacter, amoebae, mitochondria, actin cytoskeleton, iron homeostasis