Clear Sky Science · sv
Flerlagrad reglering av GluK3-kainatreceptorer medierad av Neto-subenheter och zink
Varför små hjärnbrytare spelar roll
Varje tanke, minne och sinnestillstånd i hjärnan bygger på mikroskopiska brytare som tillåter laddade partiklar att strömma in och ut ur nervceller. Denna studie fokuserar på en sådan brytare, en relativt okänd receptor kallad GluK3. Genom att avslöja hur partnerproteiner och zinkjoner finjusterar GluK3:s beteende ger arbetet ledtrådar till hur hjärnkretsar håller jämvikt — och hur den jämvikten kan rubbas vid tillstånd som epilepsi, depression och schizofreni.
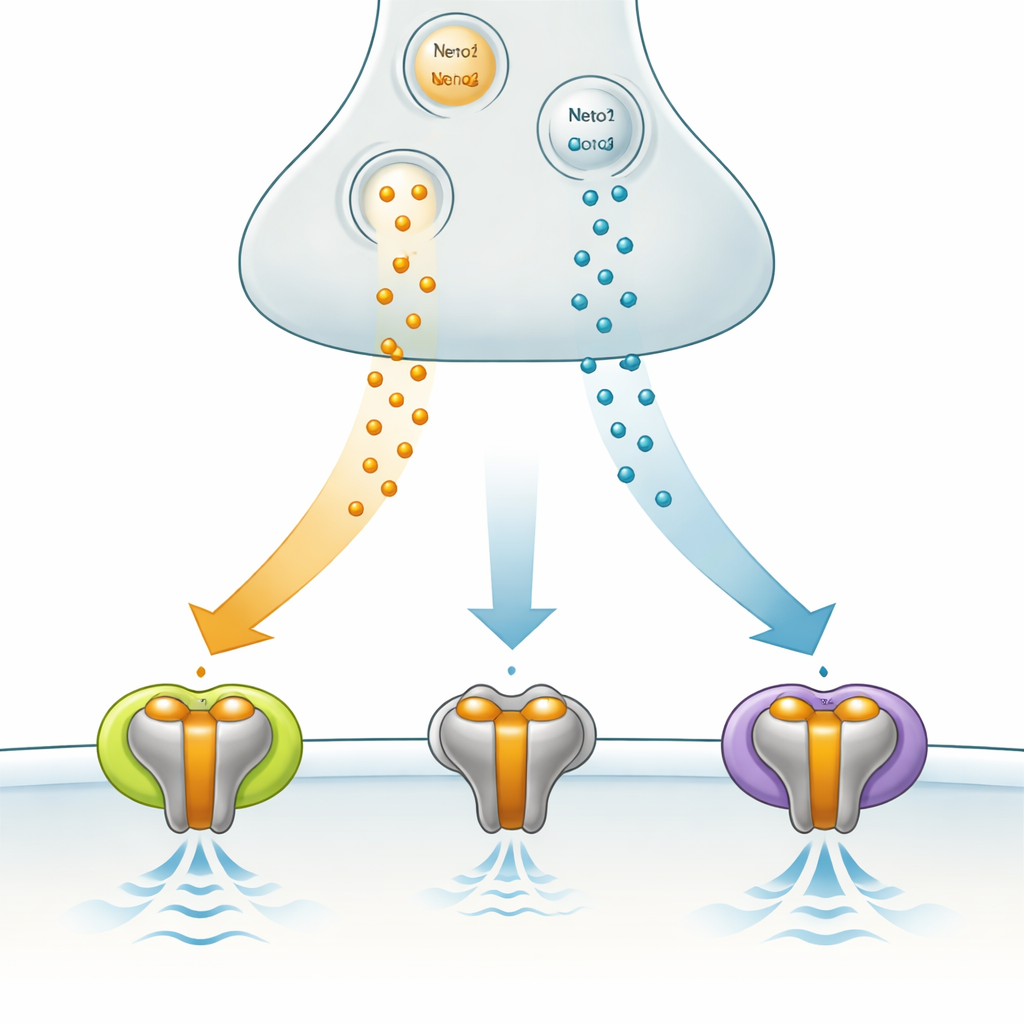
En specialiserad signalport i hjärnan
GluK3 tillhör kainatreceptor-familjen, en del av den större gruppen glutamatreceptorer som medierar snabb kommunikation mellan neuroner. Till skillnad från några av sina släktingar slår GluK3 inte bara på eller av signaler; den fungerar mer som ett filter som svarar bäst på korta, kraftiga utbrott av signalsubstansen glutamat. Den är rikligt förekommande i hjärnregioner som hippocampus, viktig för minne och nätverksrytmer, och förändringar i GluK3-funktion har kopplats till ångestrelevanta beteenden. Dessa egenskaper gör GluK3 till ett lovande, men fortfarande dåligt förstått, mål för att påverka hjärnaktivitet vid hälsa och sjukdom.
Hjälpproteiner som drar i trådarna
Forskargruppen undersökte hur två hjälpproteiner, Neto1 och Neto2, ändrar GluK3-beteende i humana celler konstruerade för att producera dessa komponenter. Båda hjälparna förlängde hur snabbt GluK3 stängs av efter aktivering, och båda minskade en naturlig form av intern blockering som normalt begränsar strömflödet. De hade emellertid motsatta effekter på hur snabbt GluK3 kan återanvändas. Med Neto1 återhämtade sig receptorerna snabbt och var redo att reagera på snabba, upprepade signaler. Med Neto2 blev återhämtningen mycket långsammare, vilket gynnade integration av signaler över längre tidsintervall. I praktiken kan en synaps genom att välja olika hjälpproteiner bestämma om GluK3 ska fungera som en snabbdetektor eller en långsammare, genomsnittande sensor.
Zink som ett andra kontrolllager
Många glutamatfrisättande nervterminaler släpper också ut zink, som kan binda till receptorer och förändra deras funktion. Tidigare arbete visade att zink ovanligt nog stärker GluK3-aktivitet, samtidigt som det tenderar att dämpa andra receptortyper. Här fann författarna att denna förstärkning starkt beror på vilken Neto-proteinvariant som är närvarande. När GluK3 agerar ensam fördubblar zink ungefär den tid receptorn förblir aktiv och ökar strömmen måttligt. Tillsats av Neto1 dämpar denna effekt. Däremot samverkar zink och Neto2 när GluK3 paras med Neto2 för att kraftigt öka strömmen, mycket mer än någon av dem kan göra var för sig. Detta tyder på att synapser rika på Neto2 och zink kan starkt förstärka GluK3-medierade signaler vid intensiv aktivitet, medan Neto1-rika synapser förblir mer återhållsamma.
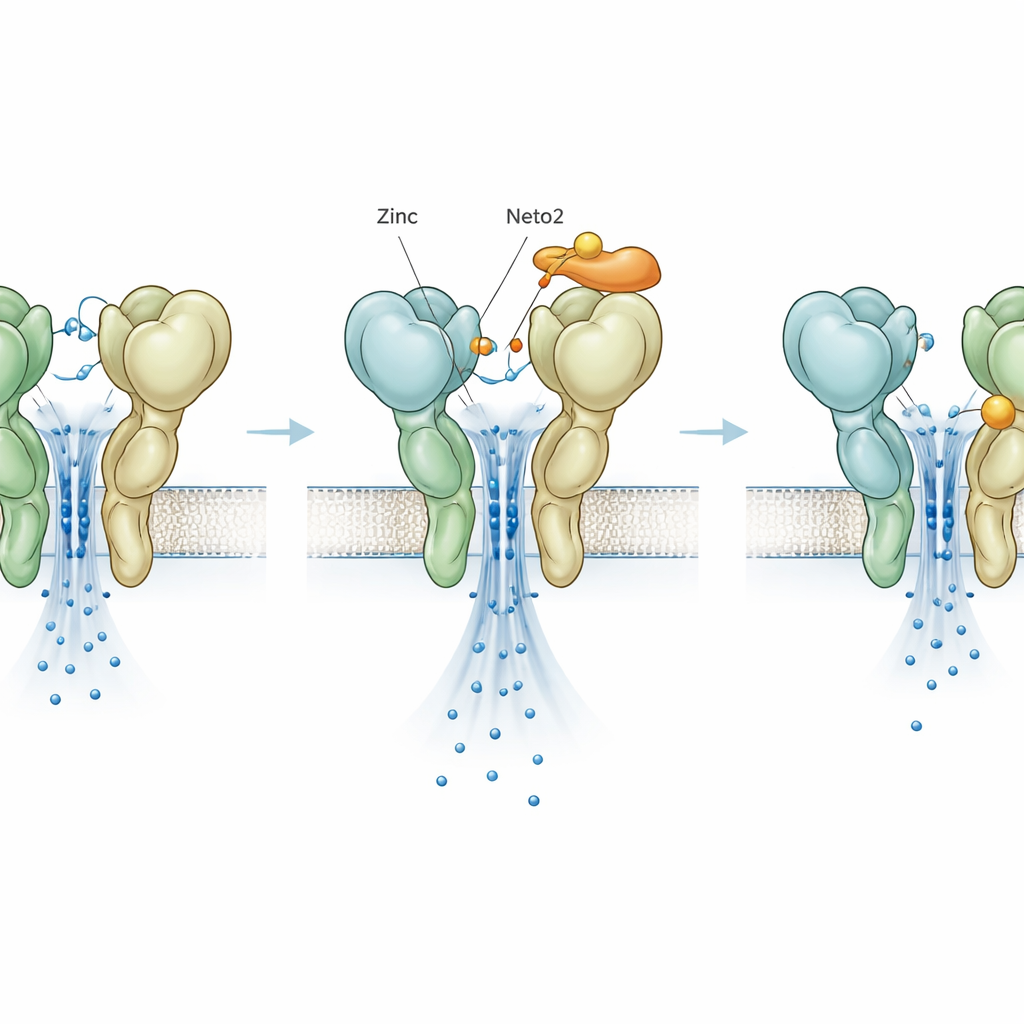
En dold broms avslöjad genom mutation
För att skilja zinkets verkan från hjälpproteinernas konstruerade forskarna en enkelbokstavsförändring i GluK3, kallad D759G, som tar bort en känd zinkbindningsplats. Som väntat gjorde denna mutation i sig receptorn mer stabil och långsammare att stänga av, vilket efterliknade den vanliga effekten av zink. Förvånande nog, när zink tillsattes till denna mutant, förstärkte det inte längre aktiviteten; istället snabbbade det upp avstängningen och minskade strömmen, vilket avslöjade en andra, tidigare dold zinkplats som fungerar som en broms. Neto1 och Neto2 utövade fortfarande sina karakteristiska effekter på mutanten, vilket visar att deras grundläggande påverkan inte beror på den ursprungliga zinkplatsen. Även denna nyupptäckta hämmande zinkverkan var dock olika justerad av de två hjälparna, vilket adderar ytterligare en ställbar ratt i systemet.
Att se struktur bakom beteende
För att koppla funktion till form använde teamet kryoelektronmikroskopi för att visualisera den mutanta GluK3-receptorn frusen i ett icke-aktivt tillstånd. Bilderna visade att den region som binder glutamat bildar en mer kompakt, tätt packad enhet i D759G-mutanten jämfört med normal GluK3. Denna strukturella sammanpressning gör troligen svårare för receptorn att svänga in i en avstängningsform, vilket förklarar varför mutanten, likt zinkbundet GluK3, förblir aktiv längre. Samtidigt visade bilderna att inte alla delar av receptorn var låsta i en enda konfiguration, vilket pekar på en inneboende flexibel arkitektur som är särskilt känslig för små kemiska knuffar.
Vad detta betyder för hjärnhälsa
Tillsammans målar studien upp GluK3 inte som en enkel av-/på-brytare utan som en fininställd knutpunkt där glutamat, hjälpproteiner och zink möts. Neto1 och Neto2 bestämmer hur snabbt signaler bleknar och hur snabbt receptorer kan svara igen, medan zink antingen kan ytterligare förstärka eller under vissa omständigheter bromsa aktiviteten via flera bindningsställen. Eftersom GluK3, Neto-proteiner och zink alla samexisterar i synapser involverade i minne och är implicerade i epilepsi och psykiatriska tillstånd kan förståelsen av denna flerlagrade kontroll leda vägen för framtida terapier som varsamt finjusterar synaptisk signalering istället för att stänga av den helt.
Citering: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Nyckelord: kainatreceptorer, GluK3, Neto-proteiner, synaptiskt zink, synaptisk plasticitet