Clear Sky Science · sv
Missbruksmedicin och depression – ett fokus på epigenetik
Varför denna forskning spelar roll i vardagen
Missbruk av beroendeframkallande läkemedel och depression behandlas ofta som separata problem, men de förekommer ofta samtidigt hos samma person. Denna översikt förklarar hur långvarig användning av substanser som metamfetamin, kokain, opioider och cannabis kan lämna bestående "molekylära ärr" i hjärnan som ökar risken för depression. Genom att avslöja dessa dolda förändringar pekar artikeln mot framtida tester som kan varna för vem som är mest sårbar – och mer precisa behandlingar som kanske kan återställa skadorna i stället för att bara dämpa symtomen.
Hur beroende och låg sinnesstämning flätas samman
Författarna börjar med att beskriva den täta kliniska kopplingen mellan drogmissbruk och depression. Personer som upprepade gånger använder beroendeframkallande substanser är mycket mer benägna att rapportera långvarig sorg, förlust av lust, sömnproblem och självmordstankar. Hjärnregioner som styr belöning, motivation, minne och beslutsfattande — den ventrala tegmentala området, nucleus accumbens, prefrontala cortex och hippocampus — är centrala för båda tillstånden. Kronisk drogpåverkan rubbar hjärnans kemikalier som dopamin och serotonin, stresshormoner som kontrolleras av hypotalamus–hypofys–binjure-axeln, immunsignaler och neuroners energiförsörjning. Tillsammans gör dessa förändringar hjärnan mindre motståndskraftig mot stress och mer benägen för depressiva tillstånd, även länge efter sista dosen.
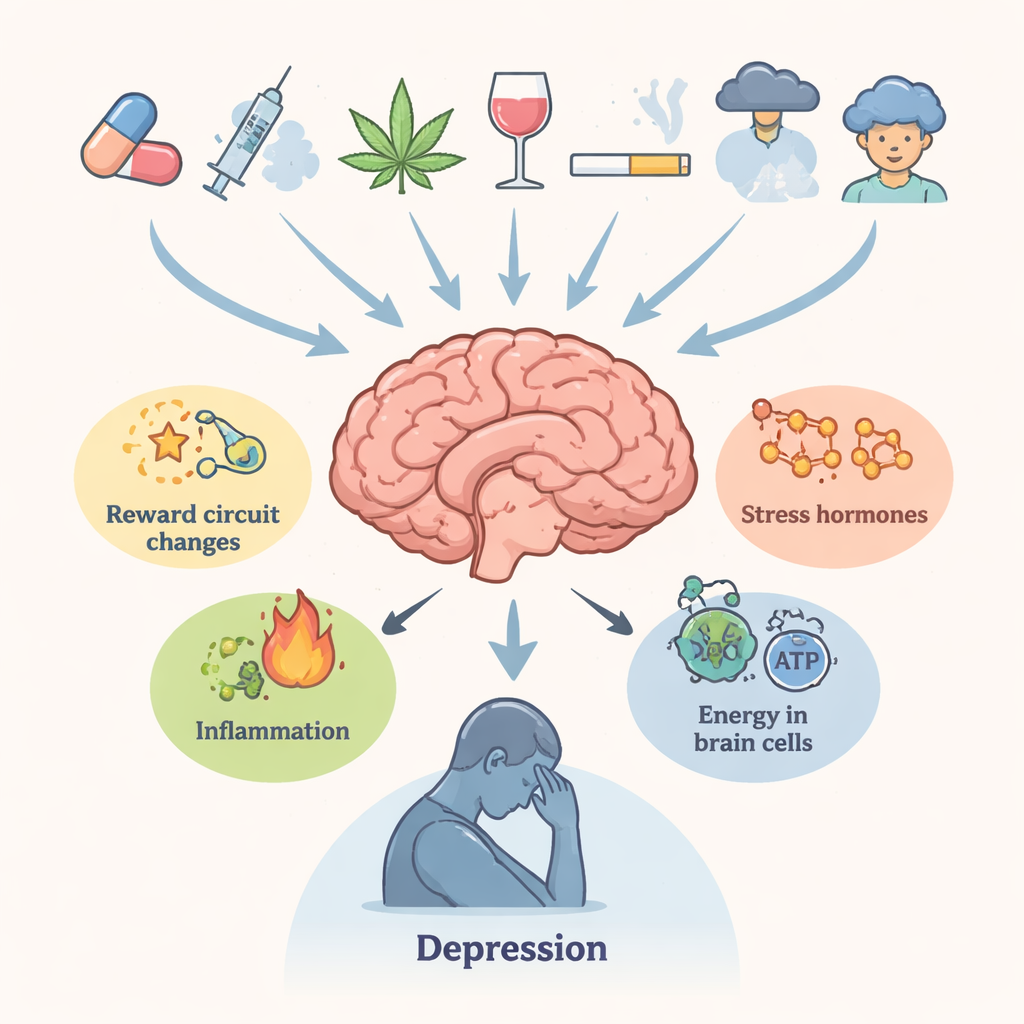
Läkemedel som omformar hjärnans kemi
Översikten går igenom flera stora drogklasser. Amfetaminliknande centralstimulerande medel och deras släktingar, inklusive syntetiska så kallade "bath salts", orsakar kraftiga dopaminpåslag och påverkan på andra transmittorer som över tid skadar nervändar, rubbar glutamatbalansen, belastar det endoplasmatiska retiklet och driver celler mot skadlig självförtäring (autofagi). Cannabisbruk i tonåren kopplas till senare depression och självmordsrisk, troligen via långvariga förändringar i cannabinoidreceptorer, vit substansstruktur och känsligheten i dopaminkretsar. Opioider, som lindrar smärta, kan utlösa inflammation, mitokondriell svikt och minskade tillväxtstödjande signaler som hjärnans neurotrofa faktor (BDNF). Kokain aktiverar upprepade gånger stressystemet och förändrar viktiga regulatorer såsom FKBP5, vilket bidrar till ångest och nedstämdhet under abstinens. I varje fall tenderar de biologiska störningarna att kvarstå, vilket hjälper till att förklara varför känslomässiga symtom kan överleva uppenbar berusning.
Epigenetik: exponeringens minne
För att förstå varför drogeffekter består fokuserar författarna på epigenetik — kemiska märkningar och molekylära brytare som justerar genaktivitet utan att förändra DNA-bokstäverna. Beroendeframkallande substanser förändrar DNA-metylering (en markering på cytosinbaser), ändrar kemiska grupper på histonproteiner som packar DNA och påverkar icke-kodande RNA som finjusterar vilka proteiner som produceras. Till exempel skiftar metamfetamin och kokain metyleringsmönster i belöningsrelaterade hjärnregioner och ändrar nivåerna av enzymer som lägger till eller tar bort dessa märkningar. Opioider och centralstimulerande medel omformar histon-acetylering och metylering på gener som styr glutamatreceptorer, stressignalering och synaptisk struktur. Dozens av microRNA, långa icke-kodande RNA och cirkulära RNA ökar eller faller vid drogpåverkan och påverkar tillsammans inflammation, neurons tillväxt och synapsers styrka. Dessa epigenetiska förändringar fungerar som ett molekylärt "minne" av drogexponering.
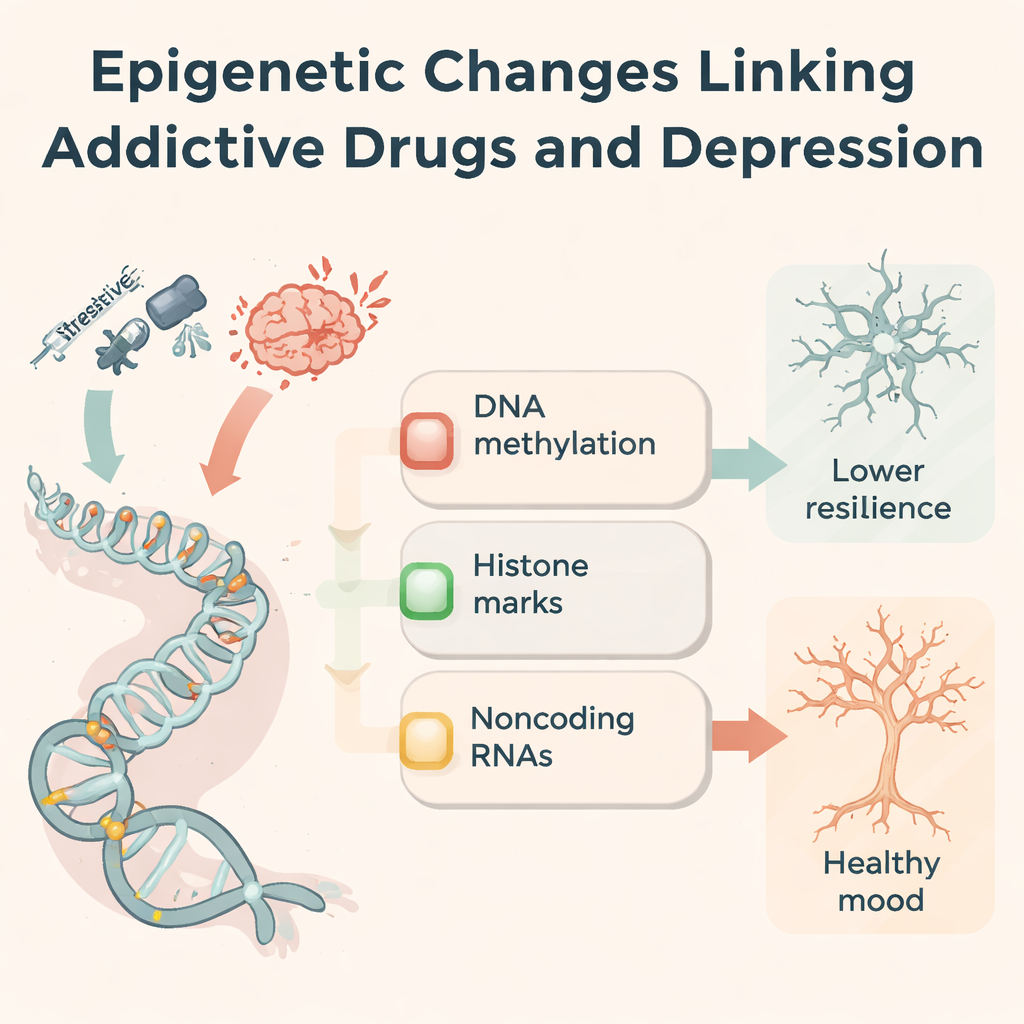
Delade molekylära vägar i depression och beroende
Samma epigenetiska maskineri syns också hos människor och djur med depression som aldrig tagit droger. Stressfyllda upplevelser kan ändra metylering av stresshormonreceptorer (såsom NR3C1 och FKBP5), sänka hjälpsamma tillväxtfaktorer som BDNF och omkoppla immunsystemet och glutamatvägar. Många av samma icke-kodande RNA som förändras av droger är också felreglerade vid depression, vilket påverkar hur nya neuroner föds, hur mikroglia reagerar på inflammation och hur starkt synapser förbinds. Författarna föreslår en trefaldig ram: reglering av stressrespons, ombyggnad av belöningskretsar och synaptisk plasticitet. Över dessa axlar konvergerar beroende och depression upprepade gånger på en liten uppsättning gener och märkningar, vilket ger en biologisk förklaring till varför de två störningarna så ofta förekommer tillsammans.
Vad detta betyder för framtida förebyggande och behandling
Avslutningsvis argumenterar översikten för att epigenetiska förändringar kan bli tidiga varningsbiomarkörer och mål för nästa generations behandlingar. Bredverkande läkemedel som suddar ut epigenetiska märkningar har redan visat vissa antidepressiva liknande effekter hos djur, men de är för grova för rutinmässig mänsklig användning. Nya verktyg — såsom CRISPR-baserade epigenomredigerare och terapier som modulerar specifika microRNA eller långa RNA — kan en dag justera problematiska gener i specifika hjärnceller medan andra sparas. Författarna varnar att mycket av dagens data kommer från g rodents och från bulkvävnad i hjärnan, och att mänsklig biologi är mer komplex. Ändå, genom att avslöja hur beroendeframkallande droger och depression skriver på samma molekylära "anteckningsbok", erbjuder arbetet en hoppfull väg mot mer personliga och bestående terapier.
Citering: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Nyckelord: missbruk och depression, epigenetik, drugmissbruk, DNA-metylering, icke-kodande RNA