Clear Sky Science · sv
Bevis för principen för NF1-genterapi i xenograftradierade musmodeller av plexiforma neurofibrom
Varför denna forskning är viktig
Personer med den ärftliga sjukdomen neurofibromatos typ 1 (NF1) utvecklar ofta stora, vanställande nervtumörer som kallas plexiforma neurofibrom. Dessa tillväxter kan orsaka smärta, rörelseproblem och stora kosmetiska bekymmer, samtidigt som dagens behandlingsmöjligheter är begränsade och operation ofta är omöjlig. Eftersom NF1 orsakas av förändringar i en enda gen har många forskare hoppats att genterapi—att åtgärda eller ersätta den felande genen—en dag skulle kunna krympa eller till och med ta bort dessa tumörer. Denna studie ger ett tidigt men kraftfullt test av den idén i möss och ställer en enkel fråga med stora konsekvenser: om man återställer den saknade NF1-genen i etablerade tumörer, försvinner de då?
Att bygga en realistisk tumörmodell i möss
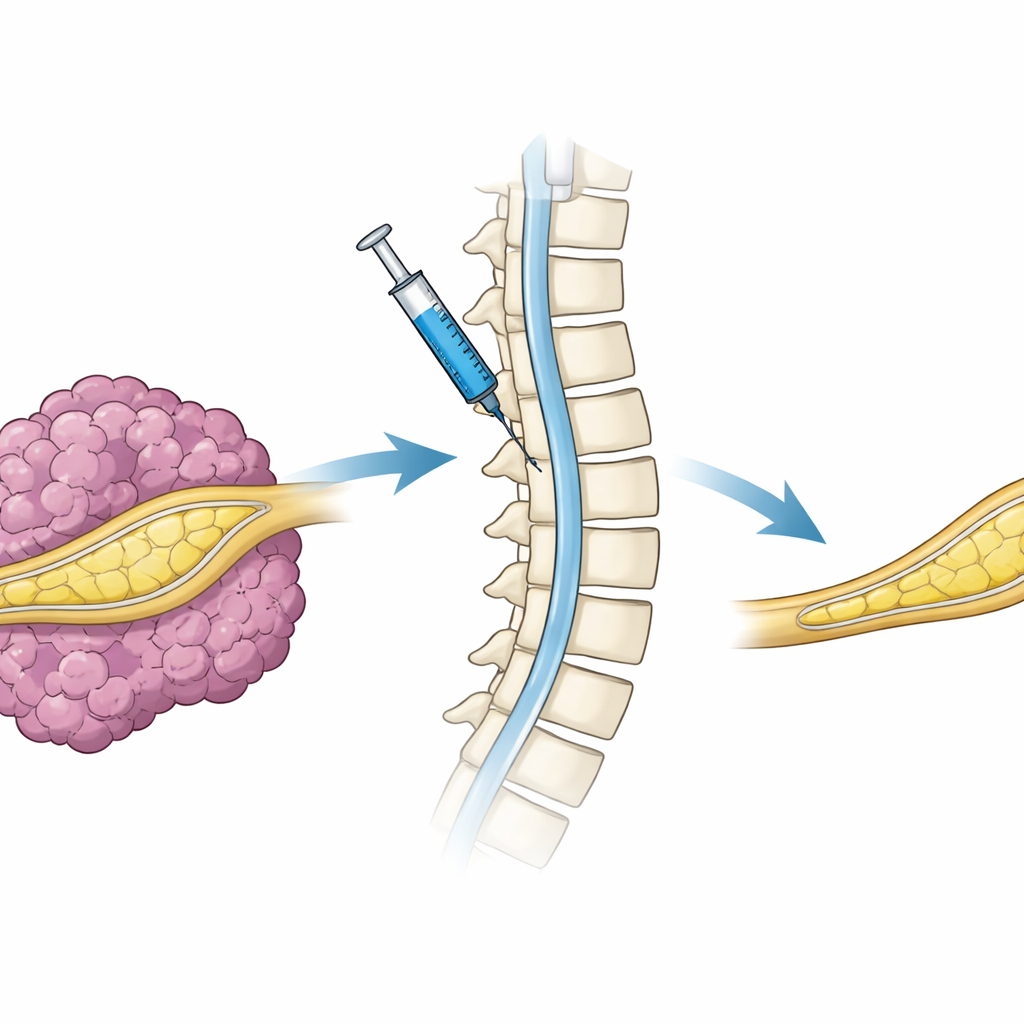
Forskarna behövde först ett laboratoriesystem som nära efterliknar mänskliga plexiforma neurofibrom. De använde mänskliga Schwann-celler, stödjecellerna som normalt omger nerver, tagna från en patient vars celler förlorat båda fungerande kopior av NF1-genen. Dessa celler placerades intill skadade ischiasnerver i immunkomprimerade möss. Under veckor utvecklade nerverna konsekvent förtjockad, mycket cellrik vävnad med oorganiserad struktur och täta kollagena band—kännetecken för plexiforma neurofibrom. Kontrolloperationer utan dessa NF1-bristande celler, eller med celler som bara bar en defekt NF1-kopia, bildade inte pålitligt tumörer. Detta visade att de mänskliga cellerna med fullständig NF1-förlust drev tumörtillväxten och skapade en robust, snabb modell för sjukdomen.
Att slå på NF1 igen i tumörcellerna
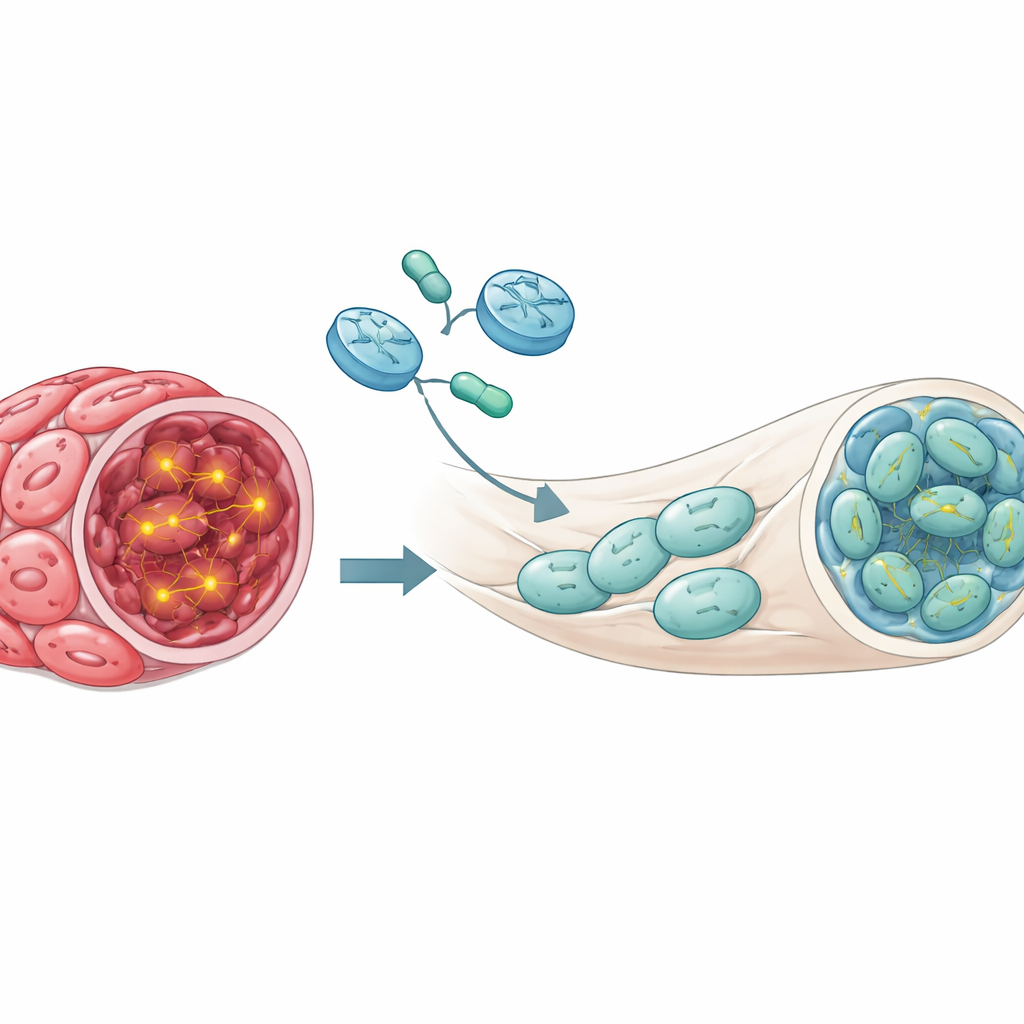
Med modellen i handen konstruerade teamet de tumörbildande Schwann-cellerna så att de bar en styrbar version av NF1-genen från möss. Omkopplaren reagerade på det vanliga antibiotikumet doxycyklin: när mössen drack vatten innehållande doxycyklin aktiverades den tillsatta NF1-genen i de implanterade cellerna. Mössen fick först tid att utveckla tumörer, och först därefter slogs genen på. Resultaten var slående. Hos djur där NF1 förblev av var majoriteten av ischiasnerverna fortfarande hem för neurofibrom. I kontrast, när NF1 återaktiverades, såg de flesta nerver normala ut under mikroskopet och kemiska markörer för överaktiv tillväxtsignalering minskade kraftigt. I praktiken tryckte återställandet av NF1 tillbaka tumörvävnaden mot ett friskt nervtillstånd.
Att vända NF1-förlusten på ett annat sätt
För att visa att effekten inte var begränsad till ett ingenjörstrick byggde forskarna en andra, kompletterande modell. Den här gången började de med mänskliga Schwann-celler som bara hade en skadad NF1-kopia—likt det som personer med NF1 ärver i alla sina celler. De lade till en genetisk brytare som tillfälligt kunde sänka den kvarvarande NF1-aktiviteten när doxycyklin fanns närvarande. När mössen drack doxycyklin föll NF1-nivåerna ytterligare och tumörer bildades lätt. Avgörande var att när doxycyklin togs bort efter att tumörer utvecklats, steg NF1-nivåerna igen och många nerver återgick mot normal struktur. Även här föll mått på tillväxtrelaterad signalering i de nerver som normaliserades. Tillsammans pekar dessa två motsatta omkopplingsstrategier—antingen att sätta på NF1 eller att släppa dess hämning—mot samma slutsats: att återställande av NF1 i tumörceller kan ångra etablerad sjukdom.
Att testa en mer realistisk leveransmetod
Bortom genetiska brytare inbyggda i celler i labbet skulle en verklig terapi behöva leverera en fungerande NF1-gen till nervsystemet hos en levande patient. För att utforska detta steg paketerade forskarna hela NF1-genen i en lentiviral vektor och injicerade den i vätskerummet runt ryggmärgen hos tumörbärande möss, en väg känd som intratekalt tillförsel. Djuren fick sedan doxycyklin så att den levererade genen skulle aktiveras. Jämfört med möss som fick ett kontrollvirus utvecklade de som behandlats med NF1-bärande virus betydligt färre tumörer, och deras nervvävnad såg mer normal ut. Även om detta var ett kort, engångsexperiment visade det att NF1-genleverans genom ryggmärgsvätskan kan nå perifera nerver och avsevärt minska tumörbördan.
Vad detta arbete betyder för personer med NF1
Denna studie erbjuder ännu ingen färdig behandling för patienter, men den svarar på en avgörande fråga: i noggrant utformade musmodeller som nära liknar mänskliga plexiforma neurofibrom kan återställande av NF1 i tumörceller krympa eller normalisera etablerade tumörer. Arbetet ger bevis för principen att NF1-genterapi är en trovärdig strategi, inte bara ett teoretiskt hopp. Många utmaningar återstår—att hitta de säkraste och mest effektiva leveransfordonen, fastställa hur mycket NF1-aktivitet som krävs och testa långtidsverkningar i mer naturliga modeller. Ändå lägger dessa resultat en vetenskaplig grund för framtida genbaserade behandlingar som en dag kan ge bestående lindring från plexiforma neurofibrom hos personer med NF1.
Citering: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
Nyckelord: neurofibromatos typ 1, genterapi, plexiformt neurofibrom, Schwann-celler, lentiviral leverans