Clear Sky Science · sv
Heterogenitet mellan VIP- och GRP-neuroner underligger AVP-receptorsignalering i musens suprachiasmatiska kärna
Varför vår kroppsklocka är så svår att ställa om
Alla som vinglat av ett långflyg eller kämpat med nattarbete vet att vår inre klocka inte gillar plötsliga tidsscheman. Denna artikel tar upp en mycket specifik fråga i kärnan av det problemet: varför känner vissa nervceller i hjärnans huvudklocka starkt av ett tidsignal medan deras grannar till stor del ignorerar det? Genom att följa en enskild kemisk signal genom denna lilla klockkrets hos möss identifierar författarna en dold undergrupp av celler som hjälper bestämma hur envis vår kroppsklocka är när den möter “jetlag.” 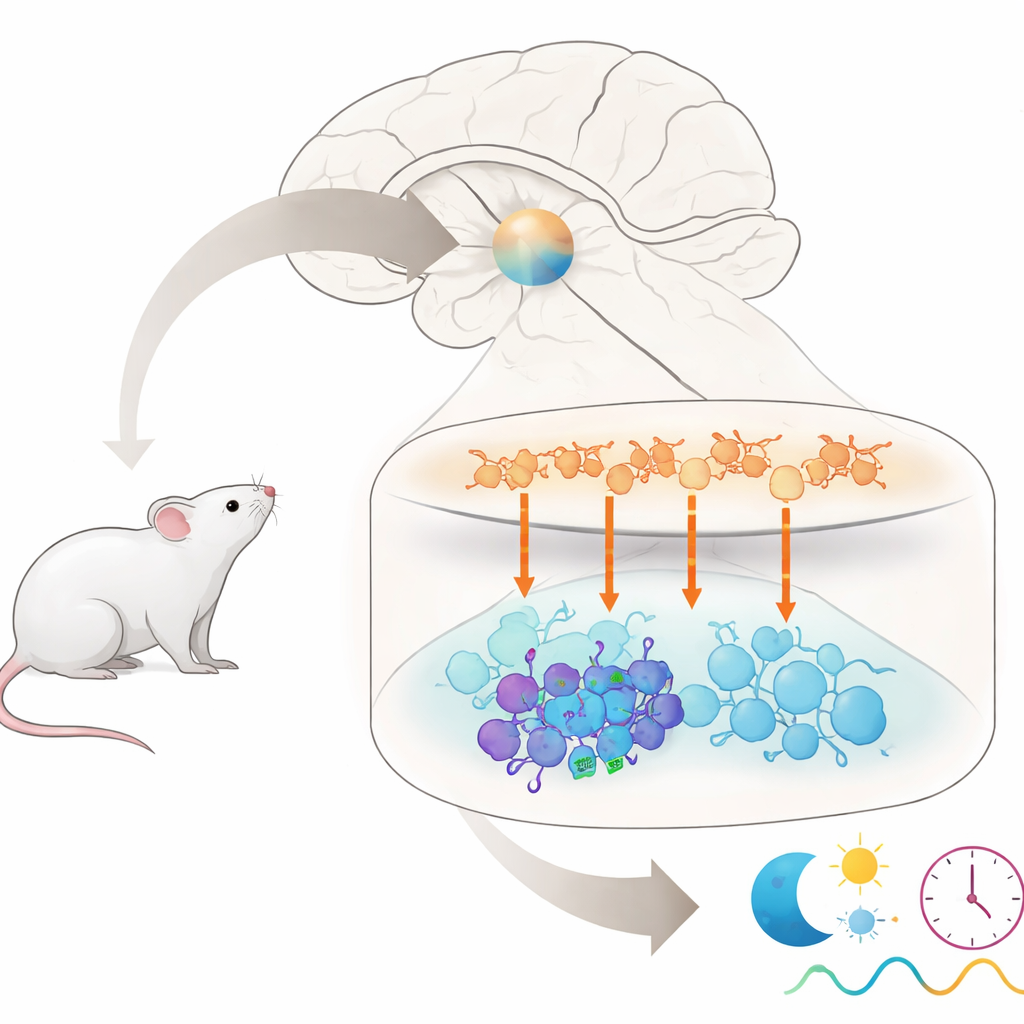
En liten klocka med många olika aktörer
Huvudklockan hos däggdjur ligger i en liten region i hjärnan kallad suprachiasmatisk kärna, eller SCN. Trots att den innehåller bara omkring 20 000 nervceller är den uppdelad i flera distinkta grupper som kommunicerar med varandra via olika kemiska budbärare. Celler i det övre “skal”-området frisätter främst en budbärare kallad argininvasopressin (AVP), medan celler i det undre “kärn”-området ofta frisätter andra budbärare, inklusive vasoaktivt intestinalpeptid (VIP) och gastrinfrisättande peptid (GRP). Tillsammans måste dessa grupper hålla sig synkroniserade för att generera de 24-timmarsrytmer som styr sömn, hormonfrisättning och många andra kroppsfunktioner. Men vilka exakt i kärnan som lyssnar på signaler från AVP-cellerna i skalet har varit oklart.
Följa kopplingarna från sändarceller till mottagarceller
Forskarna kartlade först hur skalets AVP-celler fysiskt kopplar till VIP- och GRP-celler i kärnan. De använde ett virus för att märka de utgående fibrerna och möjliga kontaktpunkter hos AVP-neuroner i möss, och färgade sedan hjärnskivor för att se var dessa fibrer slutade. De fann att AVP-fibrer bildade uppenbara kontaktställen på både VIP- och GRP-celler, men i olika proportioner: ungefär en fjärdedel av VIP-cellerna och mer än hälften av GRP-cellerna visade dessa appositioner. Detta visade att AVP-neuroner når båda typer av kärnceller, men avslöjade ännu inte vilka som faktiskt svarar på signalen. För att testa detta använde teamet optogenetik—aktivering av AVP-neuroner med blått ljus—och sökte efter c-Fos, en markör för cellulär aktivering, i VIP- och GRP-neuroner.
En liten VIP-undergrupp som verkligen “hör” AVP
När AVP-neuronerna stimulerades med ljus aktiverades många AVP-celler själva med c-Fos, som väntat. Viktigt var att en liten undergrupp av VIP-celler i kärnan också visade c-Fos-aktivering, trots att de inte uttryckte det ljuskänsliga proteinet direkt. Detta indikerade att de drevs indirekt av AVP-påverkan. I kontrast visade GRP-celler sällan c-Fos, trots att de mottog AVP-kontakter. Författarna sökte sedan efter genbudskapet för AVP-receptorn känd som V1a i dessa populationer med känsliga RNA-avbildningsmetoder. De upptäckte att V1a fanns endast i en minoritet av VIP-celler och knappt var detekterbar i GRP-celler. Således verkar en liten V1a-positiv undergrupp bland de många VIP-neuronerna vara särskilt inställd för att ta emot och svara på AVP-signaler, medan de flesta GRP-neuroner inte gör det. 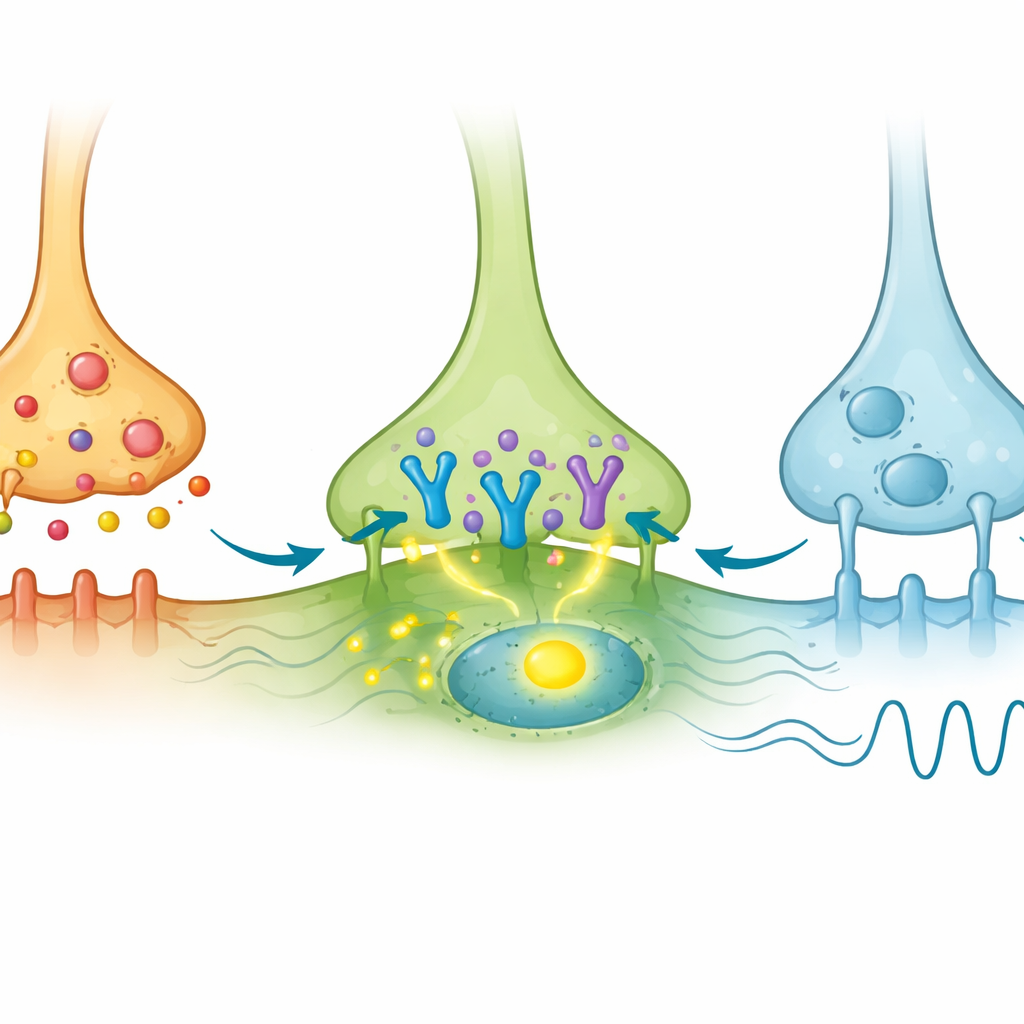
Hur en liten cellgrupp formar återhämtningen från jetlag
För att undersöka funktionen hos dessa V1a-bärande VIP-neuroner skapade forskarna möss där V1a-receptorn togs bort enbart från VIP-celler. Dessa djur bibehöll en normal dygnsrytm i konstant mörker, vilket visar att denna receptor i VIP-celler inte behövs för att sätta klockans grundläggande takt. När ljus–mörker-schemat däremot plötsligt försköts framåt eller bakåt med åtta timmar för att efterlikna jetlag justerade de modifierade mössen sina aktivitetsmönster snabbare än sina normala kullsyskon, särskilt efter förskjutningar framåt och hos hanmöss. I andra experiment hade borttagning av V1a över hela hjärnan eller specifikt i SCN gett liknande “jetlag-resistent” beteende. De nya resultaten tyder alltså på att en förvånansvärt liten grupp VIP-neuroner som bär V1a-receptorer kan ha ett oproportionerligt stort inflytande på hur stel eller flexibel den övergripande klockan är.
Vad detta betyder för vår tidsuppfattning
I vardagstermer visar studien att inom hjärnans centrala klocka fungerar AVP-producerande neuroner som tidhållare i ett övre skikt, och sänder signaler via V1a-receptorer till ett utvalt fåtal VIP-neuroner i det undre skiktet. Dessa få VIP-celler hjälper hela nätverket att motstå plötsliga förändringar i ljus–mörkercykeln och bromsar hur snabbt klockan ställer om sig efter ett skifte. Att ta bort deras AVP-känsliga receptor gör systemet mer villigt att skifta, vilket underlättar jetlagnliknande anpassningar hos möss. Genom att kartlägga denna dolda mångfald bland klockneuroner ger arbetet en mer detaljerad kopplingskarta över hur vår inre tidsuppfattning stabiliseras—och antyder att selektiv påverkan av liknande vägar hos människor en dag kan hjälpa till att hantera jetlag eller andra rytmrubbningar.
Citering: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Nyckelord: circadiansk klocka, suprachiasmatisk kärna, vasopressin-signalering, VIP-neuroner, jetlag