Clear Sky Science · sv
Mitochondriellt energifel som ligger bakom FLVCR1-relaterad sensorisk neuropati
När smärtnerver får slut på kraft
Vissa personer föds nästan utan förmåga att känna smärta. Vid första anblick kan det låta som en välsignelse, men det blir snabbt en förbannelse: utan smärta som varningssignal får de brännskador, frakturer, infektioner och till och med blindhet. Denna studie undersöker en sällsynt form av sådana smärt- och känselbortfallsstörningar och avslöjar en överraskande bov: de små kraftverken inne i nervcellerna vars energiproduktion går allvarligt fel.
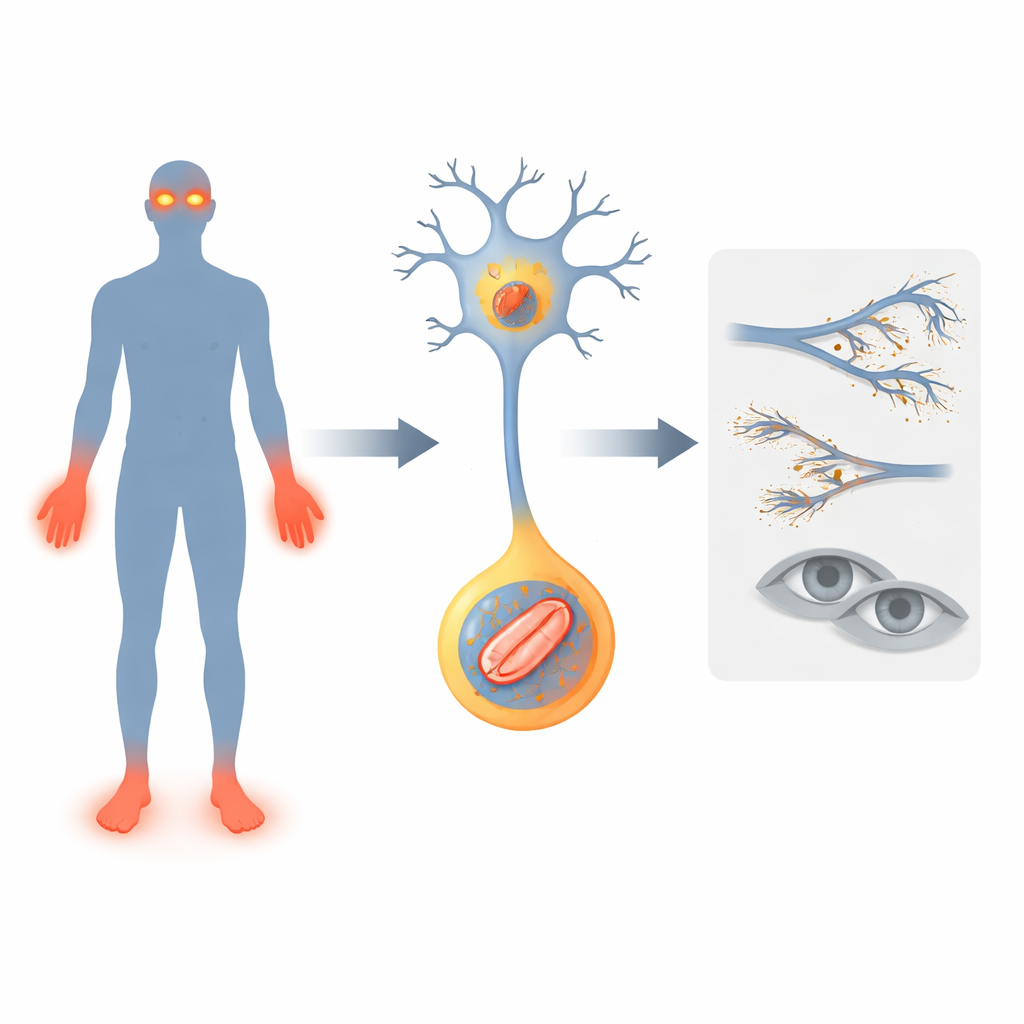
Ett genfel som tystar larmklockorna
Forskarnas fokus ligger på en gen kallad FLVCR1, redan kopplad till sällsynta nervtillstånd där personer förlorar smärtkänsel, får ostadig gång och ibland progressiv synnedsättning. De beskriver två nya patienter med förändringar i FLVCR1. Båda barnen visade tidiga problem: försenade motoriska milstolpar, frekventa fall, djupa infektioner och amputationer av fingrar och tår eftersom skador gick obemärkta förbi. Den ena utvecklade också en degenerativ ögonsjukdom kallad retinitis pigmentosa, vilket ledde till nattblindhet. Dessa fall vidgar bilden av hur FLVCR1-defekter kan yttra sig hos människor och stärker idén att genen är viktig för att bevara smärtrelaterade nerver och ljuskänsliga celler i näthinnan.
Att modellera sjukdomen i små fiskar
För att utforska hur FLVCR1 påverkar utvecklande sensoriska nerver vände teamet sig till zebrafisk, vars genomskinliga embryon tillåter direkt observation av nervceller. De minskade nivåerna av fiskens motsvarighet till genen, flvcr1a, med genetiska verktyg. Fiskar med sänkt flvcr1a hade färre dorsalrotganglier, kluster av neuroner som upptäcker beröring och smärta längs ryggraden. Beteendemässigt rörde sig dessa fiskar mindre av egen drift och simmade bara korta sträckor när deras svans försiktigt rördes vid, vilket tyder på en försvagad sensorisk respons. Eftersom tidigare musmodeller dog för tidigt för att kunna analysera deras sensoriska nerver, ger dessa zebrafiskar det första levande systemet där FLVCR1-relaterade nervdefekter och beteende kan följas i detalj.
Tre problemvägar konvergerar på cellernas kraftverk
FLVCR1 sitter i cellmembran och hanterar flera nyckelsubstanser. Tidigare arbete har antytt roller i hantering av kolin (en byggsten för membranlipider), hem (det järnhaltiga pigmentet som driver många enzymer) och kalciumflöde mellan cellens kompartiment. Forskarna samlade hudceller (fibroblaster) från fyra patienter med olika FLVCR1-mutationer och jämförde dem med celler från friska personer och symtomfria bärare. De fann att patientceller hade lägre kolinnivåer och mer flytande cellmembran, förändringar som kan rubba det känsliga lipidmiljö som mitokondrierna behöver. De upptäckte också att ett avgörande enzym för hemproduktion inne i mitokondrierna, ALAS1, var mindre aktivt, även om det totala heminnehållet såg nästan normalt ut. Samtidigt var de fysiska kontaktställena mellan det endoplasmatiska retikulumet och mitokondrierna—där kalcium normalt flödar in i mitokondrierna—kortare och mindre frekventa, och kalciumupptaget i mitokondrierna var minskat. Tre problem—kolinbrist, trög hemproduktion och försvagat kalciumöverförande—pekar alla mot nedsatt mitokondriell funktion.
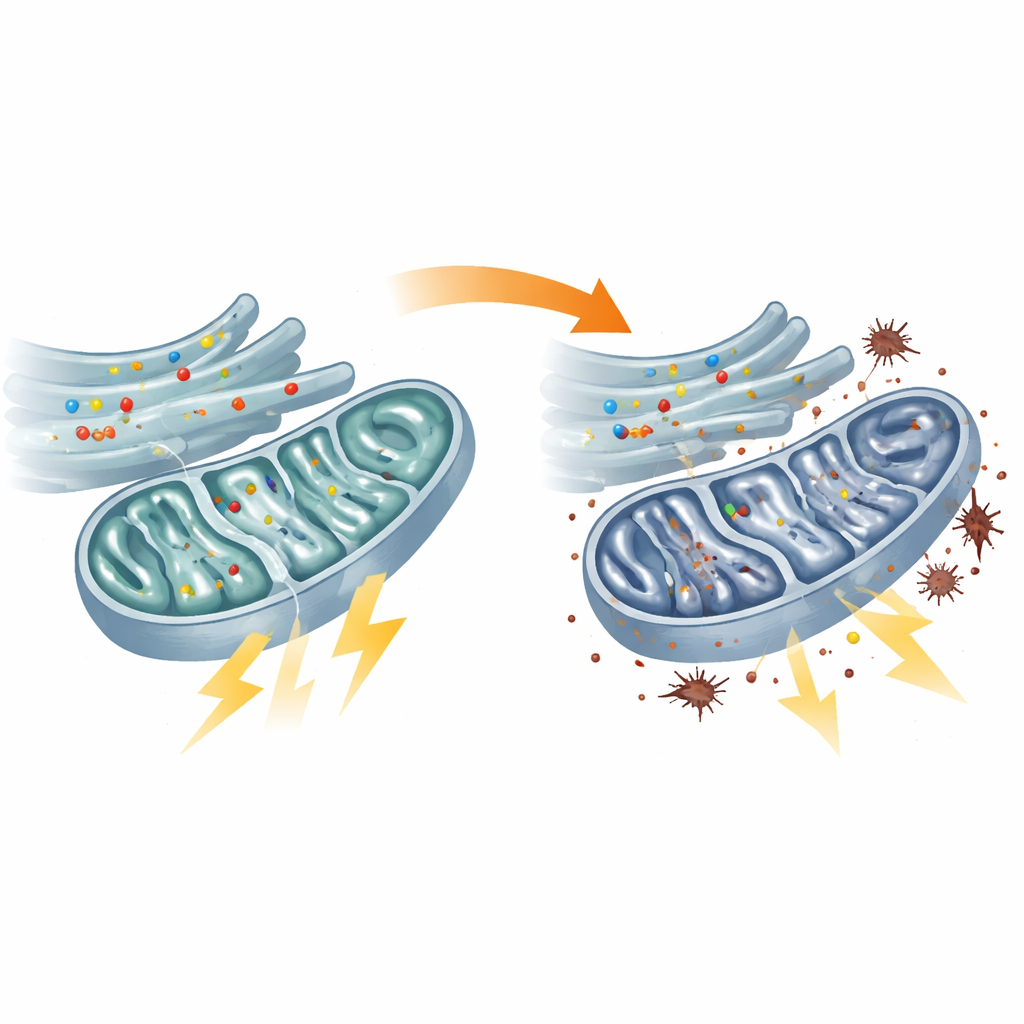
Utsvultna mitokondrier och överbelastade reservsystem
Direkta tester av energimetabolismen bekräftade att mitokondrierna i patienternas fibroblaster presterade under förväntan. Den centrala bränslebearbetande hubben, TCA-cykeln, gick långsammare, flera av dess nyckelenzymer var mindre aktiva och reaktionskedjan som normalt omvandlar bränsle till ATP, cellens energivaluta, var dämpad. Som ett resultat föll ATP-nivåerna inne i mitokondrierna. Cellerna försökte kompensera genom att öka glykolysen, en mindre effektiv, sockerförbrännande väg utanför mitokondrierna. Denna omställning i energistrategi hade en kostnad: elektroner läckte från den pressade mitokondriella maskineriet och utlöste högre nivåer av lipidperoxidation, en form av oxidativ skada på cellmembran. Liknande defekter sågs i zebrafisk med reducerat flvcr1a, vilket kopplar mitokondriellt fel direkt till djurmodellen för sensorisk neuropati.
Vinkar om framtida behandlingar genom att stärka cellenergin
Uppmuntrande nog kunde några av dessa defekter mildras i laboratoriet. När teamet konstgjort ökade kalciuminflödet i mitokondrier genom att överuttrycka en kanalprotein kallad MCU i patientceller, återhämtade sig energiproduktionen och tecken på oxidativ skada sjönk. Tillförsel av en hemförlängare, 5-aminolevulinsyra (ALA), förbättrade också TCA-cykelns aktivitet, respirationskedjans funktion och ATP-nivåer, även om långvarig ALA-exponering varit skadlig i tidigare studier. Extra kolin normaliserade membranfluiditeten och hjälpte till att minska lipidskador, men gav endast blygsamma kortsiktiga vinster i energiproduktion. Dessa räddningsförsök antyder att ingen enskild väg ensam ansvarar; istället pressar ett nätverk av störd kolin-, hem- och kaliumhantering mitokondrierna in i kronisk underprestation.
Varför dessa fynd betyder något för patienter
Genom att följa konsekvenserna av FLVCR1-mutationer från molekyler till celler till hela organismer föreslår detta arbete att energifel i mitokondrier är en drivande kraft bakom denna form av smärtlös neuropati och dess associerade synproblem. Sensoriska nerver och fotoreceptorer är ovanligt energikrävande eftersom de upprätthåller långa axoner eller kontinuerligt förnyar ljuskänsliga strukturer, vilket gör dem särskilt sårbara när mitokondriellt utflöde sviktar. Studiets zebrafiskmodell och patienthärledda celler erbjuder nu praktiska testplattformar för terapier som stärker mitokondriell metabolism. Medan behandlingar som kolintillskott, kontrollerad hämförstärkning eller läkemedel som ökar mitokondriellt kalciumupptag kommer att kräva noggrann utvärdering i djurmodeller och kliniska prövningar, är budskapet klart: att återställa kraftförsörjningen i sköra neuroner kan en dag hjälpa till att skydda människor födda utan naturens viktigaste varningssignal—smärta.
Citering: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
Nyckelord: sensorisk neuropati, mitokondriell dysfunktion, FLVCR1, smerteinsensitivitet, nervenergiomsättning