Clear Sky Science · sv
Strukturella grunder för fladdermusreceptors igenkänning av SARS-CoV-2 och SARS2-liknande koronavirus från fladdermöss
Varför den här fladdermus–virus-berättelsen fortfarande spelar roll
COVID-19-pandemin började för mer än sex år sedan, men forskare pusslar fortfarande ihop hur viruset som orsakar den, SARS-CoV-2, blev så effektivt på att infektera människor. Ett centralt mysterium är hur detta virus, och dess nära släktingar som hittats hos fladdermöss, fäster vid ett protein som kallas ACE2 på cellernas yta — ett första och avgörande steg för infektion. Att förstå dessa mikroskopiska lås-och-nyckel-interaktioner kan klargöra varifrån viruset kom, hur det anpassade sig och vad som kan hända om närbesläktade virus hoppar över till människor framöver. 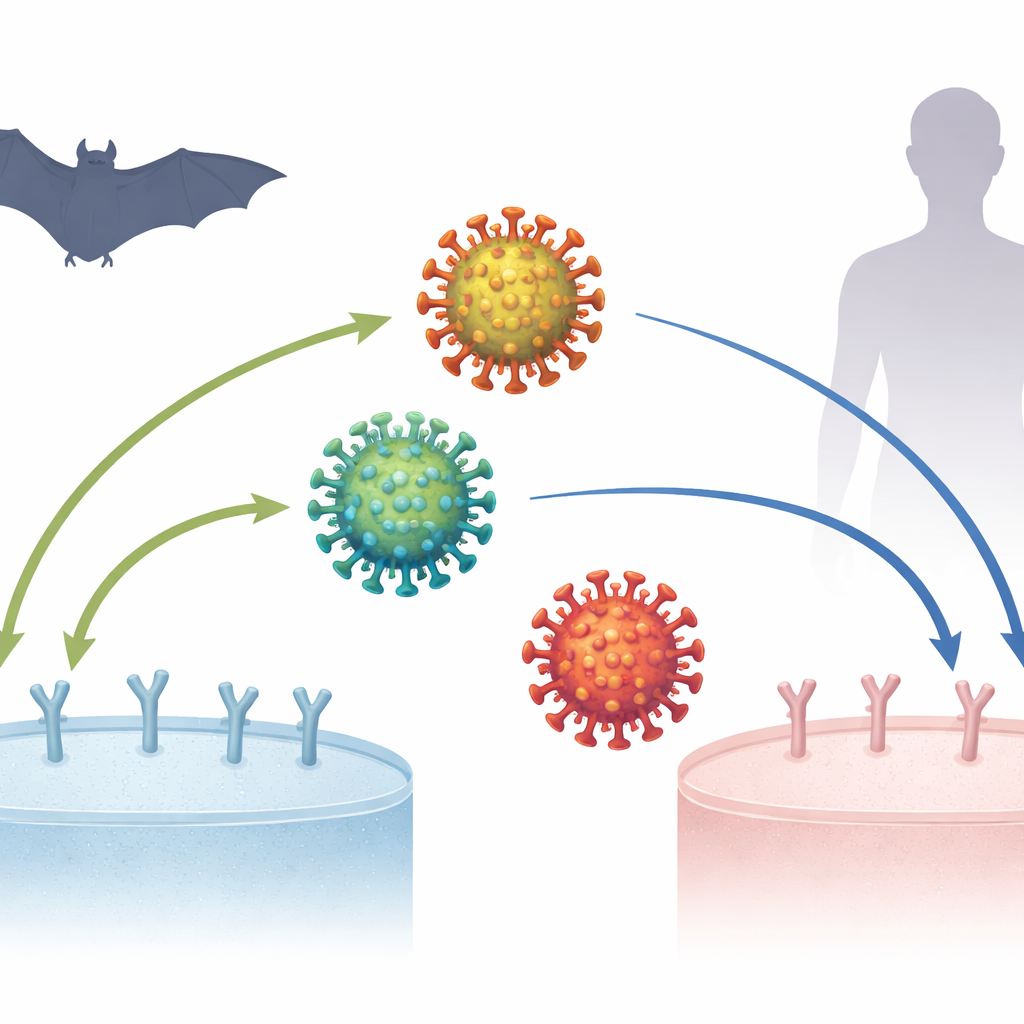
Att granska virusets handslag
Studien fokuserar på spikeproteinet, den kronliknande strukturen på virusets yta som greppar ACE2. En liten region av spiken, receptorbindande domänen (RBD), fungerar som ett fingertoppsliknande grepp som tar tag i ACE2:s ”dörrhandtag”. Tidigare arbete visade att när koronavirus hoppar mellan arter — till exempel från fladdermöss till djur som civetter och vidare till människor — plockar RBD ofta upp mutationer som förbättrar dess grepp om den nya värdens ACE2. Men SARS-CoV-2 utgjorde ett pussel: dess ursprungliga form band redan mycket väl till mänskligt ACE2, även innan mycket tid hunnit gå för anpassning, och vissa fladdermusvirus nära SARS-CoV-2 verkade binda mänskligt ACE2 bättre än fladdermuss-ACE2. Detta fick vissa att undra om SARS-CoV-2 kunde vara ett undantag från de vanliga evolutionära reglerna.
Att testa fladdermus- och mänskliga receptorer
För att undersöka detta mysterium granskade forskarna två fladdermuskoronavirus nära SARS-CoV-2, kända som BANAL-52 och BANAL-236. De jämförde hur starkt RBD:erna från dessa virus och från SARS-CoV-2 fäste vid ACE2 från människor och från flera fladdermusarter. Med cellbaserade bindningsassay, högprecisions-biosensormätningar och infektionsprov med ofarliga ”pseudovirus” fann de ett tydligt mönster. BANAL-52:s RBD band starkast till ACE2 från en fladdermusart, Rhinolophus sinicus, och något svagare till mänskligt ACE2. SARS-CoV-2:s RBD, däremot, visade en måttlig preferens för mänskligt ACE2 framför fladdermus-ACE2. Sammantaget grep BANAL-52:s RBD både fladdermus- och mänskliga receptorer hårdare än SARS-CoV-2:s, men var mest finjusterad för just den fladdermusens ACE2. 
Hur en atomskalig justering tippar vågskålen
Forskargruppen gick sedan vidare till röntgenkristallografi, som visar strukturer på atomnivå, för att se exakt hur virusets ”finger” och ACE2:s ”dörrhandtag” rör vid varandra. De fokuserade på två nyckelpositioner: en på det virala RBD (kallad rest 498) och en på ACE2 (rest 41). I BANAL-52 använder både den virala platsen och fladdermus-ACE2 samma byggsten, histidin, vilket möjliggör en mycket tät, lagerliknande interaktion — stapling som två mynt och dessutom bildande av en vätebindning. I mänskligt ACE2 bär samma position en närbesläktad men något annorlunda byggsten, tyrosin, som fortfarande staplar bra med BANAL-52:s histidin men saknar den extra vätebindningen. SARS-CoV-2 använder i stället glutamin vid denna virala position, vilket inte kan stapla på samma sätt, vilket resulterar i svagare bindning till både fladdermus- och mänskligt ACE2. Genom att avsiktligt byta dessa aminosyror i fladdermus-ACE2 bekräftade forskarna att förstärkning eller försvagning av just denna kontaktpunkt kunde växla vilken virusstam eller värd som gynnades.
Varför mänskligt ACE2 är en så välkomnande dörr
Bortom denna enskilda kontakt frågade författarna varför mänskligt ACE2 i allmänhet är en så effektiv port för koronavirus. Genom att jämföra fladdermus- och mänskligt ACE2 sida vid sida identifierade de flera människospecifika drag som förbättrar virusets handslag. Två positioner på mänskligt ACE2, innehållande aminosyrorna histidin (vid plats 34) och metionin (vid plats 82), skapar starkare vätebindningar och fettiga ”fläckar” som hjälper RBD att lägga sig mer bestämt. En annan mänsklig rest, treonin vid plats 27, gör bindningen något svagare än i fladdermusvarianten, men sammantaget vinner de tillsatta gynnsamma kontakterna. Dessa detaljer stämmer med tidigare arbete som visar att mänskligt ACE2 har flera ”hotspots” som naturligt gör det till en attraktiv receptor för ett brett spektrum av koronavirus.
Omformulera ursprungshistorien
När alla data sätts ihop argumenterar studien för att SARS-CoV-2 och dess fladdermusrelaterade virus fortfarande följer det vanliga evolutionära manuskriptet. BANAL-52:s spike verkar bäst anpassad till ACE2 från vissa fladdermöss, samtidigt som den också är kompatibel med mänskligt ACE2. SARS-CoV-2:s spike är i sin tur bättre inställd på mänskligt ACE2 än på fladdermus-ACE2, hjälpt av särskilda kontaktpunkter på den mänskliga receptorn. Små förändringar på bara några positioner — särskilt vid den virala rest 498 och närliggande platser — kan förskjuta balansen av vilken värd som gynnas. För icke-specialister är slutsatsen att det inte finns något behov av att åberopa exotiska förklaringar: välkända, väletablerade strukturella principer för protein–protein-interaktion är tillräckliga för att förklara hur dessa virus känner igen fladdermus- och människoceller, och de stöder en nära evolutionär koppling mellan SARS-CoV-2 och närbesläktade fladdermuskoronavirus.
Citering: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Nyckelord: SARS-CoV-2 evolution, bat coronaviruses, ACE2 receptor, virus host range, spike protein binding