Clear Sky Science · sv
Afrikansk svinpestvirus–kodad proteinet MGF 505–3R försvagar medfödd immunitet via ubiquitin–medierad nedbrytning av MyD88
Varför detta spelar roll för djurhälsa och mer därtill
Afrikansk svinpest har härjat bland grisfarmer världen över, hotat livsmedelsförsörjningen och orsakat enorma ekonomiska förluster. Viruset är dödligt delvis därför att det smyger förbi kroppens tidiga varningssystem. Denna studie avslöjar hur ett viralt protein, kallat MGF 505–3R, diskret saboterar en viktig larmknapp inne i cellerna och visar att en liten fragment av detta protein också kan omvandlas till ett kraftfullt antiinflammatoriskt verktyg hos möss.
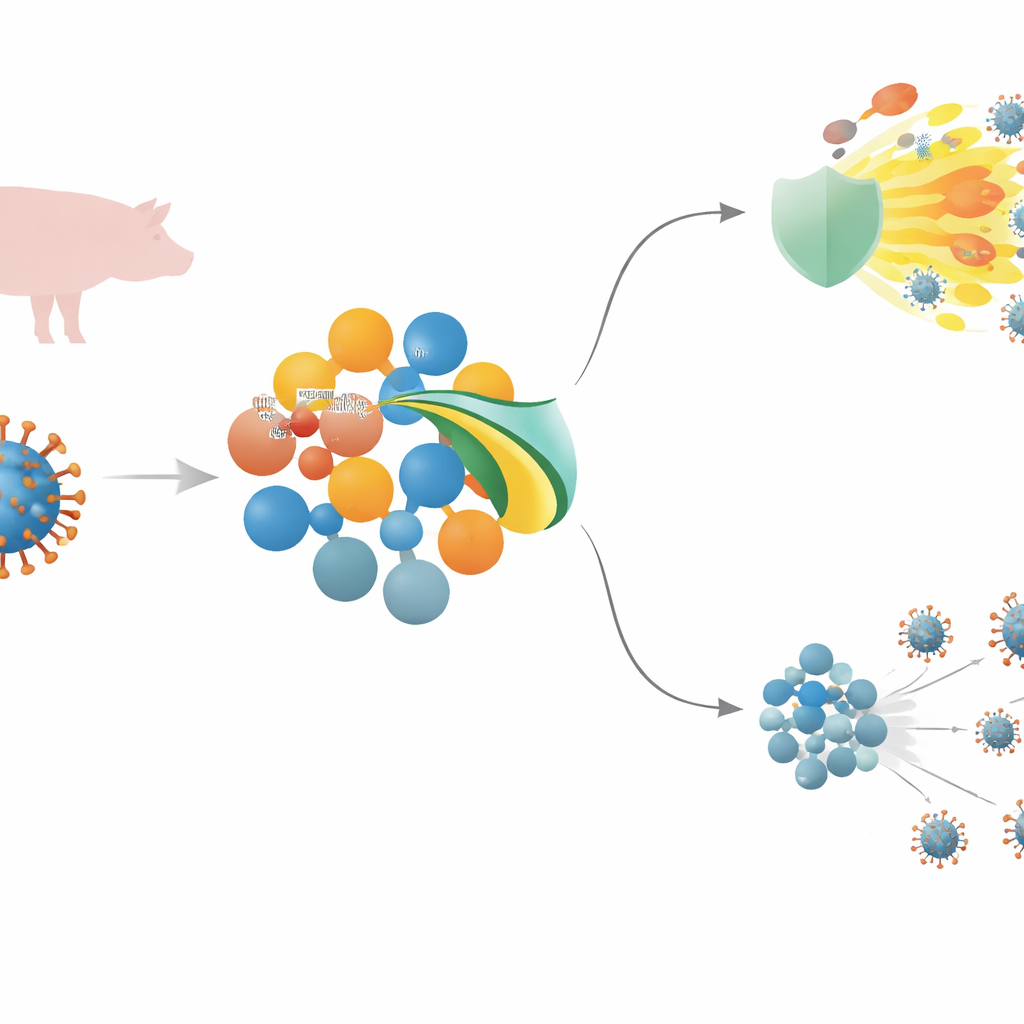
Ett dödligt grisvirus och kroppens första försvarslinje
Afrikansk svinpestvirus (ASFV) är ett stort DNA-virus som kan döda nästan varje infekterad gris. För att vinna mark måste det överlista den medfödda immuniteten — det snabba, första försvaret som upptäcker inkräktare och utlöser inflammation och antivirala molekyler. Centralt i detta svar står en signalväg som inkluderar sensorer på cellytan, ett reläprotein kallat MyD88 och en huvudregulator känd som NF–κB, vilka tillsammans driver produktionen av inflammatoriska budbärare och antivirala interferoner. ASFV bär många gener som tros störa dessa signaler, men för flera av dem, inklusive MGF 505–3R, var deras exakta metoder inte väl förstådda.
Hur viruset kapar ledningarna till immunlarmet
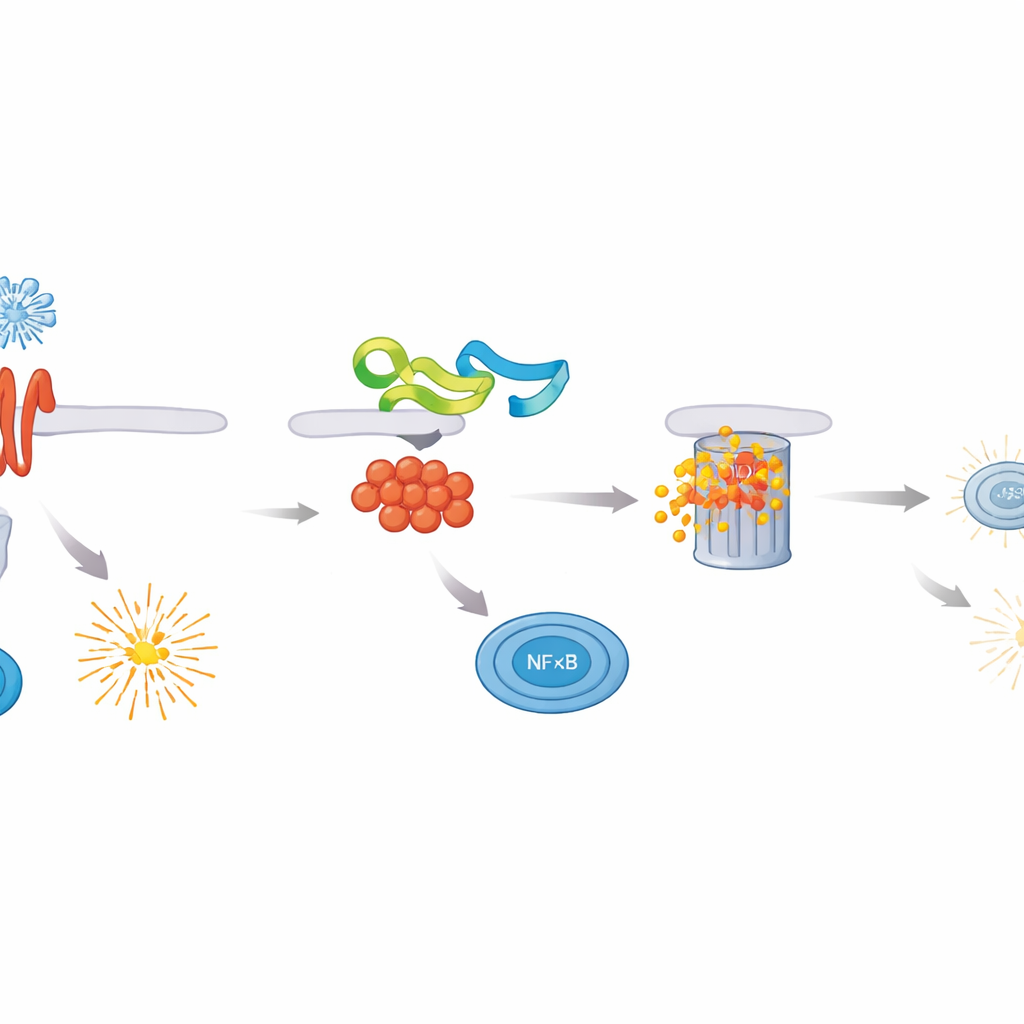
Forskarlaget screenade ASFV-proteiner för deras förmåga att dämpa NF–κB-aktivitet och fann att MGF 505–3R var en särskilt stark hämmare. När detta virala protein var närvarande producerade celler som utsattes för olika immunstimuli betydligt färre inflammatoriska cytokiner och mycket lägre nivåer av typ I- och typ III-interferoner. Närmare granskning visade att MGF 505–3R verkar direkt på MyD88, den centrala adaptorn som kopplar många immunsensorer till NF–κB. MGF 505–3R binder MyD88 och märker det för borttagning via cellens protein-nedbrytningsmaskineri, med en form av märkning kallad K48-bundet ubiquitin. När MyD88 bryts ned lyckas inte NF–κB flytta in i kärnan och aktivera skyddande gener, vilket lämnar cellerna mer mottagliga för virusets tillväxt.
Zooma in på ett litet men kraftfullt proteinfragment
För att lokalisera den avgörande delen av MGF 505–3R skapade teamet förkortade versioner av proteinet och testade deras effekter. De upptäckte att aminosyrorna 89–277 var både nödvändiga och tillräckliga för att binda MyD88, främja dess ubiquitinering och blockera NF–κB-aktivering. Med hjälp av datorbaserade strukturförutsägelser skar de ut två korta peptider från detta område. En av dem, pep3R–1, utmärkte sig: den minskade kraftigt NF–κB-aktivitet, blockerade fosforylering och nukleär translokation av NF–κB-subenheten p65, och sänkte uttrycket av inflammatoriska cytokiner och interferoner i immunceller stimulerade med flera farosignaler. I cellkultur dämpade både fullängds MGF 505–3R och pep3R–1 inte bara antiviralt signalering utan möjliggjorde också att ett testvirus replikerade mer effektivt, vilket betonar hur potent denna väg är för att kontrollera infektioner.
Att omvandla ett viralt knep till potentiell medicin
Teamet undersökte sedan om peptiden kunde utnyttjas för att stilla skadlig inflammation snarare än att hjälpa virus. I en musmodell för kolit utlöstad av kemikalien DSS förlorar djuren normalt vikt, utvecklar blodig diarré och visar svåra skador och infiltration av immunceller i kolon. Möss behandlade med pep3R–1 klarade sig avsevärt bättre: sjukdomspoängen var lägre, tarmarna var längre och friskare, och mikroskopisk undersökning visade bevarad vävnadsarkitektur med avsevärt färre inflammatoriska celler. Nivåerna av viktiga inflammatoriska molekyler såsom TNF–α, IL–1β, IL–6 och ett enzym kopplat till vita blodkroppsinflux var alla reducerade i kolontissue och blod. I ett separat experiment minskade pep3R–1 också den inflammatoriska responsen mot ett systemiskt bakteriellt toxin, vilket indikerar att den kan dämpa både lokal och kroppsomfattande inflammatoriska stormar.
Vad detta betyder för grisar, människor och framtida behandlingar
Denna studie visar att ASFV-proteinet MGF 505–3R hjälper viruset att frodas genom att demontera ett centralt immunrelä, MyD88, och därigenom stänga av både inflammatoriska och interferonberoende försvar. Samtidigt kan ett litet fragment av detta virala protein, pep3R–1, omdisponeras för att säkert dämpa överdriven inflammation hos möss, inklusive i en tarmsjukdomsmodell. Även om mycket återstår att göra—såsom att förbättra stabilitet, leverans och tester i fler sjukdomssammanhang—avslöjar studien både en kritisk svag punkt som antivirala strategier kan rikta in sig på och en lovande ritning för att utforma nya peptidbaserade antiinflammatoriska läkemedel inspirerade av viralt immunsmuggling.
Citering: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Nyckelord: Afrikansk svinpest, medfödd immunitet, NF-kappaB, MyD88, antiinflammatorisk peptid