Clear Sky Science · sv
Onormal järnhomeostas orsakar skada på kokleära hårceller och hörselförlust hos Gprasp2‑deficienta möss
Varför detta spelar roll för vardaglig hörsel
Hörselnedsättning ses ofta som enkel "slitage", men för många drivs den av dolda genetiska defekter. Denna studie avslöjar hur en sällan studerad gen, GPRASP2, hjälper till att skydda de känsliga ljudkännande cellerna i innerörat från järninducerad skada. Genom att visa exakt vad som går fel när genen saknas öppnar arbetet dörrar för mer precisa diagnoser och framtida behandlingar av ärftliga hörselproblem och möjligen relaterade humörstörningar.
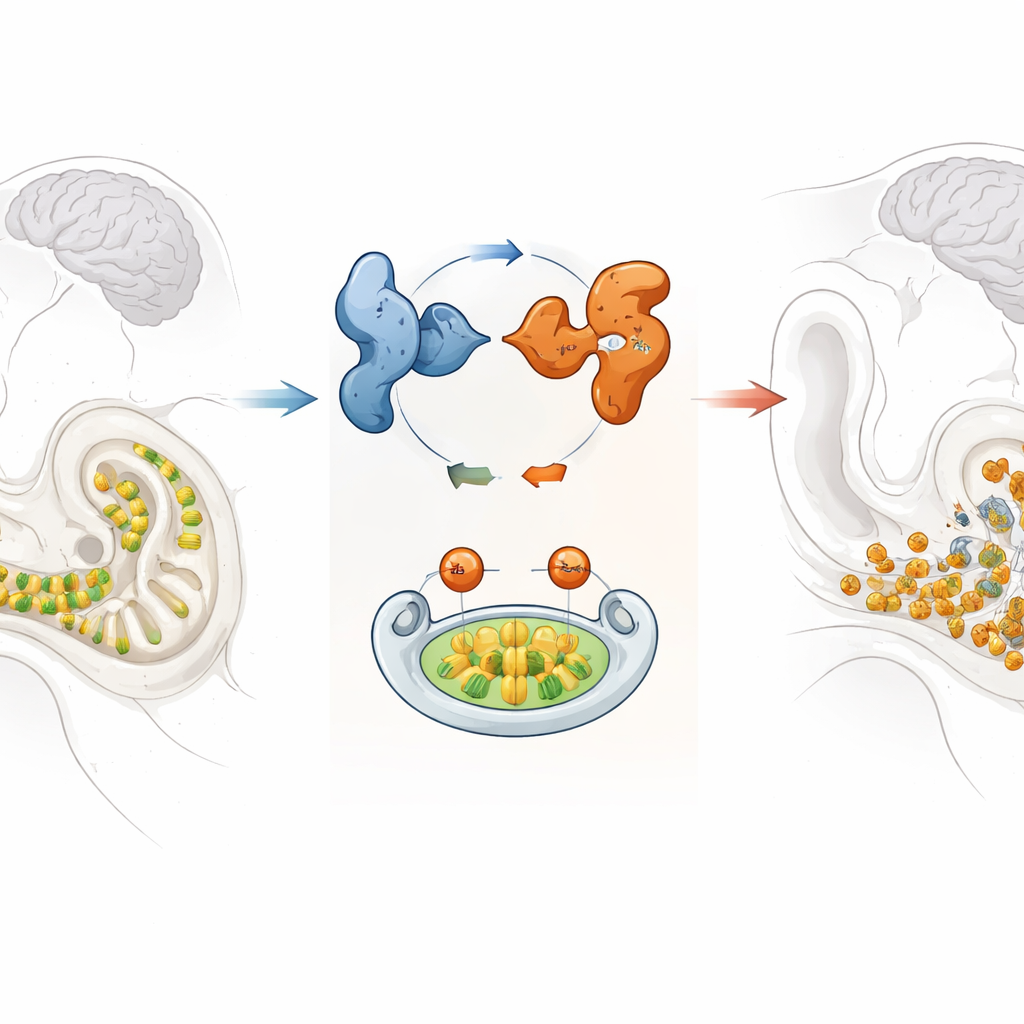
En bräcklig ljudsensor i innerörat
Inne i den snurrade koklean sitter rader av hårceller som omvandlar små vibrationer till elektriska signaler som hjärnan kan tolka. När dessa hårceller väl är borta växer de inte tillbaka, så att bevara deras hälsa är avgörande för livslång hörsel. Forskarna fokuserade på GPRASP2, en gen som tidigare hittats muterad i en familj med X‑bundet syndromiskt hörselnedsättning, vilket innebär att tillståndet främst drabbar män och kan komma med ytterligare symtom. Även om GPRASP2 var känd för att vara aktiv i hjärnan och innerörat var dess exakta roll i hörseln tidigare oklar.
Vad som händer när genen saknas
För att efterlikna det mänskliga tillståndet använde teamet CRISPR‑genredigering för att skapa möss som saknar en fungerande kopia av Gprasp2‑genen. Dessa djur visade tydlig hörselnedsättning över ett brett frekvensområde vid känsliga elektriska mätningar från hörselnerven. Deras svar på plötsliga höga ljud var dämpade, medan balans och motorik var i stort sett normala, vilket tyder på ett specifikt hörselproblem snarare än en generell rörelsestörning. Intressant nog uppvisade mössen även depressionsliknande beteenden i flera standardtester, vilket antyder att denna gen kopplar samman hörsel och humör genom sina funktioner i både öra och hjärna.
Skador inne i koklean
När forskarna granskade inneröronen hos Gprasp2‑deficienta möss fann de att många yttre hårceller saknades eller satt fel, och att de återstående cellerna ofta hade förvrängda buntar av små projektioner som normalt fungerar som stämgafflar. De såg också förändringar i stria vascularis, en mycket aktiv vävnad som upprätthåller den speciella vätske‑ och elektriska miljön som krävs för hörsel. På mikroskopisk nivå var markörer för celldöd och oxidativ stress förhöjda i de yttre hårcellerna och närliggande nervceller, vilket indikerar att dessa strukturer var hårt angripna av reaktiva molekyler och hade ökad sannolikhet att dö.
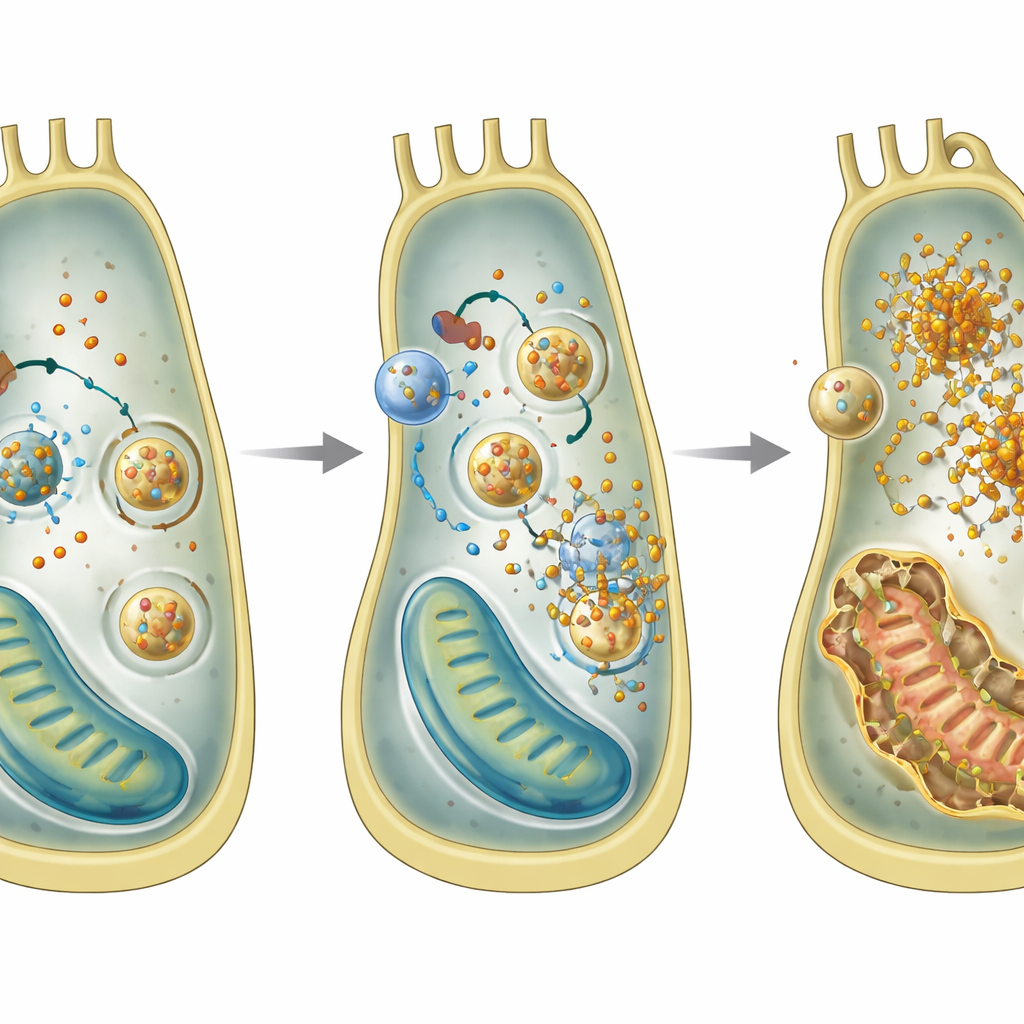
Järnöverskott och okontrollerad återvinning
Djupare analyser i en innerörats cellinje visade vad som går fel inne i enskilda celler utan GPRASP2. De upptäckte ett mönster kännetecknande för en form av celldöd kallad ferroptos, driven av järn och lipidperoxidation. Celler utan Gprasp2 ackumulerade mer järn i sin tvåvärt form, producerade fler reaktiva syrearter, hade lägre nivåer av antioxidantet glutation och visade skadade mitokondrier. Gen‑ och proteinanalyser pekade på ökad ferritinofagi, en process där järnlagrande partiklar levereras till återvinningskompartment och bryts ned, vilket frigör extra järn i cellen. Att blockera detta återvinningssteg minskade järnuppbyggnaden och stödjer idén att överdriven ferritinofagi är central för skadan.
En nyckelpartnerprotein som håller järnet i schack
Forskarna frågade sedan hur GPRASP2 styr denna järnhantering. Genom att kartlägga proteiner som interagerar med GPRASP2 identifierade de NCAM1, ett celladhesionsmolekyl mest känt för sina roller i lärande, minne och humör. De visade att GPRASP2 fysiskt binder till NCAM1, och att förlust av GPRASP2 gör att NCAM1‑nivåerna sjunker i hårceller och i odlade auditiva celler. Låg NCAM1 kopplades till ökad ferritinofagi och järnöverskott. Återställande av NCAM1 i Gprasp2‑deficienta celler minskade järnnivåerna och dämpade viktiga regulatorer av ferritinofagi, även om generell autofagi förblev aktiv. Detta tyder på att GPRASP2 finjusterar en specifik järnåtervinningsväg via NCAM1, snarare än att slå på eller av hela återvinningssystemet.
Vad detta betyder för hörseln och vidare
Enkelt uttryckt visar arbetet att GPRASP2 fungerar som en säkerhetsansvarig för järn inne i kokleära hårceller. När GPRASP2 finns samarbetar det med NCAM1 för att förhindra att för mycket lagrat järn släpps tillbaka i cellen och därigenom begränsa oxidativ skada. När genen störs rubbas järnhanteringen, cellerna rostar inifrån och viktiga hårceller dör, vilket leder till hörselförlust. Eftersom GPRASP2 och NCAM1 också verkar i hjärnan kan samma väg bidra till att förklara humörförändringar som ses hos vissa patienter. Att förstå denna järnbaserade felmekanism ger ett tydligt mål för framtida läkemedel eller genterapier som syftar till att bevara hörseln hos personer med GPRASP2‑relaterade eller liknande genetiska sjukdomar.
Citering: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Nyckelord: ärftlig hörselnedsättning, kokleära hårceller, järnhomeostas, ferroptos, GPRASP2